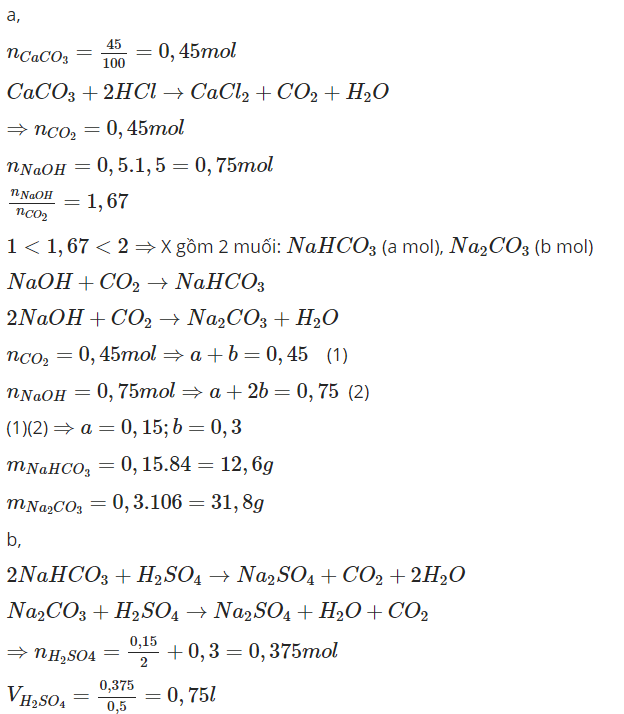Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1,
Có \(m_{ct_{NaOH}}=\frac{200.10}{100}=20g\)
\(\rightarrow n_{NaOH}=\frac{m}{M}=\frac{20}{40}=0,5mol\)
\(n_{CO_2}=\frac{V}{22,4}=\frac{5,6}{22,4}=0,25mol\)
Lập tỷ lệ \(T=\frac{n_{NaOH}}{n_{CO_2}}\)
\(\rightarrow T=\frac{0,5}{0,25}=2\)
Vậy sản phẩm là muối trung hoà duy nhất là \(Na_2CO_3\)
PTHH: \(2NaOH+CO_2\rightarrow Na_2CO_3+H_2O\)
Phản ứng xảy ra hết bởi vì \(\frac{n_{NaOH}}{2}=n_{CO_2}\)
\(\rightarrow n_{Na_2CO_3}=0,25mol\)
\(\rightarrow m_{Na_2CO_3}=0,25.106=26,5g\)
2,
a. Có \(n_{CO_2}=\frac{V}{22,4}=\frac{16,8}{22,4}=0,75mol\)
\(600ml=0,6l\)
\(n_{NaOH}=C_M.V=0,6.2=1,2mol\)
Xét tỷ lệ số mol \(T=\frac{n_{NaOH}}{n_{CO_2}}\)
\(\rightarrow T=\frac{1,2}{0,75}=1,6\)
\(\rightarrow1< T< 2\)
Vậy sản phẩm tạo thành hai muối là \(NaHCO_3;Na_2CO_3\)
Với PTHH có sản phẩm là \(Na_2CO_3\) đặt a là số mol của \(CO_2\)
Với PTHH có sản phẩm là \(NaHCO_3\) đặt b là số mol của \(CO_2\)
\(2NaOH+CO_2\rightarrow Na_2CO_3+H_2O\left(1\right)\)
\(NaOH+CO_2\rightarrow NaHCO_3\left(2\right)\)
Do vậy \(\hept{\begin{cases}2a\left(mol\right)=n_{NaOH}\left(1\right)\\b\left(mol\right)=n_{NaOH}\left(2\right)\end{cases}}\)
Có các biểu thức về số mol
\(∑n_{CO_2}=0,75mol\)
\(\rightarrow a+b=0,75\left(3\right)\)
\(∑n_{NaOH}=1,2mol\)
\(\rightarrow2a+b=1,2\left(4\right)\)
Từ (3) và (4), có hệ phương trình
\(\hept{\begin{cases}a+b=0,74\\2a+b=1,2\end{cases}}\)
\(\rightarrow\hept{\begin{cases}a=0,45mol\\b=0,3mol\end{cases}}\)
Thay số mol vào (1) \(\rightarrow m_{Na_2CO_3}=0,45.106=47,7g\)
Thay số mol vào (2) \(\rightarrow m_{NaHCO_3}=0,3.84=25,2g\)
Vậy tổng khối lượng mối trong dung dịch A sẽ là: \(m_A=m_{Na_2CO_3}+m_{NaHCO_3}=25,2+47,7=72,9g\)
b. Vì \(Na_2CO_3\) tác dụng với \(BaCl_2\) nên ta có
PTHH: \(BaCl_2+Na_2CO_3\rightarrow BaCO_3\downarrow+2NaCl\)
\(n_{BaCO_3}=n_{Na_2CO_3}=0,45mol\)
\(\rightarrow m_{BaCO_3}=0,45.197=88,65g\)

Theo đề bài ta có : \(\left\{{}\begin{matrix}nCO2=\dfrac{16,8}{22,4}=0,75\left(mol\right)\\nNaOH=0,6.2=1,2\left(mol\right)\end{matrix}\right.\)
Ta xét tỉ lệ :
T = \(\dfrac{nNaOH}{nCO2}=\dfrac{1,2}{0,75}=1,6< 2\)
Ta có : 1 < T < 2 => Dung Dịch A gồm 2 muối là Na2CO3 và NaHCO3
a) Gọi x ,y lần lượt là số mol của CO2 tham gia vào 2 PT :
Ta có PTHH :
\(\left(1\right)CO2+2NaOH\rightarrow Na2CO3+H2O\)
xmol............2xmol..........xmol
\(\left(2\right)CO2+NaOH\rightarrow NaHCO3\)
ymol............ymol..........ymol
Ta có Hệ PT : \(\left\{{}\begin{matrix}x+y=0,75\left(a\right)\\2x+y=1,2\left(b\right)\end{matrix}\right.\) => \(\left\{{}\begin{matrix}x=0,45\\y=0,3\end{matrix}\right.\) => \(\left\{{}\begin{matrix}nNa2CO3=nCO2\left(1\right)=x=0,45\left(mol\right)\\nNaHCO3=nCO2\left(2\right)=y=0,3\left(mol\right)\end{matrix}\right.\) => \(\left\{{}\begin{matrix}mNa2CO3=0,45.106=47,7\left(g\right)\\mNaHCO3=0,3.84=25,2\left(g\right)\end{matrix}\right.\) => mA = 47,7 + 25,2 = 72,9 (g)
b) Ta có :
Na2CO3 + BaCl2 ---> BaCO3\(\downarrow\) + 2NaCl
0,45mol..........................0,45mol
=> m(KT)=mBaCO3 = 0,45.197=88,65(g)

\(n_{CaO}=\dfrac{2,8}{56}=0,2\left(mol\right)\)
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
0,2 0,2
a. \(n_{CO_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
0,075 0,075
vì \(\dfrac{0,075}{1}< \dfrac{0,2}{1}\) => dd \(Ca\left(OH\right)_2\) dư sau pứ.
=> \(m_{CaCO_3}=0,075.100=7,5\left(g\right)\)
b. \(n_{CaCO_3}=\dfrac{1}{100}=0,01\left(mol\right)\)
Thấy: \(n_{CaCO_3}< n_{Ca\left(OH\right)_2}\)
Nên ta có 2 trường hợp.
TH 1: \(dd.Ca\left(OH\right)_2.dư\)
Có:
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
0,1 0,1
m muối tạo thành là m kt = 1 (g)
\(V_{CO_2}=0,1.22,4=2,24\left(l\right)\)
TH 2: khí \(CO_2\) dư
Có:
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
0,2 0,2 0,2
\(CO_2+CaCO_3+H_2O\rightarrow Ca\left(HCO_3\right)_2\)
0,1 0,1 0,1
\(m_{muối}=m_{CaCO_3}+m_{Ca\left(HCO_3\right)_2}=1+0,1.162=17,2\left(g\right)\)
\(V_{CO_2}=0,3.22,4=6,72\left(l\right)\)

a)
Do A và B đều là kim loại hóa trị II nên ta sử dụng phương pháp trung bình coi A và B là một chất gọi là X
=> CT chung của 2 muối là XCO3
Ta có nCO2 = \(\dfrac{1,12}{22,4}\) = 0,05 ( mol )
XCO3 + H2SO4 → XSO4 + H2O + CO2
0,05 <---- 0,05 <---0,05 <-- 0,05 < -0,05
bảo toàn khối lượng ta có
mXSO4 = mXCO3 + mH2SO4 - mH2O - mCO2
= 4,68 + ( 98 . 0,05 ) - ( 18 . 0,05 ) - ( 44 . 0,05 )
= 6,48 ( gam )
b) MXCO3 = mXCO3 : nXCO3 = 4,68 : 0,05 = 93,6
=> X = 93,6 - 12 - 16 . 3 = 33,6
có nACO3 : nBCO3 = 2 : 3
và nACO3 + nBCO3 = 0,05
=> nACO3 = 0,02 và nBCO3 = 0,03
=> nA = 0,02 và nB = 0,03
=> ( 0,02 . A + 5 : 3 . 0,03 . B) / 0,05 = 33,6
=> A = 24 ( là magie - Mg ) do B = A . 5 :3
=> B = 40 ( là canxi - Ca )
=> mMgCO3 = 1,68 ( gam )
=> %mMgCO3 = \(\dfrac{1,68}{4,68}\) . 100 \(\approx\) 36 %
=> %mCaCO3 = 100 - 36 = 64%

\(n_{CaCO_3}=\dfrac{45}{100}=0,45\left(mol\right)\\ n_{NaOH}=0,5.1,5=0,75\left(mol\right)\\ CaCO_3+2HCl\rightarrow CaCl_2+CO_2+H_2O\\ n_{CO_2}=n_{CaCO_3}=0,45\left(mol\right)\\ Vì:1< \dfrac{n_{NaOH}}{n_{CO_2}}=\dfrac{0,75}{0,45}=\dfrac{5}{3}< 2\\ \Rightarrow Sp:Na_2CO_3,NaHCO_3\\ Đặt:n_{Na_2CO_3}=a\left(mol\right);n_{NaHCO_3}=b\left(mol\right)\left(a,b>0\right)\\ \Rightarrow\left\{{}\begin{matrix}2a+b=0,75\\a+b=0,45\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,3\\b=0,15\end{matrix}\right.\\ \Rightarrow ddX:m_{Na_2CO_3}=0,3.106=31,8\left(g\right);m_{NaHCO_3}=84.0,15=12,6\left(g\right)\)

1.
\(n_{CO_2}=\dfrac{2.24}{22.4}=0.1\left(mol\right)\)
\(n_{Ca\left(OH\right)_2}=0.075\left(mol\right)\)
\(T=\dfrac{0.1}{0.075}=1.33\)
=> Tạo ra 2 muối
\(n_{CaCO_3}=a\left(mol\right),n_{Ca\left(HCO_3\right)_2}=b\left(mol\right)\)
Khi đó :
\(a+b=0.075\)
\(a+2b=0.1\)
\(\Rightarrow\left\{{}\begin{matrix}a=0.05\\b=0.025\end{matrix}\right.\)
\(m_{sp}=0.05\cdot100+0.025\cdot162=9.05\left(g\right)\)
2.
\(n_{CO_2}=\dfrac{1.12}{22.4}=0.05\left(mol\right)\)
\(n_{Ba\left(OH\right)_2}=0.2\cdot0.2=0.04\left(mol\right)\)
\(T=\dfrac{0.005}{0.04}=1.25\)
=> Tạo ra 2 muối
\(n_{BaCO_3}=a\left(mol\right),n_{Ba\left(HCO_3\right)_2}=b\left(mol\right)\)
Ta có :
\(a+b=0.04\)
\(a+2b=0.05\)
\(\Rightarrow\left\{{}\begin{matrix}a=0.03\\b=0.01\end{matrix}\right.\)
\(m_{BaCO_3}=0.03\cdot197=5.91\left(g\right)\)

a) \(BaCl_2+H_2SO_4\rightarrow BaSO_4\downarrow+2HCl\)
b) \(n_{BaCl_2}=\dfrac{52}{208}=0,25\left(mol\right)\)
PTHH: \(BaCl_2+H_2SO_4\rightarrow BaSO_4\downarrow+2HCl\)
0,25----->0,25------->0,25---->0,5
=> \(m_{H_2SO_4}=0,25.98=24,5\left(g\right)\)
=> \(m_{ddH_2SO_4}=\dfrac{24,5.100}{19,6}=125\left(g\right)\)
c) \(m_{BaSO_4}=0,25.233=58,25\left(g\right)\)
d)
\(n_{NaOH}=\dfrac{8}{40}=0,2\left(mol\right)\)
PTHH: \(NaOH+HCl\rightarrow NaCl+H_2O\)
Xét tỉ lệ \(\dfrac{0,5}{1}>\dfrac{0,2}{1}\) => NaOH hết, HCl dư
=> Quỳ tím chuyển màu đỏ