Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Na + H2O ---> NaOH + 1/2H2;
x x x/2
NaOH + HCl ---> NaCl + H2O;
0,1 0,1
Dung dịch X gồm NaCl và NaOH dư;
Số mol NaOH dư = x - 0,1 mol; lượng NaOH dư được trung hòa bằng 0,02 mol HCl nên: x - 0,1 = 0,02 hay x = 0,12 mol.
Vậy: m = 23.0,12 = 2,76 g; V = 0,06.22,4 = 1,344 lít.

Hòa tan hỗn hợp 1,69g Oleum có công thức H2SO4.3SO3 vào nước dư. Trung hòa dung dịch thu được Vml dung dịch KOH 1M. Giá trị của V là:
A.20
B.40
C.30
D.10
Giải thích:
\(H2SO4.3SO3+H2O=4H2SO4\)
\(n\left(o\le um\right)=0.005mol\)
\(\Rightarrow nH2SO4=0.005.4=0.02mol\)
\(H2SO4+2KOH=K2SO4+H2O\)
\(\Rightarrow nKOH=0.04\)
\(\Rightarrow\) Giá trị của V là: 40

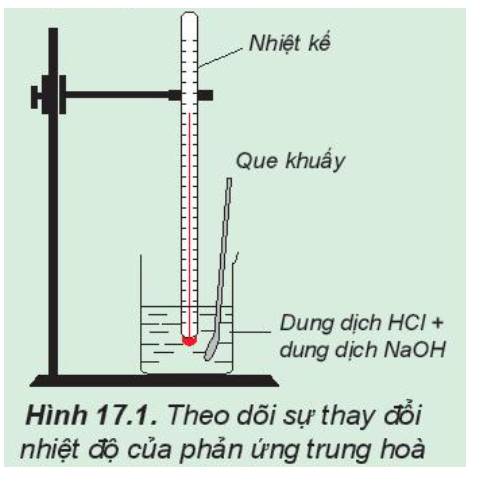
1.
Phản ứng hóa học: NaOH + HCl → NaCl + H2O
Nhiệt độ đo được (HCl) lúc ban đầu thấp hơn so với nhiệt độ sau phản ứng
=> Phản ứng trung hòa là phản ứng tỏa nhiệt
2.
Trong thí nghiệm trên, nếu thay các dung dịch HCl và NaOH bằng các dung dịch loãng hơn thì nhiệt độ sau phản ứng vẫn tăng nhưng tăng ít hơn so với thí nghiệm trên.

a,\(n_{Na}=\dfrac{4,6}{23}=0,2\left(mol\right)\)
PTHH: 2Na + 2H2O → 2NaOH + H2
Mol: 0,2 0,2 0,1
\(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
b,\(C_{M_{ddNaOH}}=\dfrac{0,2}{0,5}=0,4M\)

PTHH: R + 2HCl ---> RCl2 + H2 (1)
Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
\(n_{HCl}=\dfrac{100}{1000}.5=0,5\left(mol\right)\)
Ta thấy: \(\dfrac{0,2}{1}< \dfrac{0,5}{2}\)
Vậy HCl dư.
Theo PT(1): \(n_R=n_{H_2}=0,2\left(mol\right)\)
=> \(M_R=\dfrac{4,8}{0,2}=24\left(g\right)\)
Vậy R là magie (Mg)
PT: Mg + 2HCl ---> MgCl2 + H2 (2)
Ta có: \(m_{dd_{MgCl_2}}=4,8+\dfrac{100}{1000}-0,2.2=4,5\left(lít\right)\)
Theo PT(2): \(n_{MgCl_2}=n_{H_2}=0,2\left(mol\right)\)
=> \(C_{M_{MgCl_2}}=\dfrac{0,2}{4,5}=\dfrac{2}{45}M\)

Đáp án:
8,625 g
Giải thích các bước giải:
nCl2=22,4/22,4=1 mol
nNaOH=0,1x2=0,2 mol
nCa(OH)2=0,1x0,5=0,05 mol
2NaOH+Cl2->NaCl+NaClO+H2O
0,2 0,1 0,1
2Ca(OH)2+2Cl2->CaCl2+Ca(ClO)2+2H2O
0,05 0,05 0,025
m=0,025x111+0,1x58,5=8,625 g

\(n_{KMnO_4}=\frac{15,8}{158}=0,1\left(mol\right)\)
PTHH : \(2KMnO_4+16HCl-->2KCl+2MnCl_2+5Cl_2+8H_2O\) (1)
\(Cl_2+H_2-as->2HCl\) (2)
Có : \(m_{ddHCl}=100\cdot1,05=105\left(g\right)\)
=> \(m_{HCl}=105-97,7=7,3\left(g\right)\)
=> \(n_{HCl}=\frac{7,3}{36,5}=0,2\left(mol\right)\)
BT Clo : \(n_{Cl_2}=\frac{1}{2}n_{HCl}=0,1\left(mol\right)\)
Mà theo lí thuyết : \(n_{Cl_2}=\frac{5}{2}n_{KMnO_4}=0,25\left(mol\right)\)
=> \(H\%=\frac{0,1}{0,25}\cdot100\%=40\%\)
Vì spu nổ thu được hh hai chất khí => \(\hept{\begin{cases}H_2\\HCl\end{cases}}\) (Vì H2 dư)
=> \(n_{hh}=\frac{13,44}{22,4}=0,6\left(mol\right)\)
=> \(n_{H_2\left(spu\right)}=n_{hh}-n_{HCl\left(spu\right)}=0,6-0,2=0,4\left(mol\right)\)
BT Hidro : \(\Sigma_{n_{H2\left(trong.binh\right)}}=n_{H_2\left(spu\right)}+\frac{1}{2}n_{HCl}=0,4+0,1=0,5\left(mol\right)\)
đọc thiếu đề câu a wtf
\(C_{M\left(HCl\right)}=\frac{0,2}{0,1}=2\left(M\right)\)


Bài 3:
nKOH = 1.0,05 = 0,05 (mol);nHCl=0,5.0,5=0,25 (mol)
PTHH: Fe + 2HCl → FeCl2 + H2
Mol: 0,0125 0,0125
PTHH: 2KOH + FeCl2 → 2KCl + Fe(OH)2
Mol: 0,05 0,025
Ta có:\(\dfrac{0,25}{2}>\dfrac{0,0125}{1}\) ⇒ HCl dư, FeCl3 pứ hết
⇒ m=0,0125.56 = 0,7 (g)
Bài 4:
a,Nếu cho giấy quỳ tím vào dung dịch sau phản ứng thì màu của giấy quỳ tím sẽ không thay đổi màu sắc
b,\(n_{NaOH}=0,5.0,15=0,075\left(mol\right);n_{HCl}=1.0,15=0,15\left(mol\right)\)
PTHH: NaOH + HCl → NaCl + H2O
Mol: 0,075 0,075 0,075
Ta có:\(\dfrac{0,075}{1}< \dfrac{0,15}{1}\) ⇒ NaOH pứ hết , HCl dư
mNaCl = 0,075.58,5 = 4,3875 (g)
c, Vdd sau pứ = 0,15 + 0,15 = 0,3 (l)
\(C_{M_{ddNaCl}}=\dfrac{0,075}{0,3}=0,25M;C_{M_{ddHCldư}}=\dfrac{0,15-0,075}{0,3}=0,25M\)
Bài 5:
a,\(n_{BaCl_2}=\dfrac{100.20,8\%}{208}=0,1\left(mol\right);n_{Na_2SO_4}=\dfrac{150.14,2\%}{142}=0,15\left(mol\right)\)
PTHH: BaCl2 + Na2SO4 → BaSO4 + 2NaCl
Mol: 0,1 0,1 0,1
Ta có: \(\dfrac{0,1}{1}< \dfrac{0,15}{1}\)⇒ BaCl2 pứ hết, Na2SO4 dư
\(\Rightarrow m_{BaSO_4}=0,1.233=23,3\left(g\right)\)
b,mdd sau pứ = 100+150 = 250 (g)
\(C\%_{ddNaCl}=\dfrac{0,2.58,5.100\%}{250}=4,68\%\)
\(C\%_{ddNa_2SO_4dư}=\dfrac{\left(0,15-0,1\right).142.100\%}{250}=2,84\%\)