Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đặt nN2O= x mol; nN2= y mol
Ta có nhhY= x+y= 1,792/ 22,4= 0,08 mol
mhhY=44x + 28y= 0,08.18.2
Giải hệ trên được x= 0,04 và y= 0,04
nAl= 0,27 mol= nAl(NO3)3
Quá trình cho e:
Al→ Al3++ 3e (1)
0,27→ 0,81 mol
Quá trình nhận e:
2NO3-+ 10e+ 12H+ → N2 + 6H2O (2)
0,4 ← 0,04 mol
2NO3-+ 8e+ 10H+ → N2O + 5H2O (3)
0,32 ← 0,04 mol
Tổng số mol e nhận ở (2) và (3) là ne nhận= 0,4+ 0,32= 0,72 mol <0,81 mol
Do đó còn xảy ra quá trình nhận e: ne nhận ở (4)= 0,81- 0,72= 0,09 mol
NO3-+ 8e+ 10H+ → NH4++ 3H2O (4)
0,09 → 0, 01125 mol
Dung dịch X chứa 0,27 mol Al(NO3)3 và 0,01125 mol NH4NO3
→m=0,27.213+ 0,01125.80=58,41 gam
Đáp án D

Ta có nhhY= x+y= 1,344/ 22,4= 0,06 mol
mhhY=44x + 28y= 0,06.18.2
Giải hệ trên được x= 0,03 và y= 0,03
nAl= 0,45 mol= nAl(NO3)3
Quá trình cho e:
Al→ Al3++ 3e (1)
0,45→ 1,35 mol
Quá trình nhận e:
2NO3-+ 10e+ 12H+ → N2 + 6H2O (2)
0,3 ← 0,03 mol
2NO3-+ 8e+ 10H+ → N2O + 5H2O (3)
0,24 ← 0,03 mol
Tổng số mol e nhận ở (2) và (3) là ne nhận= 0,3+ 0,24= 0,54 mol <1,35 mol
Do đó còn xảy ra quá trình nhận e: ne nhận ở (4)= 1,35- 0,54= 0,81 mol
NO3-+ 8e+ 10H+ → NH4++ 3H2O (4)
0,81 → 0, 10125 mol
Dung dịch X chứa 0,45 mol Al(NO3)3 và 0,10125 mol NH4NO3
→m=103,95 gam
Đáp án A

Đáp án B
Quy đổi hỗn hợp X thành Mg : x mol, Al: y mol và Fe: z mol, O :0,32 mol
→ 24x + 27y +56z =20,2
X +HNO3 → hỗn hợp khí
Theo quy tắc đường chéo tính được NO : 0,14 mol và N2O : 0,02 mol


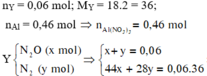
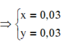


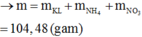
\(\overline{M}=\dfrac{28.nN_2+44.nN_2O}{nN_2+nN_2O}=20,4.2\left(1\right)\)
\(nN_2+nN_2O=\dfrac{2,24}{22,4}=0,1\left(2\right)\)
Từ (1), (2) suy ra\(\left\{{}\begin{matrix}nN_2=0,02\\nN_2O=0,08\end{matrix}\right.\)
gọi x, y lần lượt là nAl và nMg
\(\left\{{}\begin{matrix}mhh=27x+24y=9\\3x+2y=10.0,02+8.0,08\left(BTne\right)\end{matrix}\right.\)
\(\left\{{}\begin{matrix}x=0,12\\y=0,24\end{matrix}\right.\)
\(\%mAl=\dfrac{mAl.100\%}{mhh}=\dfrac{0,12.27.100\%}{9}=36\%\)