
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

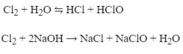

a) PTHH: \(K_2O+H_2O\rightarrow2KOH\)
Ta có: \(n_{KOH}=2n_{K_2O}=2\cdot\dfrac{23,5}{94}=0,5\left(mol\right)\) \(\Rightarrow C_{M_{KOH}}=\dfrac{0,5}{0,5}=1\left(M\right)\)
b) PTHH: \(2KOH+H_2SO_4\rightarrow K_2SO_4+2H_2O\)
Theo PTHH: \(n_{H_2SO_4}=\dfrac{1}{2}n_{KOH}=0,25\left(mol\right)\)
\(\Rightarrow m_{ddH_2SO_4}=\dfrac{0,25\cdot98}{20\%}=122,5\left(g\right)\) \(\Rightarrow V_{ddH_2SO_4}=\dfrac{122,5}{1,14}\approx107,46\left(ml\right)\)
c) Theo PTHH: \(n_{KOH}=0,5\left(mol\right)\) \(\Rightarrow m_{ddKOH}=\dfrac{0,5\cdot56}{5,6\%}=500\left(g\right)\) \(\Rightarrow V_{ddKOH}=\dfrac{500}{1,045}\approx478,47\left(ml\right)\)
Câu 8 :
số mol của kali oxit
nK2O = \(\dfrac{m_{K2O}}{M_{K2O}}=\dfrac{23,5}{94}=0,25\left(mol\right)\)
a) Pt : K2O + H2O → 2KOH\(|\)
1 1 2
0,25 0,5
Số mol của dung dịch kali hdroxit
nKOH = \(\dfrac{0,25.2}{1}=0,5\left(mol\right)\)
Nồng độ mol của dung dịch kali hidroxit
CMKOH = \(\dfrac{n}{V}=\dfrac{0,5}{0,5}=1\left(l\right)\)
b) Pt : H2SO4 + 2KOH → K2SO4 + 2H2O\(|\)
1 2 1 2
0,25 0,5
Số mol của axit sunfuric
nH2SO4 = \(\dfrac{0,25.1}{2}=0,25\left(mol\right)\)
khối lượng của axit sunfuric
mH2SO4 = nH2SO4. MH2SO4
= 0,25 . 98
= 24,5 (g)
Khối lượng của dung dịch axit sunfuric
C0/0H2SO4 = \(\dfrac{m_{ct}.100}{m_{dd}}\Rightarrow m_{dd}=\dfrac{m_{ct}.100}{C}=\dfrac{24,5.100}{20}=122,5\) (g)
Thể tích của dung dịch của axit sunfuric cần dùng
D = \(\dfrac{m}{V}\Rightarrow V=\dfrac{m}{D}=\dfrac{122,5}{1,14}=107,45\left(ml\right)\)
c) Pt : 2KOH + H2SO4 → K2SO4 + 2H2O\(|\)
2 1 1 2
0,5 0,25
Số mol của kali hidroxit nKOH = \(\dfrac{0,25.2}{1}=0,5\left(mol\right)\)
Khối lượng của kali hidroxit
mKOH = nKOH . MKOH
= 0,5 . 56
= 28 (g)
Khối lượng của dung dịch kali hidroxit
C0/0KOH = \(\dfrac{m_{ct}.100}{m_{dd}}\Rightarrow m_{dd}=\dfrac{m_{ct}.100}{C}=\dfrac{28.100}{5,6}=500\left(g\right)\)
Thể tích của dung dịch kali hidorxit cần dùng
D = \(\dfrac{m}{V}\Rightarrow V=\dfrac{m}{D}=\dfrac{500}{1,045}=478,47\left(ml\right)\)
Chúc bạn học tốt

a) CO2+H2O->H2CO3
SO2+H2O->H2SO3
b)Na2O+H2O->2NaOH
CaO+H2O->Ca(OH)2
C)Na2O+HCl->NaCl+H2O
CuO+2HCl->CuCl2 +H2O
CaO+2HCl->CaCl2+H2O
d)2NaOH+CO2->Na2CO3+H2O
2NaOH+SO2->Na2SO3+H2O

a) H2SO4 + NạOH → H2O + NaHSO4
b) H2SO4 + 2NaOH → 2H2O + Na2SO4

A, B, C đều là các hợp chất vô cơ của natri.
dd A + dd B → khí X
dd A + dd C → khí Y
=> A,B, C đều phải là các chất tan được trong nước (tính tan vật lí)
=> A phải có tính axit thì mới tác dụng được với dd B, C để giải phóng ra khí
X, Y đều tác dụng được với dd kiềm => X, Y đều là oxit axit
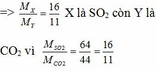
=> A là NaHSO4
B là Na2SO3 hoặc NaHSO3
C là Na2CO3 hoặc NaHCO3
2NaHSO4 + Na2SO3 → 2Na2SO4 + SO2↑ + H2O
NaHSO4 + NaHSO3 → Na2SO4 + SO2↑ + H2O
2NaHSO4 + Na2CO3 → 2Na2SO4 + CO2↑ + H2O
NaHSO4 + NaHCO3 → Na2SO4 + CO2↑ + H2O
SO2, CO2 đều tác dụng được với dung dịch kiềm
Ví dụ:
SO2 + 2NaOH → Na2SO3 +H2O
CO2 + 2NaOH → Na2CO3 + H2O