Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

TN1. nKOH = 0,22 mol
2KOH + ZnSO4 → Zn(OH)2 + K2SO4 (1)
2KOH + Zn(OH)2 → K2ZnO2 + 2H2O (2)
Gọi x là số mol của Zn(OH)2 phản ứng ở pt (2)
ð Số mol của Zn(OH)2 tạo ra ở pt (1) là \(x+\frac{3a}{99}\); nKOH = 2x + \(2\left(x+\frac{3a}{99}\right)\)= 0,22 mol (1')
TN2. nKOH = 0,28 ; Lượng KOH ở thí nghiệm 2 lớn hơn TN1 là 0,28 – 0,22 = 0,06 mol.
Tương tự như trên ta có: nKOH = (2x + 0,06) + \(2\left(x+0,03+\frac{2a}{99}\right)\)= 0,28 mol (2')
Từ (1') và (2') => x = 0,01 ; a = 2,97 ==> nZnSO4 = = 0,1 mol => mZnSO4 = 161.0,1 = 16,1g


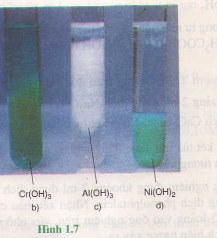
Cr(NO3)3 + 3NaOH(vừa đủ) → Cr(OH)3↓ + 3NaNO3 ;
AlCl3 + 3KOH (vừa đủ) → Al(OH)3↓ + 3KC1 ;
Ni(NO3)2 + 2NaOH → Ni(OH)2↓+ 2NaNO3.
nhìn cái ảnh này là thể hiện tự đăng rồi. Bữa trước môn sinh cũng thế chứ đâu

Câu 1 : Qua nhận xét về phân tử khối và liên kết hidro trong mỗi hợp chất, ta có :
Thứ tự : Axit > Ancol > Este > Hidrocacbon
Ta thấy : Glyxin ở dạng ion lưỡng cực nên có nhiệt độ sôi cao hơn axit propionic
Vậy, theo chiều tăng dần nhiệt độ sôi, nhiệt độ nóng chảy là :
Glyxin > Axit propionic > Butan-1-ol >Metyl axetat > Butan

Dùng dd AgNO3/NH3 nhận biết đc C2H2 do tạo kt vàng C2Ag2
C2H2 +2AgNO3 +2NH3 =>C2Ag2 + 2NH4NO3
Dùng dd Br2 C2H4 làm dd Br2 nhạt màu
C2H4 +Br2 =>C2H4Br2
C2H6 ko hien tuong
dẫn các khí đi qua dung dịch \(AgNO_3\)/\(NH_3\)
khí nào bị giữ lại , tạo kết tủa vàng là \(C_2H_2\)
\(C_2H_2+2\left(Ag\left(NH_3\right)_2\right)OH->C_2Ag_2+4NH_3+2H_2O\)
dẫn 2 khí còn lại đi qua dung dịch \(Br_2\)
khí nào làm mất màu dung dịch \(Br_2\) là \(C_2H_4\)
\(C_2H_4+Br_2->C_2H_4Br_2\)
khí nào không làm mất màu dung dịch \(Br_2\) là \(C_2H_6\)

– Fe(III) và Cl(I).
Công thức chung có dạng:
Theo quy tắc hóa trị, ta có: III.x = I.y → x/y= I/III
Công thưucs hóa học là: FeCl3
– Fe2(SO4)3, Fe(NO3)3, FePO4, Fe(OH)3.
H2S, SO2, SO3.
Trong X2(SO4)3, nguyên tử X có hóa trị III. Trong H3Y, nguyên tử Y có hóa trị III.
Vậy công thức hóa học giữa X và Y là XY.
a) Nguyên tố sắt(III) với nguyên tố Cl (I)
=> Fe2Cl3
Phân tử khối của Fe2Cl3 là : 56 . 2 + 35,5 .3 = 218,5 ( đvc )
nhóm SO4 (II); nhóm NO3 (I)
=> SO4(NO3)4
Phân tử khối của SO4(NO3)4 là : 456 ( đvc )
nhóm PO4 (III); nhóm OH (I).
=> PO4OH3
Phân tử khối của PO4OH3 là : 114 ( đvc )
b) Nguyên tố S (II) với nguyên tố H
=> SH2
Phân tử khối của SH2 là : 34 ( đvc )
nguyên tố S (IV) với nguyên tố O
=> SO4
Phân tử khối của SO4 là : 96 ( đvc )
nguyên tố S (VI) với nguyên tố O.
=> SO6
Phân tử khối SO6 là : 128 ( đvc )


Đáp án B
Glucozo không tạo kết tủa trắng khi tác dụng với dung dịch brom => loại D
Glyxin không làm chuyển màu quỳ tím => loại C
Hồ tinh bột không phản ứng với Cu(OH)2 trong môi trường kiềm tạo dung dịch xanh lam => loại A