Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Xét hiệu độ âm điện các nguyên tố trong phân tử, ta có:
\(PH_3\): \(2,20-2,19=0,01< 0,4\text{ }\Rightarrow\) Liên kết cộng hoá trị không cực.
\(H_2S\): \(2,58-2,20=0,38< 0,4\text{ }\Rightarrow\) Liên kết cộng hoá trị không cực.
\(NH_3\): \(3,04-2,20=0,84>0,4\&< 1,7\text{ }\Rightarrow\) Liên kết cộng hoá trị có cực.
\(BeCl_2\): \(3,16-1,57=1,59>0,4\&< 1,7\text{ }\Rightarrow\) Liên kết cộng hoá trị có cực.
\(HF:\) \(3,98-2,20=1,78>1,7\text{ }\Rightarrow\) Liên kết ion
\(BF_3:\) \(3,98-2,04=1,94>1,7\text{ }\Rightarrow\) Liên kết ion
\(LiF:\) \(3,98-0,98=3,00>1,7\text{ }\Rightarrow\) Liên kết ion
\(ClO_2\): \(3,44-3,16=0,28< 0,4\text{ }\Rightarrow\) Liên kết cộng hoá trị không cực.

Xét hiệu độ âm điện :
\(P_2O_5\): \(3,44-2,19=1,25>0,4\&< 1,7\text{ }\Rightarrow\) Liên kết cộng hoá trị có cực.
\(HAt\): \(2,20-2,2=0< 0,4\text{ }\Rightarrow\)Liên kết cộng hoá trị không cực.
\(C_3O_2\): \(3,44-2,55=0,89>0,4\&< 1,7\text{ }\Rightarrow\) Liên kết cộng hoá trị có cực.
\(CsF\): \(3,98-0,79=3,19>1,7\text{ }\Rightarrow\) Liên kết ion.
\(NaCl\): \(3,16-0,93=2,23>1,7\text{ }\Rightarrow\) Liên kết ion.
\(CaO\): \(3,44-1,00=2,44>1,7\text{ }\Rightarrow\) Liên kết ion.
\(PN\): \(3,04-2,19=0,85>0,4\&< 1,7\text{ }\Rightarrow\) Liên kết cộng hoá trị có cực.
\(ClF_3\): \(3,98-3,16=0,82>0,4\&< 1,7\text{ }\Rightarrow\) Liên kết cộng hoá trị có cực.

Xét hiệu độ âm điện :
\(C_2N_2\): \(3,04-2,55=0,49>0,4\&< 1,7\text{ }\Rightarrow\) Liên kết cộng hoá trị có cực.
\(HBr\): \(2,96-2,20=0,76>0,4\&< 1,7\text{ }\Rightarrow\) Liên kết cộng hoá trị có cực.
\(HI\): \(2,66-2,20=0,46>0,4\&< 1,7\text{ }\Rightarrow\) Liên kết cộng hoá trị có cực.
\(H_2O_2\): \(3,44-2,20=1,24>0,4\&< 1,7\text{ }\Rightarrow\) Liên kết cộng hoá trị có cực.
\(S_3\): \(2,58-2,58=0< 0,4\text{ }\Rightarrow\) Liên kết cộng hoá trị không cực.
\(N_2O\): \(3,44-3,04=0,4\text{ }\Rightarrow\) Liên kết cộng hoá trị có cực.
\(SO_2\): \(3,44-2,58=0,86>0,4\&< 1,7\text{ }\Rightarrow\) Liên kết cộng hoá trị có cực.
\(C_6H_6\): \(2,55-2,20=0,35< 0,4\text{ }\Rightarrow\) Liên kết cộng hoá trị không cực.
\(LiF\): \(3,98-0,98=3,0\text{ }\Rightarrow\) Liên kết ion.
\(H_2S\): \(2,58-2,20=0,38< 0,4\text{ }\Rightarrow\) Liên kết cộng hoá trị không cực.
\(N_2H_4\): \(3,04-2,20=0,84>0,4\&< 1,7\text{ }\Rightarrow\) Liên kết cộng hoá trị có cực.

Xét hiệu độ âm điện của các phân tử :
\(H_2\): \(2,20-2,20=0< 0,4\text{ }\Rightarrow\) Liên kết cộng hoá trị không cực.
\(O_2\): \(3,44-3,44=0< 0,4\text{ }\Rightarrow\) Liên kết cộng hoá trị không cực.
\(O_3\): \(3,44-3,44=0< 0,4\text{ }\Rightarrow\) Liên kết cộng hoá trị không cực.
\(H_2O\): \(3,44-2,20=1,24>0,4\&< 1,7\text{ }\Rightarrow\) Liên kết cộng hoá trị có cực.
\(BeCl_2\): \(3,16-1,57=1,59>0,4\&< 1,7\text{ }\Rightarrow\) Liên kết cộng hoá trị có cực.
\(CO\): \(3,44-2,55=0,89>0,4\&< 1,7\text{ }\Rightarrow\) Liên kết cộng hoá trị có cực.
\(CO_2\): \(3,44-2,55=0,89>0,4\&< 1,7\text{ }\Rightarrow\) Liên kết cộng hoá trị có cực.
\(NH_3\): \(3,04-2,20=0,84>0,4\&< 1,7\text{ }\Rightarrow\) Liên kết cộng hoá trị có cực.
\(PH_3\): \(2,20-2,19=0,01< 0,4\text{ }\Rightarrow\) Liên kết cộng hoá trị không cực.
\(BF_3\): \(3,98-2,04=1,94>1,7\text{ }\Rightarrow\) Liên kết ion.
\(HF\): \(3,98-2,20=1,78>1,7\text{ }\Rightarrow\) Liên kết ion.
\(HCl\): \(3,16-2,20=0,96>0,4\&< 1,7\text{ }\Rightarrow\) Liên kết cộng hoá trị có cực.
\(N_2\): \(3,04-3,04=0< 0,4\text{ }\Rightarrow\) Liên kết cộng hoá trị không cực.
\(NO\): \(3,44-3,04=0,4\text{ }\Rightarrow\) Liên kết cộng hoá trị có cực.

F O Cl N
Độ âm điện: 3,98 3,44 3,16 3,14
Nhận xét: tính phi kim giảm dần.
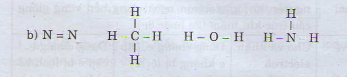
N2 CH4 H2O NH3
Hiệu độ âm điện: 0 0,35 1,24 0,84
Phân tử N2, CH4 có liên kết cộng hóa trị không phân cực. Phân tử H2O có liên kết cộng hóa trị phân cực mạnh nhất trong dãy.

Trả lời :
\(HNO\): \(H-N=O\)
\(C_2N_2\): \(N\equiv C-C\equiv N\)
\(HCN\): \(H-C\equiv N\)
\(C_3O_2\): \(O=C=C=C=O\)
\(N_2O\): \(N\equiv N\rightarrow O\)

Dùng que đóm còn than hồng để nhận biết O2. Còn lại hai bình là H2S và SO2 mang đốt, khí nào cháy được là H2S, khí không cháy là SO2.
2H2S + 3O2 -> 2H2O + 2SO2.

a) 4HCl + MnO2 --> MnCl2 + Cl2 +2H2O
2Fe + 3Cl2 ---> 2FeCl3
FeCl3 + 3NaOH --> Fe(OH)3 + 3NaCl
NaCl + H2SO4 đ---> NaHSO4 + HCl
2HCl + CuO ---> CuCl2 + H2O
CuCl2 +2AgNO3 ---> Cu(NO3)2 + 2AgCl
b) 2KMnO4 + 16HCl ---> 2KCl + 2MnCL2 +5Cl2 +8H2O
Cl2 + H2--->2HCl
6HCl + Fe2O3 ---> 2FeCl3 +3H2O
FeCl3 + 3AgNO3 --> Fe(NO3)3 +3AgCl
2AgCl --to---> 2Ag + Cl2
Cl2 + 2NaBr ---> 2NaCl + Br2
Br2 + 2NaI --> 2NaBr + I2
I2 +Zn --to--> ZnI2
ZnI2 + 2NaOH --> Zn(OH)2 +2NaI
c) 2KCl ---dpnc--> 2K + Cl2
Cl2 + 2KOH --> KCl + KClO + H2O
4KClO --> KClO3 +3 KCl
4KClO3 ---> 3KClO4 + KCl
3KClO4 + 8Al ---> 4Al2O3 + 3KCl
KCl + AgNO3 --> AgCl + KNO3
d) 3Cl2 + 6KOH ---> KClO3 + 5KCl +3H2O
2KClO3 ---> 2KCl +#O2
2KCl --> 2K + Cl2
2Cl2 + Ca(OH)2 ---> CaCl2 +Ca(ClO)2
Ca(ClO)2 ---> CaCl2 + O2
CaCl2 ---> Ca + Cl2
Cl2 ra O2 ????
e)6HCl + KClO3 ---> KCl +3Cl2 +3H2O
3Cl2 +6KOH --> 5KCl + KClO +3 H2O
2KClO3 --> 2KCl + 3O2
2KCl --> 2K + CL2
CL2 +H2 --> 2HCl
2HCl +Fe--> FeCl2 + H2
Cl2 + 2FeCl2 -->2FeCl3
FeCl3 +3NaOH --> Fe(OH)3 +3NaCl

a) (1) MnO2 + 4 HCl(đặc) -to-> MnCl2 + Cl2 + 2 H2O
(2) Cl2 + H2 \(\Leftrightarrow\) 2 HCl
(3) HCl + NaOH -> NaCl + H2O
(4) 2 NaCl + 2 H2O -đpddcmnx-> 2 NaOH + H2 + Cl2
(5) Cl2 + 2 H2O + SO2 -> H2SO4 + 2 HCl
(6) H2SO4 + BaCl2 -> BaSO4 + 2 HCl
b)
(1) BaCl2 -điện phân nóng chảy nhiệt độ cao-> Ba + Cl2
(2) Cl2 + H2 \(\Leftrightarrow\) 2 HCl
(3) Fe + 2 HCl -> FeCl2 + H2
(4) 2 FeCl2 + Cl2 -to-> 2 FeCl3
(5) 2 FeCl3 + 3 Ba(OH)2 -> 2 Fe(OH)3 +3 BaCl2
(6) BaCl2 + H2SO4 -> BaSO4 + 2 HCl
c) (1) BaCl2 + H2SO4 -> BaSO4 +2 HCl
(2) 2 HCl + CuO -> CuCl2 + H2O
(3) CuCl2 + 2 KOH -> Cu(OH)2 + 2 KCl
(4) KCl + H2O -đpddcmnx-> KOH + 1/2 Cl2 + 1/2 H2
(5) 6 KOH + 3 Cl2 -to->5 KCl + KClO3 +3 H2O
(6) 2 KClO3 -to-> 2 KCl + 3 O2
a)
(1) MnO2 + 4HCl(đ) -to-> MnCl2 + Cl2 + 2H2O
(2) Cl2 + H2 <-as-> 2 HCl
(3) HCl + NaOH => NaCl + H2O
(4) 2NaCl + 2H2O -đpddcmn-> 2NaOH + H2 + Cl2
(5) Cl2 + 2H2O + SO2 => H2SO4 + 2HCl
(6) H2SO4 + BaCl2 => BaSO4 + 2HCl
b)
(1) BaCl2 -đpdd-> Ba + Cl2
(2) Cl2 + H2 ⇔ 2HCl (Đk : ánh sáng hoặc nhiệt độ)
(3) Fe + 2HCl => FeCl2 + H2
(4) 2FeCl2 + Cl2 -to-> 2FeCl3
(5) 2FeCl3 + 4Ba(OH)2 => 2Fe(OH)3 + 3BaCl2
(6) BaCl2 + H2SO4 => BaSO4 + 2HCl
c)
(1) BaCl2 + H2SO4 => BaSO4 +2HCl
(2) 2HCl + CuO => CuCl2 + H2O
(3) CuCl2 + 2KOH => Cu(OH)2 + 2KCl
(4) 2KCl + 2H2O -đpddcmn-> 2KOH + Cl2 + H2
(5) 6KOH + 3Cl2 -to-> 5KCl + KClO3 +3H2O
(6) 2KClO3 -to-> 2KCl + 3O2
Đáp án D
Cấu hình electron của C là 6C: [He]2s22p2. C ở trạng thái kích thích có cấu hình: [He]2s12p3 → Khi đó C có 4 electron độc thân.
Do có 4 electron độc thân nên mỗi C tạo ba liên kết cộng hóa trị với 3 nguyên tử H và 1 nguyên tử C còn lại.
Công thức cấu tạo có thể có của C2H6 là
→ Số liên kết cộng hóa trị trong phân tử C2H6 là 7