Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(HgO\left(0,1\right)+H_2\left(0,1\right)\rightarrow Hg\left(0,1\right)+H_2O\)
Ta có: \(n_{HgO}=\dfrac{21,7}{217}=0,1\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Hg}=0,1.201=20,1\left(g\right)\\m_{H_2}=0,1.2=0,2\left(g\right)\end{matrix}\right.\)
a. Số mol thủy ngân (II) oxit là: n = =
= 0,1 (mol)
phương trình phản ứng:
HgO + H2 → H2O + Hg
1 mol 1 mol 1mol 1 mol
0,1 0,1 0,1 0,1
Khối lượng thủy ngân thu được: m = 0,1.201 = 20,1 (g)
b. Số mol khí hi đro: n = 0,1 mol
Thể tích khí hiđro cần dùng ở đktc là:
V = 22,4.0,1 = 2,24 (lít)

a. Số mol thủy ngân (II) oxit là: n = \(\frac{m}{M}\) = \(\frac{21,7}{217}\) = 0,1 (mol)
phương trình phản ứng:
HgO + H2 → H2O + Hg
1 mol 1 mol 1mol 1 mol
0,1 0,1 0,1 0,1
Khối lượng thủy ngân thu được: m = 0,1.201 = 20,1 (g)
b. Số mol khí hi đro: n = 0,1 mol
Thể tích khí hiđro cần dùng ở đktc là:
V = 22,4.0,1 = 2,24 (lít)
a/ PTHH: HgO + H2 ===> Hg + H2O
nHgO = 21,7 / 217 = 0,1 mol
=> nHg = nHgO = 0,1 mol
=> mHg = 0,1 x 201 = 20,1 gam
b/ Theo phương trình, ta có:
nH2 = nHgO = 0,1 mol
=> VO2(đktc) = 0,1 x 22,4 = 2,24 lít

Bài 10: nH2= 0,125 mol
2H2 + O2 → 2H2O
0,125 mol 0,0625 mol 0,125 mol
a) VO2= 0,0625 x 22,4= 1,4 (l) ; mO2= 0,0625 x 32= 2 (g)
b) mH2O= 0,125 x 18 = 2,25 (g)
Bài 11: nH2= 22,4/22,4 = 1 mol; nO2= 16,8/22,4 =0,75 mol
2H2 + O2 → 2H2O
Ban đầu: 1 mol 0,75 mol
PƯ: 1 mol 0,5 mol 1 mol
Còn lại: 0 mol 0,25 mol 1 mol
mH2O= 1 x 18= 18 (g)

10) lập pthh của pư
2H2 + O2 → 2H20
2mol 1mol 2mol
0,125mol 0,0625mol 0,125mol
số mol của H2
nH2= 2,8 : 22,4 =0,125mol
thể tích khí H2
vH2= 0,0624 .22,4 =1,4 lít
khối lượng khí o2
mO2 = 0,0625 . 32= 2 gam
b) khối lượng H20 thu được
mH2O =0,125 . 18 = 2,25 gam
11) số mol h2
nH2= 22,4 : 2,24 = 10 mol
soosmol của O2
nO2= 16,8 : 22,4 = 0,75 mol
lập pthh của pư
2H2 + 02 → 2 H20
2mol 1mol 2mol
10mol 0,75mol 1,5mol
xét tỉ lệ
\(\frac{nH2}{2}\) = \(\frac{10}{2}\) = 5 > \(\frac{nO2}{1}\)= \(\frac{0,75}{1}\)= 0,75
vậy H2 dư sau pư tính theo O2
số mol H2 dư = ( 0.75 .2) : 1= 1,5 mol
số mol H2 dư = 5 - 1,5=3,5mol
khối lượng H2 dư
m= 3,5 .2=7 gam
khối lượng nước thu được
m=1,5 .2 =3gam

\(n_{HgO}=\dfrac{43,4}{217}=0,2\left(mol\right)\)
PTHH: HgO + H2 --to--> Hg + H2O
0,2 0,2 0,2
\(\rightarrow\left\{{}\begin{matrix}m_{Hg}=201.0,2=40,2\left(g\right)\\V_{H_2}=0,2.22,4=4,48\left(l\right)\end{matrix}\right.\)
nHgO = 43,4 : 217 = 0,2 (mol)
pthh : HgO + H2 -t> Hg + H2O
0,2 0,2 0,2
mHg = 0,2 . 201 = 40,2 (G)
VH2 = 0,2 . 22,4 = 4,48 (L)

nCuO = 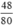 = 0,6 mol.
= 0,6 mol.
Phương trình hóa học của phản ứng khử CuO:
CuO + H2 → Cu + H2O.
nCu = 0,6mol.
mCu = 0,6 .64 = 38,4g.
Theo phương trình phản ứng trên:
nH2 = 0,6 mol
VH2 = 0,6 .22,4 = 13,44 lít.

a, PTHH:
H2 + ZnO → Zn + H2O
nZnO = 8,1 / 81 = 0,1 ( mol)
Thep PTHH nH2 = nZnO = 0,1( mol)
nzn = nZnO = 0,1 (mol)
VH2 = 0,1 x 22,4 = 2,24 (l)
b, mZn = 0,1 x 65 = 6,5 (g)
c, Zn + 2HCl → ZnCl2 + H2
mHCl = 200 x 7,3 % = 14,6 ( g)
nHCl = 14,6 / 36,5 = 0,4 ( mol)
Theo PTHH nH2 = 1/2nHCl= 0,4 /2 = 0,2( mol)
VH2 = 0,2 x 22,4 = 4,48( l)
d, y H2 + FexOy → x Fe + yH2O
Theo câu a nH2 = 0,1 ( mol)
Theo PTHH nFexOy= 1/ynH2 = 0,1 /y ( mol)
mFexOy = 0,1/y( 56x + 16y)= 3,24 (g)
đoạn này bạn tự tính nhé!

1. Tính khối lượng chất tham gia và sản phẩm
* Các bước giải:
- Đổi số liệu đầu bài. Tính số mol của chất mà đầu bài cho.
- Lập phương trình hoá học.
- Dựa vào số mol chất đã biết để tính số mol chất cần tìm.
2. Tính thể tích khí tham gia và tạo thành
H2+Cl2->2HCl
\(n_{H_2}=67,2:22,4=3\left(mol\right)\)
Ta có: \(n_{H_2}=n_{Cl_2}=3\left(mol\right)\)
\(V_{Cl_2}=3.22,4=67,2l\)
\(n_{HCl}=2n_{Cl_2}=2.3=6\left(mol\right)\)
\(m_{HCl}=6.36,5=219g\)

nHgO =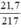 = 0,1 mol.
= 0,1 mol.
Phương trình hóa học của phản ứng khử HgO:
HgO + H2 → Hg + H2O
nHg = 0,1 mol.
mHg = 0,1 .201 = 20,1g.
nH2 = 0,1 mol.
VH2 = 0,1 .22,4 =2,24l.