Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Do tính khử Zn > Fe nên Zn phản ứng trước.
Do khối lượng rắn khan ở thí nghiệm 2 > thí nghiệm 1.
Do đó, ở thí nghiệm 1 HCl hết, kim loại có thể dư. Ở thí nghiệm 2, kim loại hết, HCl có thể dư.
\(Zn + 2HCl \to ZnCl_2 + H_2\\ Fe + 2HCl \to FeCl_2 + H_2\\ n_{Zn} = a ; n_{Fe} = b\\ m_A = 65a + 56b = 18,6\\ m_{chất\ rắn} = 136a + 127b = 39,9\\ \Rightarrow a = 0,2; b = 0,1\\ \Rightarrow m_{Zn} = 0,2.65 = 13(gam) ; m_{Fe} = 0,1.56 = 5,6(gam)\)
Thí nghiệm 1 :
\(n_{Fe\ pư} = x(mol) ; n_{Fe\ dư} = y(mol)\\ \Rightarrow x + y = 0,1(1)\\ n_{FeCl_2} = x (mol)\\ \Rightarrow m_{chất\ rắn} = 0,2.136 + 127x + 56y = 34,575(2)\\ (1)(2)\Rightarrow x = 0,025 ; y = 0,075\\ n_{HCl} = 2n_{Zn} + 2n_{Fe\ pư} = 0,2.2 + 0,025.2 = 0,45(mol)\\ C_{M_{HCl}} = \dfrac{0,45}{0,5} = 0,9M\)

-Vì khối lượng hỗn hợp kim loại ở 2 trường hợp đều bằng nhau. Chỉ thay đổi lượng HCl. Do trường hợp 800ml HCl thì khối lượng chất rắn tăng lên nên nếu với 500ml HCl mà kim loại hết thì khi tăng lên 800ml HCl thì khối lượng chất rắn không thể tăng lên nữa nên:
-Trường hợp 500ml HCl thì hỗn hợp kim loại dư, HCl hết.
-Trường hợp 500ml HCl thì hỗn hợp kim loại hết, HCl dư.
-Ta sẽ tìm khối lượng mỗi kim loại trong trường hợp 800ml HCl:
-Gọi \(n_{Zn}=x;n_{Fe}=y\)
Zn+2HCl\(\rightarrow\)ZnCl2+H2
Fe+2HCl\(\rightarrow\)FeCl2+H2
Chất rắn thu được là ZnCl2 x mol và FeCl2 y mol
hệ: \(\left\{{}\begin{matrix}65x+56y=18,6\\136x+127y=39,9\end{matrix}\right.\)
giải ra x=0,2 và y=0,1
mZn=65.0,2=13gam; mFe=56.0,1=5,6gam
-Tính nồng độ mol HCl theo trường hợp 500ml HCl vì HCl phản ứng hết.
Cứ 1 mol hỗn hợp kim loại tạo 1 mol hỗn hợp muối thì tăng 71 gam
Vậy x mol hỗn hợp kim loại tạo x mol hỗn hợp muối thì tăng 34,575-18,6=15,975 gam
\(\rightarrow x=\dfrac{15,975}{71}=0,225mol\)
\(\rightarrow n_{HCl}=2x=0,45mol\rightarrow C_{M_{HCl}}=\dfrac{0,45}{0,5}=0,9M\)
Ngoài ra còn có thể tính cách khác nữa!bạn tự tham khảo nhé!

3. CuO +H2SO4 -->CuSO4 +H2O
nCuO=64/80=0,8(mol)
theo PTHH :nCuO =nH2SO4=nCuSO4=0,8(mol)
=>mddH2SO4 20%=0,8.98.100/20=392(g)
mCuSO4=0,8.160=128(g)
mdd sau phản ứng =64 +392=456(g)
mH2O=456 -128=328(g)
giả sử có a g CuSO4.5H2O tách ra
trong 250g CuSO4 tách ra có 160g CuSO4 và 90g H2O tách ra
=> trong a g CuSO4.5H2O tách ra có : 160a/250 g CuSO4 và 90a/250 g H2O tách ra
=>mCuSO4(còn lại)=128 -160a/250 (g)
mH2O (còn lại)=328 -90a/250 (g)
=>\(\dfrac{128-\dfrac{160a}{250}}{328-\dfrac{90a}{250}}.100=25\)
=>a=83,63(g)

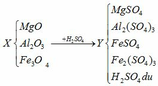
(a) Hòa tan MgO, Al2O3 và Fe3O4 vào H2SO4:
(1) MgO + H2SO4 → MgSO4 + H2O
(2) Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
(3) Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3 + 4H2O
Trung hòa Y:
(4) H2SO4 + 2NaOH → Na2SO4 + 2H2O
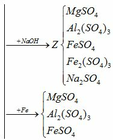
Cho dung dịch Y (MgSO4, Al2(SO4)3, FeSO4, Fe2(SO4)3, H2SO4) qua cột chứa bột sắt:
(5) H2SO4 + Fe → FeSO4 + H2
(6) Fe2(SO4)3 + Fe → 3FeSO4
(b) nH2SO4 = 0,45.1 = 0,45 mol
Gọi số mol của MgO, Al2O3 và Fe3O4 trong hỗn hợp ban đầu lần lượt là x, y, z (mol)
Ta có: 40x + 102y + 232z = 20,68 (*)
- Khi hòa tan hỗn hợp vào H2SO4:
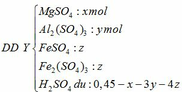
- Trung hòa ¼ dung dịch Y cần 0,025 mol NaOH vậy trung hòa Y cần 0,1 mol NaOH:
Theo PTHH (4): nH2SO4 dư = 0,5nNaOH = 0,05 mol
=> 0,45 – x – 3y – 4z = 0,05
=> x + 3y + 4z = 0,4 (**)
Dung dịch thu được chứa các chất:
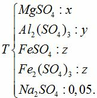
- Giả sử dẫn toàn bộ dung dịch Y qua cột chứa bột Fe:
(5) H2SO4 + Fe → FeSO4 + H2
0,05 → 0,05 (mol)
(6) Fe2(SO4)3 + Fe → 3FeSO4
z → 3z (mol)
Dung dịch sau chứa các chất tan:
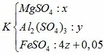
Theo đề bài ta có: mK – mT = 4.1,105
=> [120x + 342y + 152(4z + 0,05)] – [120x + 342y + 152.z + 400z + 0,05.142] = 4,42
=> z = 0,07 (***)
Từ (*) (**) (***) ta giải được z = 0,06; y = 0,02; z = 0,07
Số mol của nguyên tố O trong hỗn hợp X:
nO = nMgO + 3nAl2O3 + 4nFe3O4 = 0,06 + 3.0,02 + 4.0,07 = 0,4 mol
Khối lượng của O: mO = 0,4.16 = 6,4 (gam)
Phần trăm khối lượng của nguyên tố O:






BTKL
mX + mdd HNO3 = mdd X + mH2O + m↑
=> mdd X = 11,6 + 87,5 – 30 . 0,1 – 46 . 0,15 = 89,2g
=> C%Fe(NO3)3 = 13,565%


Thí nghiệm 1 :
\(m_{Cl} = m_{muối} - m_{kim\ loại} = 5,82-2,98 = 2,84(gam)\\ \Rightarrow n_{HCl} = n_{Cl} = \dfrac{2,84}{35,5} = 0,08(mol)\\ \Rightarrow C_{M_{HCl}} = \dfrac{0,08}{0,2} = 0,4M\)
Thí nghiệm 2 :
\(\left\{{}\begin{matrix}Fe:a\left(mol\right)\\Zn:b\left(mol\right)\end{matrix}\right.\)\(\Rightarrow\) 56a + 65b = 2,98(1)
\(\left\{{}\begin{matrix}FeCl_2:a\left(mol\right)\\ZnCl_2:b\left(mol\right)\end{matrix}\right.\)\(\Rightarrow\) 127a + 136b = 6,53(2)
(1)(2) suy ra: a = 0,03 ; b = 0,02
Vậy :
\(\%m_{Fe} = \dfrac{0,03.56}{2,98}.100\% = 56,38\%\\ \%m_{Zn} = 100\% -56,38\% = 43,62\%\)