Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gợi Ý nhé:
Đối với loại toán này ta nên tìm cách tổ hợp từ các quá trình đã cho để loại đi các chất trung gian và được phương trình cần tính nhiệt phản ứng.
Từ các dữ kiện của bài toán ta có:
CO(NH2)2 (r) + 2HCl (k) \(\rightarrow\) COCl2 (k) + 2NH3 (k) - \(\Delta\)H3 = + 201,0 kJ
COCl2 (k) \(\rightarrow\) CO (k) + Cl2 (k) - \(\Delta\)H2 = + 112,5 kJ
CO (k) + H2O(h) \(\rightarrow\) CO2 (k) + H2 (k) \(\Delta\)H1 = - 41,3 kJ
H2O (l) \(\rightarrow\) H2O (h) \(\Delta\)H5 = 44,01 kJ
H2 (k) + Cl2 (k) \(\rightarrow\) 2HCl (k) 2. \(\Delta\)H4 = 2.(- 92,3) = - 184,6 kJ
Cộng theo từng vế các quá trình trên và loại đi các chất trung gian, ta thu được phương trình: CO(NH2)2 (r) + H2O (l) \(\rightarrow\) CO2 (k) + 2NH3 (k) có nhiệt của phản ứng là DH = (- \(\Delta\)3) + (- \(\Delta\)H2) + \(\Delta\)H1 + \(\Delta\)H5 + 2. \(\Delta\)H4. Thay số có \(\Delta\)H = 131,61 kJ.

Xét hiệu độ âm điện của các phân tử :
\(H_2\): \(2,20-2,20=0< 0,4\text{ }\Rightarrow\) Liên kết cộng hoá trị không cực.
\(O_2\): \(3,44-3,44=0< 0,4\text{ }\Rightarrow\) Liên kết cộng hoá trị không cực.
\(O_3\): \(3,44-3,44=0< 0,4\text{ }\Rightarrow\) Liên kết cộng hoá trị không cực.
\(H_2O\): \(3,44-2,20=1,24>0,4\&< 1,7\text{ }\Rightarrow\) Liên kết cộng hoá trị có cực.
\(BeCl_2\): \(3,16-1,57=1,59>0,4\&< 1,7\text{ }\Rightarrow\) Liên kết cộng hoá trị có cực.
\(CO\): \(3,44-2,55=0,89>0,4\&< 1,7\text{ }\Rightarrow\) Liên kết cộng hoá trị có cực.
\(CO_2\): \(3,44-2,55=0,89>0,4\&< 1,7\text{ }\Rightarrow\) Liên kết cộng hoá trị có cực.
\(NH_3\): \(3,04-2,20=0,84>0,4\&< 1,7\text{ }\Rightarrow\) Liên kết cộng hoá trị có cực.
\(PH_3\): \(2,20-2,19=0,01< 0,4\text{ }\Rightarrow\) Liên kết cộng hoá trị không cực.
\(BF_3\): \(3,98-2,04=1,94>1,7\text{ }\Rightarrow\) Liên kết ion.
\(HF\): \(3,98-2,20=1,78>1,7\text{ }\Rightarrow\) Liên kết ion.
\(HCl\): \(3,16-2,20=0,96>0,4\&< 1,7\text{ }\Rightarrow\) Liên kết cộng hoá trị có cực.
\(N_2\): \(3,04-3,04=0< 0,4\text{ }\Rightarrow\) Liên kết cộng hoá trị không cực.
\(NO\): \(3,44-3,04=0,4\text{ }\Rightarrow\) Liên kết cộng hoá trị có cực.

với yếu tố nhiệt độ thì giảm nhiệt độ vì đây là phản ứng tỏa nhiệt vì giảm nhiệt độ phản ưng chuyển dịch theo chiều tỏa nhiệt
với áp suất : tăng áp suất vì vế trái có 4 phân tử khí vế phải có 2 phân tử khí khi tăng áp suất là chuyển dịch theo chiều giảm số phân tử khí
tăng nồng độ N2 hoặc H2 hoặc tăng cả hai vì khi làm như vậy tốc độ phản ứng sẽ xảy ra theo chiều làmtăng nộng độ chất đó

Áp suất tăng 2 lần thì thể tích giảm 2 lần nên nồng độ tăng 2 lần và phản ứng xảy ra chiều thuận. Do đó tốc độ phản ứng sẽ tăng 2.2 = 4 lần.
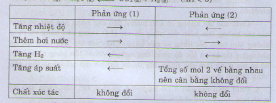
Đáp án D.
Thêm H2, cân bằng chuyển dịch theo chiều nghịch. Tăng áp suất, cân bằng không chuyển dịch (do số mol phân tử khí ở hai vế là như nhau). Chất xúc tác không làm chuyển dịch cân bằng.