Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, - Trích lần lượt các chất ra làm mẫu thử
- Cho HCl qua lần lượt từng mẫu thử ; mẫu nào không tác dụng được là Cu và NaCl ; mẫu nào tạo ra dung dịch lục nhạt và có khí bay ra là Fe ; mẫu nào tác dụng được mà không có hiện tượng gì xảy ra là P2O5 và BaO
Fe + 2HCl \(\rightarrow\) FeCl2 + H2\(\uparrow\)
2P2O5 + 3HCl \(\rightarrow\) POCl3 + 3HPO3
BaO + 2HCl \(\rightarrow\) BaCl2 + H2O
- Cho NaCl và Cu lên ngọn lửa đèn cồn , muối của Na chyá với ngọn lửa màu vàng
- Còn lại là Cu
- Sục khí CO2 vào BaO và P2O5 ; mẫu nào tạo ra kết tủa trắng là BaO
BaO + CO2 \(\rightarrow\) BaCO3
- Còn lại P2O5

5/ tương tự 1,2,3
Mình làm tắt nhé
+ Dùng quỳ tím thì phân biệt được HCl : quỳ tím hóa đỏ
+ Dùng NaCl thì phân biệt được AgNO3 : Có kết tủa trắng xuất hiện
+ Còn lại là K2SO4
P/S : Giả thiết đề câu 2 và 5 HCl là dd nha! còn nếu là khí thì bạn dùng quỳ tím ẩm
1, - Trích mỗi chất làm mẫu thử
- Cho quỳ tím vào các chất trên:
+ dd làm quỳ tím hóa đỏ là H2SO4
+ dd làm quỳ tím hóa xanh là NaOH
+ dd không làm đổi màu quỳ tím là Na2SO4 và NaCl
- Cho dd BaCl2 vào 2 mẫu thử còn lai:
+ dd có kết tủa trắng là Na2SO4
+ dd không có hiện tượng xảy ra là NaCl
PTHH: BaCl2+Na2SO4--->BaSO4+2NaCl

. 2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O (1)
a/158 mol ............................................... a/63,2 mol
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O (2)
a/87 mol ..............................a/87mol
Ta có: a/63,2>a/87. Vậy khí clo ở phản ứng (1) thu được nhiều hơn phản ứng (2)
b. 2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O (1’)
amol 2,5a mol
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O (2’)
amol a mol
Ta có 2,5a > a. Vậy dùng KMnO4 để điều chế thì thu được nhiều khí clo hơn so với dùng MnO2 khi lấy cùng khối lượng cũng như số mol.

a)
-Thử bằng quỳ tím:
+ Quỳ tím hóa đỏ\(\rightarrow\)H2SO4 và HCl
+ Quỳ tím hóa xanh\(\rightarrow\)NaOH và Ca(OH)2
- Cho BaCl2 vào 2 mẫu làm quỳ tím hóa đỏ:
+ Có kết tủa trắng\(\rightarrow\)H2SO4:
BaCl2+H2SO4\(\rightarrow\)BaSO4\(\downarrow\)+2HCl
+ Không hiện tượng là HCl
- Cho Na2CO3 vào 2 mẫu làm quỳ tím hóa xanh:
+ Có kết tủa trắng\(\rightarrow\)Ca(OH)2:
Ca(OH)2+Na2CO3\(\rightarrow\)CaCO3\(\downarrow\)+2NaOH
+ không hiện tượng là NaOH
b)
- Thử bằng quỳ tím:
+ Quỳ tím hóa đỏ\(\rightarrow\)H2SO4
+ Không hiện tượng\(\rightarrow\)CuSO4, AgNO3, NaCl
- Cho HCl vào 3 mẫu còn lại:
+ Có kết tủa trắng\(\rightarrow\)AgNO3:
AgNO3+HCl\(\rightarrow\)AgCl\(\downarrow\)+HNO3
+ Không hiện tượng\(\rightarrow\)CuSO4 và NaCl
- Cho BaCl2 vào 2 mẫu còn lại:
+ Có kết tủa trắng\(\rightarrow\) CuSO4:
CuSO4+BaCl2\(\rightarrow\)BaSO4\(\downarrow\)+CuCl2
+ Không hiện tượng\(\rightarrow\)NaCl

1. Fe + H2SO4 => FeSO4 + H2
2. Fe(OH)2 + H2SO4 => FeSO4 + 2H2O
3. Fe + 4HNO3 loãng => Fe(NO3)3 + NO +2H2O
4. 3FeO + 10HNO3 => 3Fe(NO3)3 + NO + 5H2O
5. 2Fe(OH)3 + 3H2SO4 => Fe2(SO4)3 + 6H2O
6. Fe2O3 + 6HNO3 => 2Fe(NO3)3 + 3H2O
7. 2Fe + 6H2SO4 đặc => Fe2(SO4)3 + 3SO2 + 6H2O
8. 2FeO + 4H2SO4 đặc => Fe2(SO4)3 + SO2 + 4H2O
9. Fe2O3 + 3H2SO4 đặc => Fe2(SO4)3 + 3H2O
10. 2Fe(OH)2 + 4H2SO4 đặc => Fe2(SO4)3 + SO2 + 6H2O
11. 2FeSO4 + 2H2SO4 đặc => Fe2(SO4)3 + SO2 + 2H2O
12. 8Fe + 30HNO3 = 8Fe(NO3)3 + 3N2O + 15H2O
13. S + 2H2SO4 đặc => 3SO2 + 2H2O
14. C + 2H2SO4 đặc => CO2 + 2SO2 + 2H2O
15. S + 4HNO3 => SO2 + 4NO2 + 2H2O
16. 3H2S + 2HNO3 đặc => 3S + 2NO + 4H2O

X1, X2, X3 là SO2, Cl2, H2O
X4, X5 là H2S, O2 dư
X6, X7, X8 là NaCl, KMnO4, H2SO4
PTHH cuối cùng e nên ktra lại đề nhé

Gọi số mol trong mỗi phần: Fe = x mol; M = y mol.
Phần 1:
Fe + 2HCl FeCl2 + H2
(mol): x x
2M + 2nHCl 2MCln + nH2
(mol): y 0,5ny
Số mol H2 = 0,07 nên x + 0,5ny = 0,07.
Phần 2:
2Fe + 6H2SO4 (đặc) Fe2(SO4)3 + 3SO2 + 6H2O
(mol): x 1,5x
2M + 2nH2SO4 (đặc) M2(SO4)n + nSO2 + 2nH2O
(mol): y 0,5nx
Số mol SO2 = 0,09 nên 1,5x + 0,5ny = 0,09. Vậy x = 0,04 và ny = 0,06.
Mặt khác: 56x + My = 2,78 nên My = 0,54. Vậy hay M = 9n.
Ta lập bảng sau:
| n | 1 | 2 | 3 |
| M | 9 ( loại ) | 18 ( loại ) | 27 ( nhận ) |
Vậy M là \(Al\) ( nhôm ) .
Đặt a là số mol Fe, b là số mol của M,trong mỗi phần,n là hóa trị của M
PTHH: Fe +2HCl ---> FeCl2 + H2
a a
2M + 2n HCl ---> 2 MCln + n H2
b bn/2
n H2= 0.07
---> a + bn/2 = 0.07 (1)
m hh A = 56a + Mb = 2.78 (2)
PTHH: Fe + 4HNO3 ----> Fe(NO3)3 + NO + 2H2O
a a
3M +4n HNO3 ---->3M(NO3)n +nNO + 2n H2O
b bn/3
n NO = a + bn/3 = 0.06 (3)
Từ (1) và (3) giải hệ ta dc : a= 0.04
bn = 0.06---> b= 0.06/n (4)
Thế à= 0.04vào pt (2) giải ra ta đc : 2.24 + Mb = 2.78
-----> b = 0.54/ M (5)
Từ (4) và (5) ----> M= 9n
Biện luận n
n=1 ----> M = 9 (loại)
n=2 ----> M= 18 (loại)
n=3-----> M=27 (nhận)
Do đó : M là Al
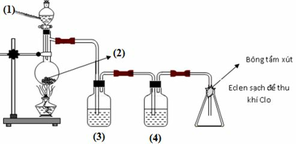
Chọn C
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O