Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- Nguyên tắc cân bằng phản ứng: Tổng số nguyên tử của một nguyên tố trước và sau phản ứng phải bằng nhau.
- Xem lại SGK lớp 8

1. Khí sinh ra do Cu + HNO3 đặc, nóng là khí NO2 (màu nâu đỏ). Cho vào ống nghiệm 1 để ngoài không khí có màu nâu đỏ. Ống nghiệm 2 để trong thùng nước đá màu nâu đỏ nhạt hơn do khi lạnh NO2 (màu nâu đỏ) chuyển hóa một phần thành N2O4 (không màu). \(PTPƯ:Cu+4HNO_3\rightarrow Cu\left(NO_3\right)_2+2NO_2+2H_2O\)
\(2NO_2\underrightarrow{^{to-thap}}N_2O_4\)
2. Hiện tượng: Phía bên cốc đựng dd NaOH sẽ nghiêng xuống làm cho cân mất thăng bằng.
Giải thích: Trong không khí luôn có một lượng nhỏ khí CO2. Dd NaOH hấp thụ khí CO2 do xảy ra
\(PTPU:2NaOH+CO_2Na_2CO_3+H_2O\)
Lượng CO2 hấp thụ thêm vào dd NaOH làm cho khối lượng cốc đựng dd NaOH tăng lên.

Câu 1. Câu trả lời đúng: B.
Hằng số K C của một phản ứng phụ thuộc duy nhất vào bản chất của phản ứng và nhiệt độ.
Câu 2. Câu trả lời đúng: D.
Pha dịch dịch 100 lần thì nồng độ giảm 100 lần ⇒ pH tăng 2 đơn vị.
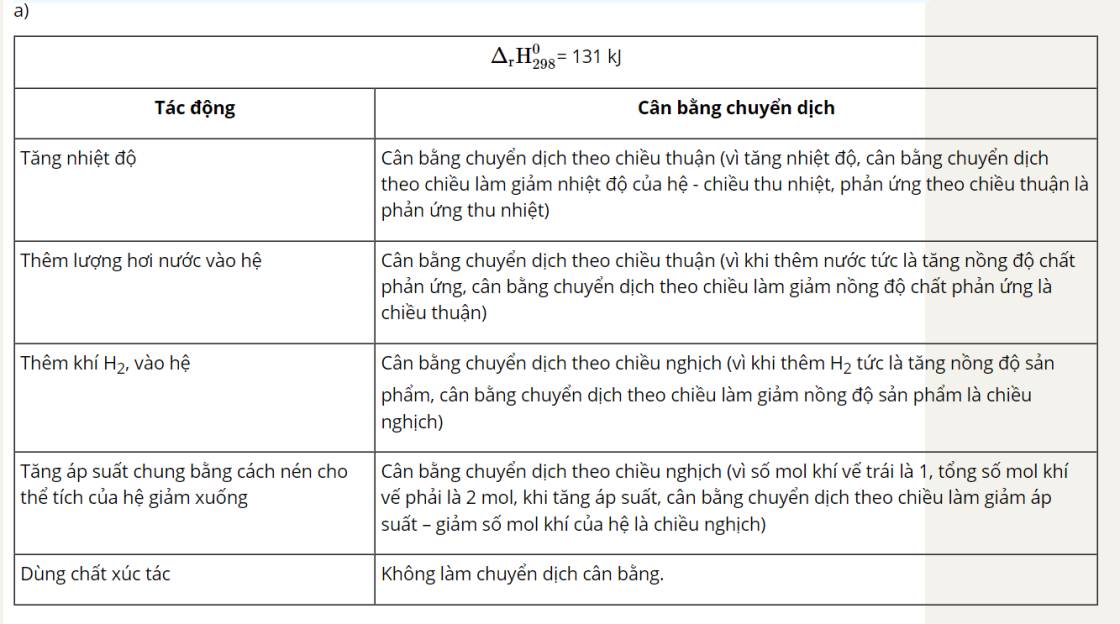
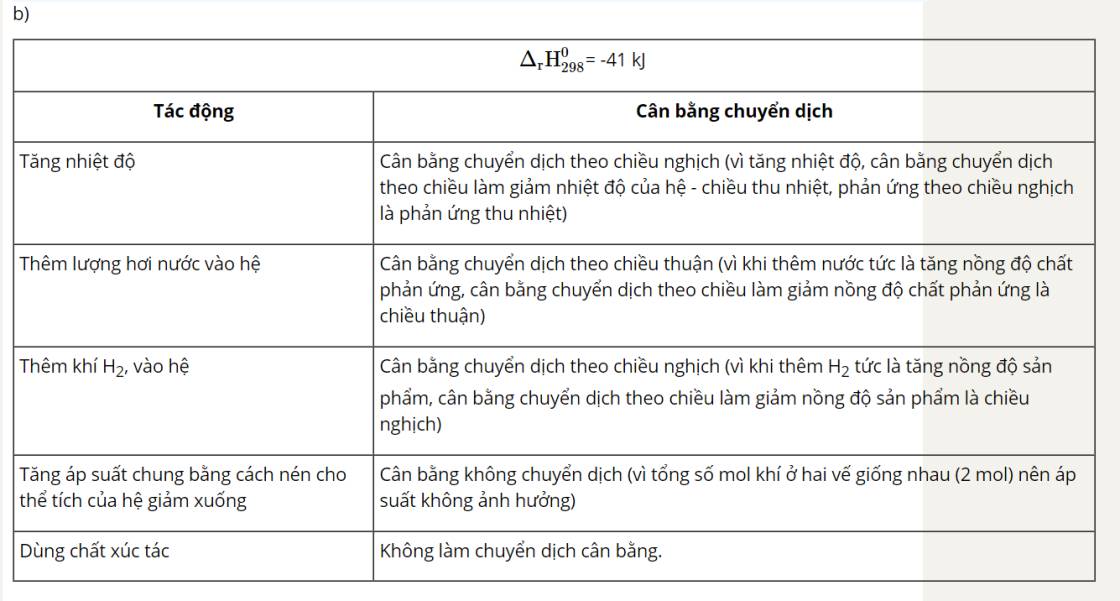
Chọn đáp án B.
Khi giảm áp suất của hệ, cân bằng chuyển dịch theo chiều làm tăng áp suất, hay làm tăng số mol khí. Do đó, cân bằng (I), (III) không chuyển dịch; cân bằng (IV) chuyển dịch theo chiều nghịch; cân bằng (II) chuyển dịch theo chiều thuận