Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi số mol của NaHCO3 và Na2CO3 trong 2 phần lần lượt là x và y (mol)
Phần I :
2NaHCO3 + Ba(OH)2 --> BaCO3↓ + Na2CO3 + H2O
Na2CO3 + Ba(OH)2 --> BaCO3↓ + NaOH
=> nBaCO3 = 1/2nNaHCO3 + nNa2CO3 = (x/2 + y) mol
=> m1 = (x/2 + y).197 gam
Phần II :
Na2CO3 + BaCl2 --> BaCO3↓ + 2NaCl
=> nBaCO3 = y mol <=> m2 = 197y gam
mà \(\dfrac{m_1}{m_2}=1.25\) => \(\dfrac{\text{(x/2 + y).197}}{197y}\)=1,25
Rút gọn phương trình => y = 2x
Vậy hỗn hợp A gồm NaHCO3 và Na2CO3 với nNa2CO3 = 2nNaHCO3
=> mA = 84x + 106.2x = 296x gam
%mNaHCO3 = \(\dfrac{84x}{296x}.100\)= 28,37% và %mNa2CO3 = 100-28,37 =71,63%

$n_{SO_2} = n_S = \dfrac{a}{32}(mol)$
$n_{NaOH} = 0,2b(mol)$
Ta thấy : d > c
Chứng tỏ X gồm hai muối $Na_2SO_3$ và $NaHSO_3$
Suy ra :
$1 < n_{NaOH} : n_{SO_2} < 2$
$⇔ 1< 0,2b : \dfrac{a}{32} < 2$
$⇔ \dfrac{a}{32} < 0,2b < \dfrac{a}{16}$
$⇔ \dfrac{5a}{32} < b < \dfrac{5a}{16}$

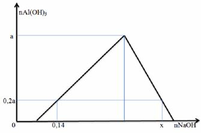
Vì nAl(OH)3 max = a → nAlCl3 = a
Giả sử số mol của AlCl3 và HCl trong mỗi phần là a, b
Bảo toàn Cl: 3a + b = 0,5 (1)
HCl + NaOH → NaCl + H2O
b → b
– Tại nNaOH = 0,14: kết tủa đang lên max (chưa bị hòa tan)
AlCl3 + 3NaOH → Al(OH)3↓ + 3NaCl
0,6a ← 0,2a
=> b + 0,6a = 0,14 (2)
Từ (1) và (2) => a = 0,15 và b = 0,05
– Tại nNaOH = x: kết tủa bị hòa tan một phần
Al(OH)3 + NaOH → NaAlO2 + 2H2O
0,12 → 0,12
Dư: 0,03
→ x = 0,05 + 3.0,15 + 0,12 = 0,62 (mol)
Vậy x = 0,62

1/Gọi công thức oxit kim loại:MxOy
_Khi cho tác dụng với khí CO tạo thành khí CO2.
MxOy+yCO=>xM+yCO2
_Cho CO2 tác dụng với dd Ca(OH)2 tạo thành CaCO3:
nCaCO3=7/100=0.07(mol)=nCO2
CO2+Ca(OH)2=>CaCO3+H2O
0.07------------------>0.07(mol)
=>nO=0.07(mol)
=>mO=0.07*16=1.12(g)
=>mM=4.06-1.12=2.94(g)
_Lượng kim loại sinh ra tác dụng với dd HCl,(n là hóa trị của M)
nH2=1.176/22.4=0.0525(mol)
2M+2nHCl=>2MCln+nH2
=>nM=0.0525*2/n=0.105/n
=>M=28n
_Xét hóa trị n của M từ 1->3:
+n=1=>M=28(loại)
+n=2=>M=56(nhận)
+n=3=>M=84(loại)
Vậy M là sắt(Fe)
=>nFe=0.105/2=0.0525(mol)
=>nFe:nO=0.0525:0.07=3:4
Vậy công thức oxit kim loại là Fe3O4.

Để dễ tính ta chia đôi lun tổng hỗn hợp : là \(\frac{5,33}{2}\)=2,665g ,
Xét phần 2: kết tủa chắc chắn chỉ có BaSO4 :0.005mol.→mol BaCl2: 0,005mol →mol(Cl-):0.005\(\times2=0,01\)
Xét p1 : mol AgNo3: 0,05mol mà mol(AgCl)↓=0,04 →2 muối hết ,Ag dư →bảo toàn ng tố Cl→mol(Cl-trong RCln)=0,04-0,01=0,03mol
m(BAcl2)=0,005\(\times208=1,04\) →m(RCln)=2,665-1,04=1,625g ,
Đặt mol RCLn :x mol →x\(\times n=0,03\)→x=\(\frac{0,03}{n}\) Ta có M(RCln)\(\times\frac{0,03}{n}\)=1,625 →Giải ra đk : R=\(\frac{56}{3}\)n → n=3,R=56 tm
Cthh : FeCl3