Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

do Cu không tác dụng với HCL , AL thì tác dụng với HCL
nên ta có AL +3HCL \(\rightarrow\)ALCL3 +\(\frac{3}{2}\)H2
số mol của khí =0,15
=>số mol của AL =\(0.15\div\frac{3}{2}\)
phần trăm của AL= \(\frac{\left(0.15\div\frac{3}{2}\right)\times27}{5}\times100\)=54%
n H2 = 3,36/ 22,4 =0,15 mol
vì cho hỗn hợp vào dung dịch HCl dư thì Cu ko t/ d nên khí H2 thoát ra là của Al phản ứng :
pthh: 2Al + 6HCl ---> 2AlCl3 + 3H2
theo pthh n Al = 2/3 n H2 = 2/3. 0,15 = 0,1 mol
---> %m Al=((0,1 .27)/5) . 100 =54%

nH2 = \(\frac{1,68}{22,4}\) = 0,075 (mol)
Mg + 2HCl \(\rightarrow\) MgCl2 + H2\(\uparrow\) (1)
0,075 <--------0,075 <--0,075 (mol)
MgO + 2HCl \(\rightarrow\) MgCl2 + H2O (2)
%mMg= \(\frac{0,075.24}{5,8}\) . 100% = 31,03 %
%m MgO = 68,97%
nMgO = \(\frac{5,8-0,075.24}{40}\) = 0,1 (mol)
Theo pt(2) nMgCl2 = nMgO= 0,1 (mol)
mdd sau pư = 5,8 + 194,35 - 0,075.2 = 200 (g)
C%(MgCl2) = \(\frac{95\left(0,075+0,1\right)}{200}\) . 100% = 8,3125%

Câu 1:
c) CM (HCl) dư = \(\frac{0,11}{0,25}\) = 0,44 (M)
ddAgồm \(\begin{cases}HCl:0,11mol\\AlCl_3:0,1mol\\CuCl_2:0,045mol\end{cases}\)
d) Các pư xảy ra theo thứ tự:
Mg + 2HCl \(\rightarrow\) MgCl2 + H2 (1)
Mg + CuCl2 \(\rightarrow\) MgCl2 + Cu (2)
3Mg + 2AlCl3 \(\rightarrow\) 3MgCl2 + 2Al (3)
Giả sử CR chỉ gồm Cu => ko xảy ra pt(3)
nCu = \(\frac{1,92}{64}\) = 0,03 (mol)
Theo pt(1) nMg= \(\frac{1}{2}\) nHCl = 0,055 (mol)
PT(2) nCu < nCuCl2 (0,03 < 0,045 )
=> CuCl2 dư
=> Giả sử đúng
mMg = (0,055 + 0,03) . 24 =2,04 (g)
Câu 3: a) Hiện tượng: Khi sục khí Cl2 vào nước vừa có tính chất vật lí , vừa tính chất hóa học:
- Vật lí: Có một phần khí tan trong nước
- Hóa học: Có chất mới tạo thành
PT: Cl2 + H2O \(\rightarrow\) HCl + HClO
b) Hiện tượng: tạo thành chất khí, cháy ở nhiệt độ cao hoặc có ánh sáng
PT: Cl2 + H2 \(\underrightarrow{t^0}\) 2HCl (khí)

Gọi số mol của Fe và Cu trong hỗn hợp lần lượt là x và y.
2Fe + 3Cl2 → 2FeCl3 (1)
x(mol) x(mol)
Cu + Cl2 → CuCl2 (2)
y(mol) y(mol)
Fe + 2HCl → FeCl2 + H2 (3)
x (mol) 2x(mol) x(mol).
Theo điều kiện bài toán và phương trình hoá học (3) ta có: 127x = 25,4 → x = 0,2
Theo phương trình phản ứng (1) và (2) ta có: 162,5x + 135y = 59,5
Vậy y = 0,2.
Khối lượng mỗi muối là: m FeCl3=32,5gam
m CuCl2=27gam
%FeCl3 = 54,62%.
%CuCl2 = 45,38%

Chọn B
Gọi a là số mol của CuO và b là số mol của F e 2 O 3 có trong 20 gam
hh 200 ml dd HCl 3,5 M => nHCl = 0,2 . 3,5 = 0,7 mol
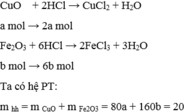
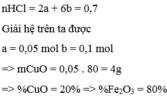
Chọn A