Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Cốc A: Fe + 2HCl ---> FeCl2 + H2 (1)
0,2 0,2 mol
Cốc B: 2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2 (2)
m/27 m/18 mol
Số mol Fe = 11,2/56 = 0,2 mol; số mol Al = m/27 mol.
Khối lượng cốc A tăng = khối lượng Fe - khối lượng H2 (bay ra) = 11,2 - 2.0,2 = 10,8 gam.
Khối lượng cốc B tăng = khối lượng Al - khối lượng H2 = m - 2.m/18 = m - m/9 = 8m/9 gam.
Vì cân ở vị trí cân bằng nên khối lượng tăng cốc A = khối lượng tăng ở cốc B. Suy ra: 8m/9 = 10,8 hay m = 12,15 g
Cốc A: Fe + 2HCl ---> FeCl2 + H2 (1)
0,2 0,2 mol
Cốc B: 2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2 (2)
m/27 m/18 mol
Số mol Fe = 11,2/56 = 0,2 mol; số mol Al = m/27 mol.
Khối lượng cốc A tăng = khối lượng Fe - khối lượng H2 (bay ra) = 11,2 - 2.0,2 = 10,8 gam.
Khối lượng cốc B tăng = khối lượng Al - khối lượng H2 = m - 2.m/18 = m - m/9 = 8m/9 gam.
Vì cân ở vị trí cân bằng nên khối lượng tăng cốc A = khối lượng tăng ở cốc B. Suy ra: 8m/9 = 10,8 hay m = 12,15 g

Câu hỏi của Dịch Thiên Tổng - Hóa học lớp 8 | Học trực tuyến

Thí nghiệm 1 :
\(Zn + 2HCl \to ZnCl_2 + H_2\\ n_{H_2} = n_{Zn} = \dfrac{13}{65} = 0,2(mol)\\ \Rightarrow m_{tăng} =m_{Zn} -m_{H_2} = 13 - 0,2.2 = 12,6(gam)\)
Thí nghiệm 2 :
\(2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2\\ n_{H_2} = \dfrac{3}{2}n_{Al} = \dfrac{3}{2}.\dfrac{a}{27} = \dfrac{a}{18}(mol)\\ \Rightarrow m_{tăng} = a - \dfrac{a}{18}.a = \dfrac{8}{9}a\)
Vì cân ở vị trí cân bằng nên :
\(12,6 = \dfrac{8}{9}a\\ \Leftrightarrow a = 14,175(gam)\)
bạn ơi ý b :lấy A (G) NHÔM ở trên td vs 1095(g) HCL 5%.tính nồng độ phần trăm của dd thu đc sau pư bn giải giúp mk nhé

công thức 1 đúng
vì Cu có hai hoá trị là hoá trị 1 và hoá trị 2 dựa theo quy tắc hoá trị thì trong công thức 1 nếu Cu có hoá trị 1 thì1.1=2.1=> vô lý
nếu Cu hoá trị 2 =>1.2=2.1(hợp lý)
mấy công thức dưới làm tương tự

a) \(Ca+2H_2O\rightarrow Ca\left(OH\right)_2+H_2\uparrow\)
\(n_{Ca}=\frac{8}{40}=0,2mol\)
Theo phương trình \(n_{H_2}=n_{Ca}=0,2mol\)
\(\rightarrow V_{H_2}=0,2.22,4=4,48l\)
b) Theo phương trình \(n_{Ca\left(OH\right)_2}=n_{Ca}=0,2mol\)
\(\rightarrow m_{Ca\left(OH\right)_2}=0,2.\left(40+17.2\right)=14,8g\)
\(m_{ddsaupu}=m_{Ca}+m_{H_2O}-m_{H_2}\)
\(\rightarrow m_{ddsaupu}=8+200-0,2.2=207,6g\)
\(\rightarrow C\%_{ddCa\left(OH\right)_2}=\frac{14,8.100}{207,6}=7,13\%\)

nFe =
nFe = 0.2 (mol).
nAl =
Xét thí nghiệm 1, ta có phương trình phản ứng:
Fe + 2HCl → FeCl2 + H2
0.2 0.4 0.2 0.2 (Mol)
Dung dịch sau phản ứng có chứa: FeCl2 - 0.2 mol và có thể có axit dư
Xét thí nghiệm 2, ta có phương trình phản ứng:
2Al + 3H2SO4 → Al2(SO4)3 + 3H2
m/27 m/54 3m/54 (Mol)
Dung dịch sau phản ứng có chứa: Al2(SO4)3 hoặc có thể có axit còn dư
Vì sau khi phản ứng cái kim đồng hồ cân nặng vẫn ở vị trí cân bằng nên ta có thể suy luận như sau:
Khối lượng kim loại Nhôm khi cho vào cốc A trừ đi khối lượng đã mất đi là khí Hidro ở cốc A phải bằng Khối lượng kim loại Nhôm cho vào cốc B trừ đi lượng khí Hidro thoát ra ở cốc B
Vậy ta có phương trình cân bằng khối lượng của 2 cốc như sau:
Cốc A{mFe - mH2} = Cốc B{mAl - mH2}
11.2 - 0.2*2 = m - 6m/54
48m = 583.2
=>m = 12.15 (g)

Bài của Minh mình thấy chưa được nha chưa trừ đi mH2 đã được giải phóng
- Xét đĩa cân có Al và H2SO4: (Gọi là đĩa A)
\(n_{Al}=\dfrac{m}{27}\left(mol\right)\)
PTHH: 2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2
\(\dfrac{m}{27}\)-->\(\dfrac{m}{18}\)--------------------------->\(\dfrac{m}{18}\)
=> mA (sau pư) = \(m+\dfrac{98m}{18}-\dfrac{2m}{18}=\dfrac{19m}{3}\left(g\right)\)
Xét đĩa cân có Mg và HCl: (Gọi là đĩa cân B)
\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
PTHH: Mg + 2HCl ---> MgCl2 + H2
0,2---->0,4------------------->0,2
=> mB (sau pư) = 4,8 + 0,4.36,5 - 0,2.2 = 19 (g)
Mà mA = mB
\(\rightarrow\dfrac{19m}{3}=19\\ \Leftrightarrow m=3\left(g\right)\)
\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\\
pthh:Mg+2HCl\rightarrow MgCl_2+H_2\)
0,2 0,4
=> \(m_{HCl}=0,4.98=39,2\left(g\right)\\
m_{Mg}+m_{HCl}=4,8+39,2=44g\)
vì 2 đĩa cân bằng nhau
=> \(m_{Mg}+m_{HCl}=m_{Al}+m_{H_2SO_4}\)
=> \(m_{Al}=m_{Mg}+m_{HCl}-m_{H_2SO_4}=4,8+39,2-39,2=4,8\left(g\right)\)
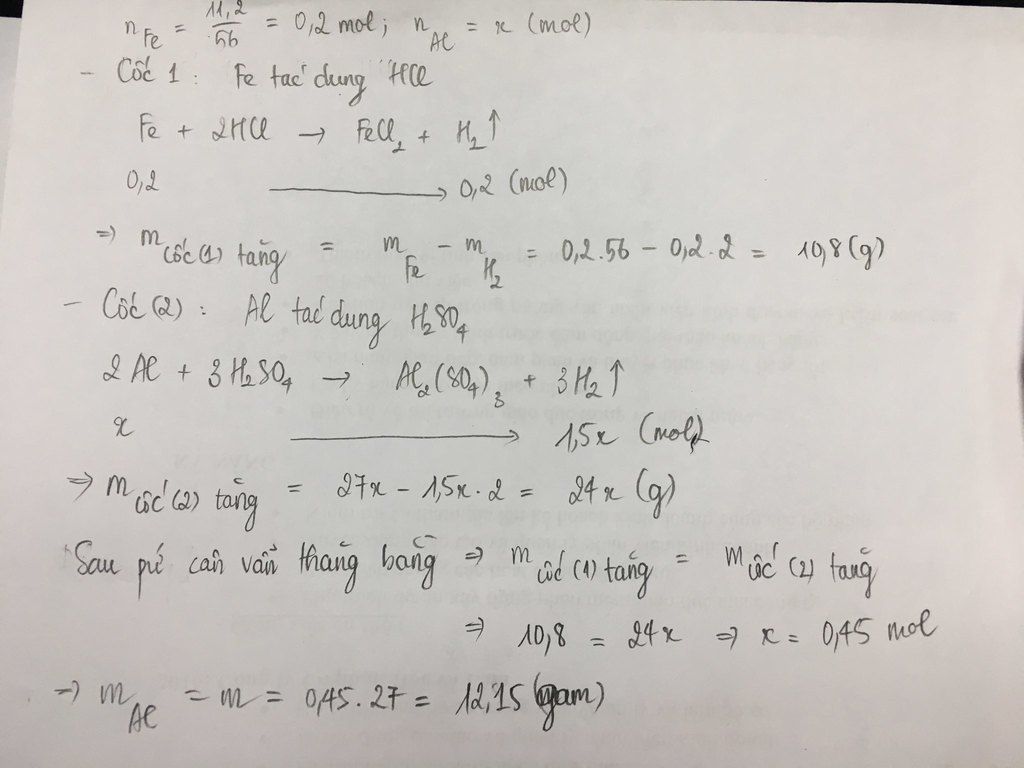
- TN1: \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
0,2------------------->0,2
=> mtăng = 13 - 0,2.2 = 12,6 (g) (1)
- TN2:
\(n_{Al}=\dfrac{a}{27}\left(mol\right)\)
PTHH: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
\(\dfrac{a}{27}\)--------------------------->\(\dfrac{a}{18}\)
=> \(m_{tăng}=a-\dfrac{a}{18}.2=\dfrac{8}{9}a\left(g\right)\) (2)
(1)(2) => \(\dfrac{8}{9}a=12,6\Rightarrow a=14,175\left(g\right)\)