Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi có ít nhất một trong các điều kiện sau:
- Tao thành chất kết tủa
Ví dụ: AgNO3 + NaCl \(\rightarrow\)AgCl\(\downarrow\)+ NaNO3
- Tạo thành chất điện li yếu
Ví dụ: CH3COONa + HCl \(\rightarrow\) CH3COOH + NaCl
- Tạo thành chất khí
Ví dụ: Na2CO3 + H2SO4 -> Na2SO4 + CO2\(\uparrow\) + H2O
Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi các ion kết hợp được với nhau tạo thành ít nhất một trong các chất sau :
- Chất kết tủa :
Ví dụ: AgNO3+HCl→AgCl↓+HNO3AgNO3+HCl→AgCl↓+HNO3
- Chất điện li yếu :
Ví dụ : HCl+CH3COONa→CH3COOH+NaClHCl+CH3COONa→CH3COOH+NaCl
- Chất khí:
Ví dụ: 2HCl+Na2CO3→2NaCl+CO2↑+H2O
bạn xem thêm tại link này nhé: https://cunghocvui.com/bai-viet/bai-1-trang-20-sach-giao-khoa-hoa-11.html

Thí dụ 1: AgNO3 + NaCl → AgCl ↓ + NaNO3
AgNO3, NaCl, NaNO3 là những chất điện li mạnh trong dung dịch, chúng phân li thành các ion. Ta có phương trình ion:
Ag+ + NO3- + Na+ + Cl- → AgCl ↓ + NO3- + Na+
Vậy thực chất trong dung dịch chỉ có phản ứng của:
Ag+ + Cl- → AgCl ↓
Còn các ion NO3- và Na+ vẫn tồn tại trong dung dịch trước và sau phản ứng.
Thí dụ 2: Na2SO3 + 2HCl → 2 NaCl + H2O + SO2 ↑
Na2SO3, HCl, và NaCl là những chất điện li mạnh trong dung dịch, chúng phân li thành các ion. Ta có phương trình ion:
2Na+ + SO32- + 2H+ + 2Cl- → 2Na+ + 2Cl- + H2O + SO2 ↑
2H+ + SO32- → H2O + SO2 ↑
Vậy thực chất trong dung dịch chỉ có phản ứng của 2H+ và SO32- còn các ion Na+ và Cl- vẫn tồn tại trong dung dịch trước và sau phản ứng. Thực chất các phản ứng trong dung dịch điện li là phản ứng giữa các ion vì các chất điện li đã phân li thành các ion.

Bản chất của phản ứng trong dung dịch các chất điện li là phản ứng giữa các ion. Thật vậy:
- NaCl + AgNO3 → AgCl ↓ + NaNO3
Bản chất Ag+ + Cl‑ → AgCl ↓
- MgCl2 + 2NaOH → Mg(OH)2 ↓+ 2NaCl
Bản chất: Mg2+ + 2OH– → Mg(OH)2 ↓

Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi
A. Các chất phản ứng phải là những chất dễ tan.
B. Các chất phản ứng phải là những chất điện li mạnh.
C. Một số ion trong dung dịch kết hợp được với nhau làm giảm nồng độ ion của chúng
D. Phản ứng không phải là thuận nghịch.

Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi
A. Các chất phản ứng phải là những chất dễ tan.
B. Các chất phản ứng phải là những chất điện li mạnh.
C. Một số ion trong dung dịch kết hợp được với nhau làm giảm nồng độ ion của chúng
D. Phản ứng không phải là thuận nghịch.

- Tạo thành chất kết tủa: NH4Cl + AgNO3 → NH4NO3 + AgCl\(\downarrow\)
Ag+ + cl‑ \(\rightarrow\) AgCl\(\downarrow\)
- Tạo thành chất điện li yếu: NaOH + HCl \(\rightarrow\)NaCl + H2O
H+ + OH– \(\rightarrow\) H2O
- Tạo thành chất khí: K2CO3 + 2HCl \(\rightarrow\) 2KCl + CO2\(\uparrow\) + H2O
2H+ + CO32– → CO2\(\uparrow\) + H2O
- Tạo thành chất kết tủa: NH4Cl + AgNO3 \(\rightarrow\) NH4NO3 + AgCl\(\downarrow\)
Ag+ + cl‑ → AgCl\(\downarrow\)
- Tạo thành chất điện li yếu: NaOH + HC1 \(\rightarrow\)NaCl + H2O
H+ + OH– \(\rightarrow\)H2O
- Tạo thành chất khí: K2CO3 + 2HC1 \(\rightarrow\) 2KC1 + CO2\(\uparrow\) + H2O
2H+ + CO32– \(\rightarrow\) CO2\(\uparrow\) + H2O
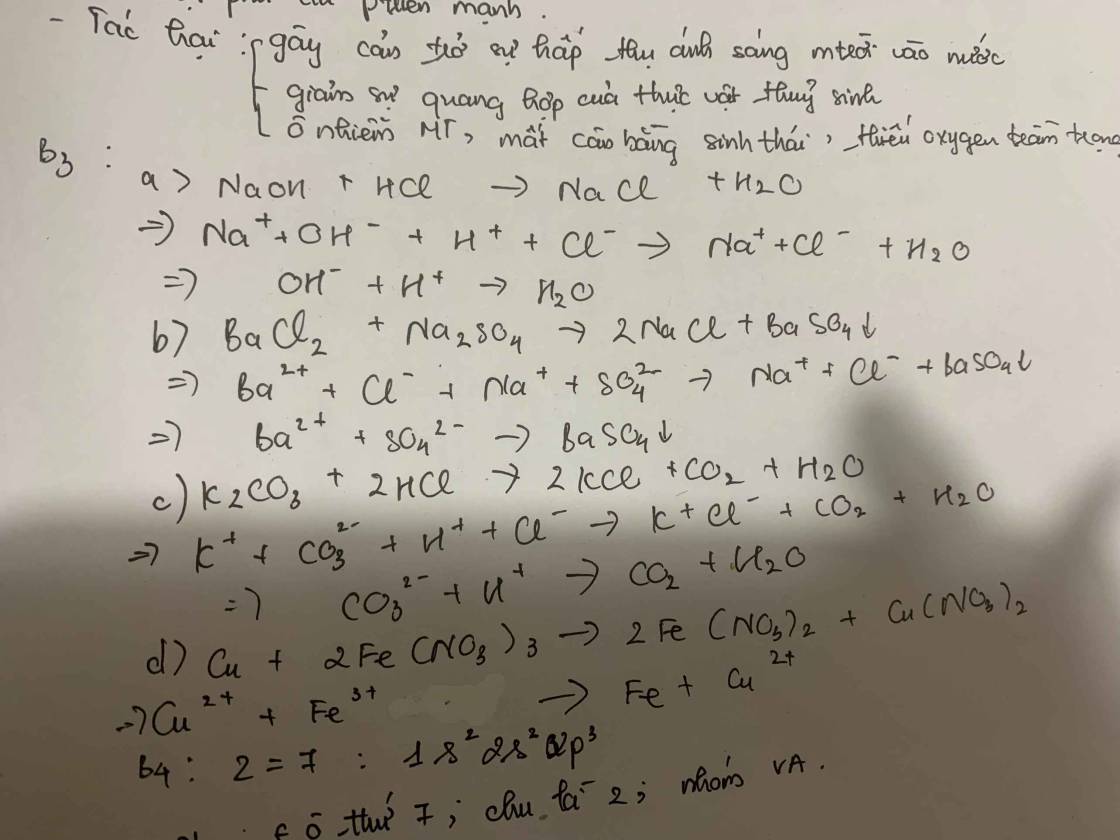
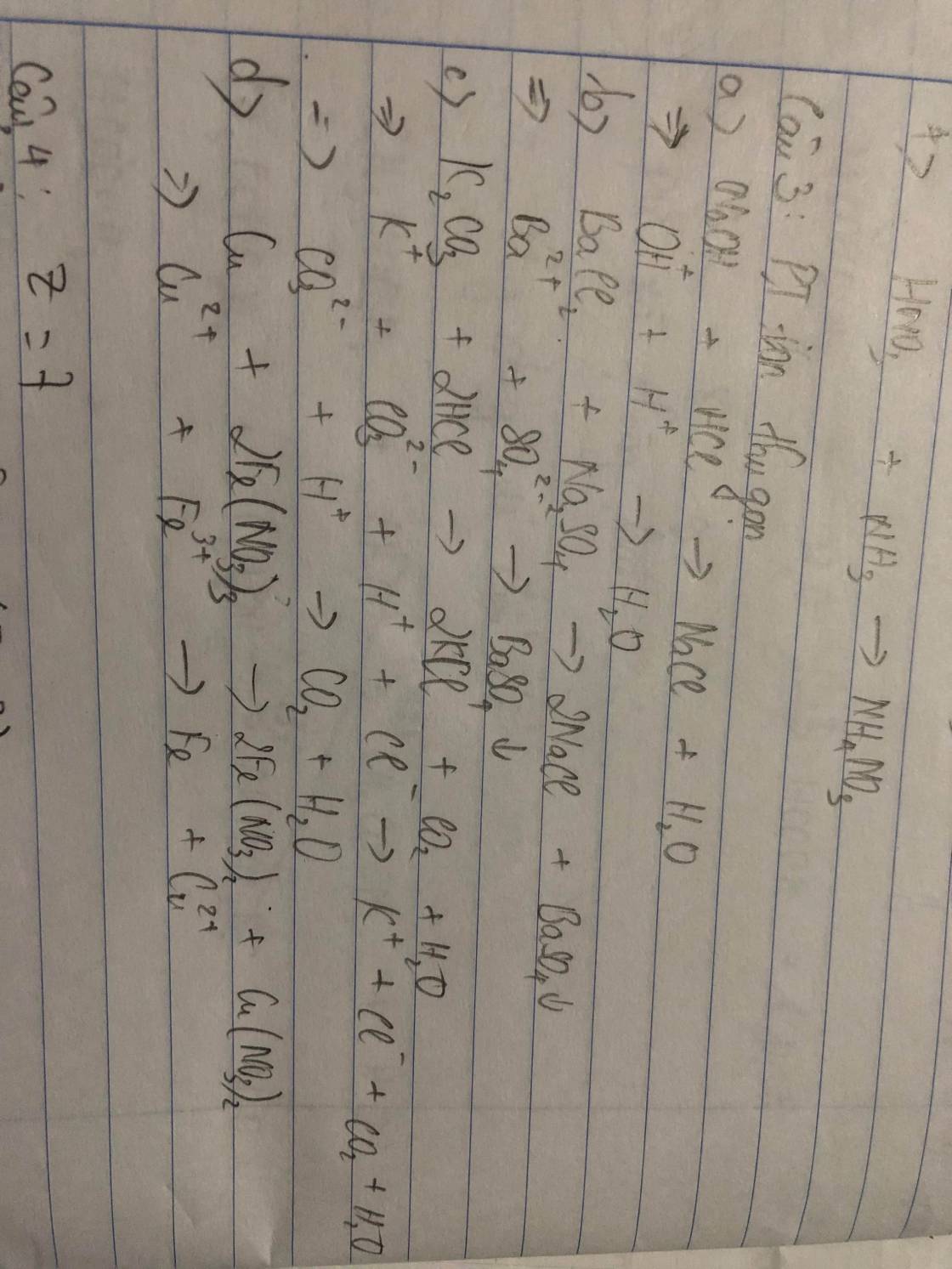
Bản chất của phản ứng trong dung dịch các chất điện li là phản ứng giữa các ion. Thật vậy:
Bản chất Ag+ + Cl‑ \(\rightarrow\) AgCl \(\downarrow\)
Bản chất: Mg2+ + 2OH– \(\rightarrow\) Mg(OH)2\(\downarrow\)