Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Ta có: \(n_{H_2}=\frac{m_{H_2}}{M_{H_2}}=\frac{0,4}{2}=0,2\left(mol\right)\)
PTHH : 2H2 + O2 -> 2H2O
b) Theo PTHH và đề bài, ta có:
\(n_{H_2O}=n_{H_2}\)= 0,2 (mol)
Khối lượng thu được là:
\(m_{H_2}=n_{H_2}.M_{H_2}=0,2.18=3,6\left(g\right)\)
c) Ta có:
\(n_{O_2}=\frac{n_{H_2}}{2}=\frac{0,2}{2}=0,1\left(mol\right)\)
Thể tích khí O2 đã sử dụng ở điều kiện tiêu chuẩn:
\(V_{O_2\left(đktc\right)}=n_{O_2}.22,4=0,1.22,4=2,24\left(l\right)\)
1) H2 + O2 → 2HCl
2) nH2 = \(\frac{m}{M}\) =\(\frac{0,4}{2}\) = 0,2 mol
H2 + O2 → 2HCl
0,2 → 0,2→ 0,4mol
mHCl= n. M = 0,4 . 35,5 = 14,2 g
3) VO2= n . 22,4 = 0,2 . 22,4 = 4,48 l
Mình không bt là cách trình bày của mình có đúng không nhưng về đáp asnn thì mình chắc 100% đấy!!!!!!!!!!!!!!![]()

\(n_{Mg}=\dfrac{2,4}{24}=0,1mol\)
\(2Mg+O_2\rightarrow\left(t^o\right)2MgO\)
0,1 0,05 0,1 ( mol )
\(V_{O_2}=0,05.22,4=1,12l\)
\(m_{MgO}=0,1.40=4g\)
nMg= 2,4 : 24 = 0,1 ( mol )
pthh 2 Mg + O2 -t--> 2MgO
0,1 ---> 0,05 --->0,1 (mol
=> VO2 = 0,05 . 22,4 = 1,12 (l)
=> mMgO = 0,1 . 40 = 4 (G)

mMg = 3.6/24 = 0.15 (mol)
2Mg + O2 -to-> 2MgO
0.15__0.075____0.15
mMgO= 0.15*40 = 6 (g)
VO2 = 0.075*22.4 = 1.68 (l)
2KClO3 -to-> 2KCl + 3O2
0.05_______________0.075
mKClO3 = 0.05*122.5 = 6.125 (g)
PTHH: \(2Mg+O_2\underrightarrow{t^o}2MgO\)
a+b) Ta có: \(n_{Mg}=\dfrac{3,6}{24}=0,15\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{O_2}=0,075\left(mol\right)\\n_{MgO}=0,15\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{O_2}=0,075\cdot22,4=1,68\left(l\right)\\m_{MgO}=0,15\cdot40=6\left(g\right)\end{matrix}\right.\)
c) PTHH: \(2KClO_3\xrightarrow[MnO_2]{t^o}2KCl+3O_2\uparrow\)
Theo PTHH: \(n_{KClO_3}=0,05\left(mol\right)\)
\(\Rightarrow m_{KClO_3}=0,05\cdot122,5=6,125\left(g\right)\)

a) Viết công thức về khối lượng của phản ứng xảy ra.
b0 Tính khối lượng của khí oxi phản ứng.
Hướng dẫn giải:
a) Công thức về khối lượng của phản ứng
mMg + mO2 = mMgO
b) Khối lượng của khí oxi tham gia phản ứng:
mO2 = mMgO – mMg
=> mO2 = 15 – 9 = 6(g)
Ta có : Sau khi cân bằng phương trình trên được :
2Mg + O2 ===> 2MgO
Công thức về khối lượng của phản ứng trên là :
m2Mg + mO2 = m2MgO
Từ trên => 9 gam+ mO2 = 15 gam
=> mO2 = 6 gam
Vậy khối lượng Oxi đã phản ứng là 6 gam

\(n_{Mg}=\dfrac{2,4}{24}=0,1\left(mol\right)\\ a,2Mg+O_2\rightarrow\left(t^o\right)2MgO\\ n_{O_2}=\dfrac{0,1}{2}=0,05\left(mol\right)\\ V_{O_2\left(đktc\right)}=0,05.22,4=1,12\left(l\right)\\ b,2KClO_3\rightarrow\left(t^o\right)2KCl+3O_2\\ n_{KClO_3}=\dfrac{0,05.2}{3}=\dfrac{1}{30}\left(mol\right)\\ \Rightarrow m_{KClO_3}=\dfrac{122,5}{30}=\dfrac{49}{12}\left(g\right)\)

nMg = 9,6/24 = 0,4 (mol)
2Mg + O2 ---to---> 2MgO
0,4____0,2_________0,4
VO2(đktc) = 0,2.22,4 = 4,48(l)
mMgO = 0,4.40 = 16(g)

a, PT: \(2Mg+O_2\underrightarrow{t^o}2MgO\)
b, Ta có: \(n_{MgO}=\dfrac{2,4}{40}=0,06\left(mol\right)\)
Theo PT: \(n_{O_2}=\dfrac{1}{2}n_{MgO}=0,03\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,03.22,4=0,672\left(l\right)\)
c, PT: \(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
Theo PT: \(n_{KClO_3}=\dfrac{2}{3}n_{O_2}=0,02\left(mol\right)\)
\(\Rightarrow m_{KClO_3}=0,02.122,5=2,45\left(g\right)\)
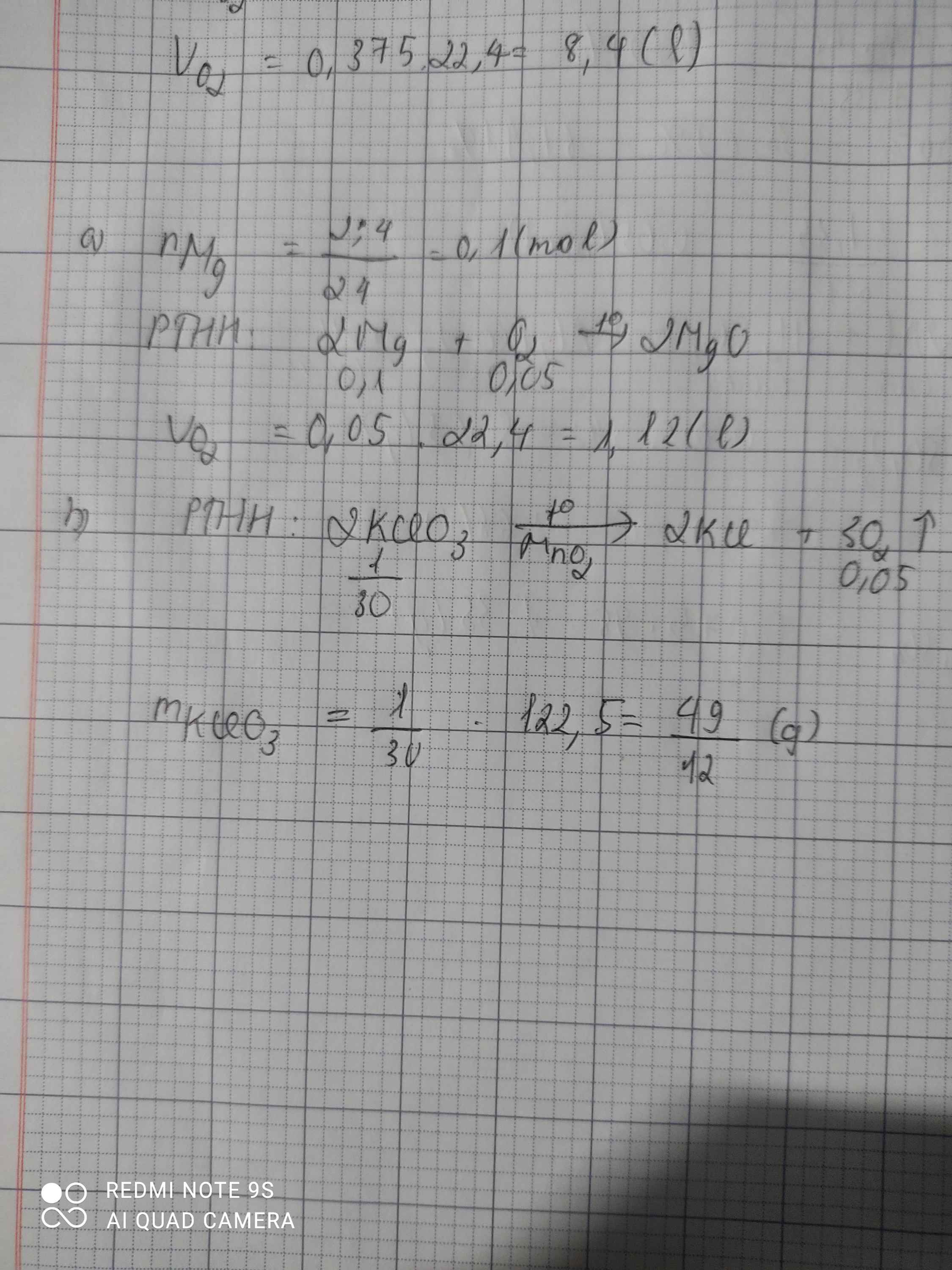
a.Mg + 1/2O2 -> MgO
b.\(nMg=\dfrac{4.8}{24}=0.2mol\) => \(nO2=0.2\times\dfrac{1}{2}=0.1mol\)
\(V_{O2}=0.1\times22.4=2.24l\)
c.\(nMgO=nMg=0.2mol\)
\(mMgO=0.2\times40=8g\)
con cảm ơn cô ạ