Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

(a) Gọi CTPT của các chất là CxHyOz
M<170 => mC<170.55,8% => 12x<94,86 => x<7,9
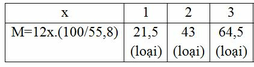
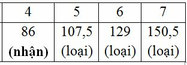
Vậy CTPT có dạng: C4HyOz (y≤10)(Do M là các số nguyên và là số chẵn)
Ta có: 12.4 + y + 16z = 86 => y + 16z = 38
+ z = 1: y = 22 (loại)
+ z = 2: y = 6 (nhận)
Vậy CTPT của các chất là: C4H6O2
b) A, B đều có nhóm CH3 và phản ứng với NaHCO3 tạo khí và chỉ có B có đồng phân hình học nên cấu tạo của A và B là:
A: CH2=C(CH3)-COOH
B: CH3-CH=CH-COOH
F, H, K có phản ứng với NaHCO3 tạo khí nên F, H, K là các axit.
- G là hợp chất không bền và chuyển hóa ngay thành G’ (G và G’ có cùng công thức phân tử) và khi oxy hóa bằng H2CrO4, hợp chất G’ chuyển hóa thành F nên G’ và F có cùng số nguyên tử C
C: CH3COOCH=CH2
F: CH3COOH
G: CH2=CH-OH
G’: CH3CHO
- H có phản ứng với NaHCO3 tạo khí nên H là axit. Mặt khác, phản ứng của H với bạc nitrat trong amoniac chỉ tạo thành các chất vô cơ nên H là HCOOH
D: HCOOCH2-CH=CH2
H: HCOOH
I: CH2=CH-CH2-OH
- L bị oxi hóa tạo HCOOH nên L là CH3OH
E: CH2=CH-COOCH3
K: CH2=CH-COOH
L: CH3OH
(1) CH2=C(CH3)-COOH (A) + NaHCO3 → CH2=C(CH3)-COONa + H2O + CO2
(2) CH3-CH=CH-COOH (B) + NaHCO3 → CH3-CH=CH-COONa + H2O + CO2
(3) CH3COOCH=CH2 (C) + NaOH → CH3COONa + CH3CHO (G’)
(4) CH3COONa + HCl → CH3COOH (F) + NaCl
(5) HCOOCH2-CH=CH2 (D) + NaOH → HCOONa + CH2=CH-CH2-OH (I)
(6) HCOONa + HCl → HCOOH (H) + NaCl
(7) CH2=CH-COOCH3 (E) + NaOH → CH2=CH-COONa + CH3OH (L)
(8) CH2=CH-COONa + HCl → CH2=CH-COOH (K) + NaCl
(9) CH3CHO + H2CrO4 → CH3COOH + H2CrO3
(10) CH3OH + 2H2CrO4 → HCOOH + 2H2CrO3 + H2O
(11) HCOOH + 2AgNO3 + 4NH3 + H2O → (NH4)2CO3 + 2Ag + 2NH4NO3
(c) Phản ứng polime hóa của A và C:
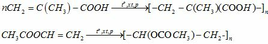
(d)


a.
BTKL ta có mX = mY => nX . MX = nY . mY
MX / My = nY / mY =0.75
Đặt nX = 1 mol => nY = 0,75 mol => nH2 phản ứng = 1 – 0,75 = 0,25mol
* TH hidrocacbon là anken: n anken = n H2 = 0,25 mol => n H2 trong X = 0,75 => M = (6,75 – 0,75 . 2)/0,25 = 21 (loại) * TH là ankin: => n akin = 0,25/2 = 0,125 => n H2 trong X = 0,875 mol => M = (6,75 – 0,875 . 2)/0,125 = 40 =>C3H4
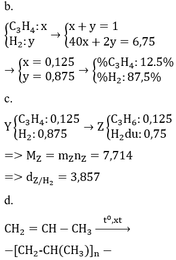


Phản ứng xà phòng hóa:
\(\left(C_{17}H_{33}COO\right)_3C_3H_5+3NaOH\xrightarrow[OH^-]{t^o}3C_{17}H_{33}COONa+C_3H_5\left(OH\right)_3\)
\(m_{C_{17}H_{33}COONa}=\dfrac{10\cdot72\%}{100\%}=7,2g\Rightarrow n_{C_{17}H_{33}COONa}=\dfrac{7,2}{304}=\dfrac{9}{380}mol\)
Theo pt: \(n_{chấtbéo}=\dfrac{n_{C_{17}H_{33}COONa}}{3}=\dfrac{\dfrac{9}{380}}{3}=\dfrac{3}{380}mol\Rightarrow m_{chấtbéo}=\dfrac{3}{380}\cdot884=6,98kg\)
\(n_{NaOH}=n_{C_{17}H_{33}COONa}=\dfrac{9}{380}mol\Rightarrow m_{NaOH}=\dfrac{9}{380}\cdot40=0,95kg=950g\)

_Nung nóng hỗn hợp gồm CuO và PbO bằng C:
Gọi a,b là số mol của CuO và PbO:
=>80a+223b=19.15(1)
2CuO+C(t*)=>2Cu+CO2
a------->0.5a--->a--->0.5a(mol)
2PbO+C(t*)=>2Pb+CO2
b------>0.5b---->b---->0.5b(mol)
_Cho CO2 sản phẩm vào dd Ca(OH)2 thu được kết tủa trắng CaCO3:
+nCaCO3=7.5/100=0.075(mol)
CO2+Ca(OH)2=>CaCO3+H2O
0.075---------------->0.075(mol)
=>0.5a+0.5b=0.075(2)
Từ(1)(2)=>a=0.1,b=0.05
=>mCuO=0.1*80=8(g)
=>mPbO=0.05*223=11.15(g)
+nCu=0.1(mol)
=>mCu=0.1*64=6.4(g)
+nPb=0.05(mol)
=>mPb=0.05*207=10.35(g)
=>m(KL)=6.4+10.35=16.75(g)
c)
+nC=0.5(a+b)=0.5(0.1+0.05)=0.075(mol)
=>mC=0.075*12=0.9(g)



a) Gọi số mol của FeCO3: x (mol) ;
số mol của FeS2: y (mol)
4FeCO3 + O2 → Fe2O3 + 4CO2↑
x → 0,25x → x (mol)
4FeS2 +11O2 → 2Fe2O3 + 8SO2↑
y → 2,75y → 2y (mol)
∑ nO2 = 0,25x + 2,75y (mol)
Cùng điều kiện về nhiệt độ và áp suất nên tỉ lệ về thể tích = tỉ lệ về số mol
=> nN2 = 4nO2 = 4(0,25x + 2,75y)
=> nN2 = x + 11y (mol)
Vậy hỗn hợp Y gồm:

Khối lượng Fe có trong Z là:

Vì H = 80% => nFe2O3 (trong X) = 0,12. 100% : 80% = 0,15 (mol)
nFe2O3 dư (trong Z) = 0,15 – 0,12 = 0,03 (mol)
Khối lượng tạp chất trong Z = 27,96 – mFe – mFe2O3 dư = 27,96 – 0,24.56 – 0,03.160 = 9,72 (g)
Bảo toàn nguyên tố Fe => nFeCO3 + nFeS2 = 2nFe2O3(trong X)
=> x + y = 0,3 (2)
Từ (1) và (2) => x = 0,18 và y = 0,12 (mol)
Áp dụng công thức PV = nRT ( với n = nCO2 + nSO2 + nN2 = 0,18 + 2. 0,12 + 0,18 +11.0,12 = 1,92)
=> P.10 = 1,92.0,082. (136,5 +273)
=> P = 6,447 ( atm) ≈ 6,5 (atm)
Ta có: mA = mFeCO3 + mFeS2 + mtạp chất = 0,18.116 + 0,12.120 + 9,72 = 45 (g)
![]()
b) hỗn hợp Y gồm:

Cho hỗn hợp Y qua O2 ( xúc tác V2O5 ) có phản ứng sau:

Khối lượng dd sau: mdd sau = mSO3 + mH2O = 0,24. 80 + 592,8 = 612 (g)


Câu 1 : C \(BaCl_2+Na_2SO_4\rightarrow BaSO_4+2NaCl\)
Câu 2 : B
\(n_{MgO}=\dfrac{16}{40}=0,4\left(mol\right)\)
a) Pt : \(MgO+2HCl\rightarrow MgCl_2+H_2O\)
0,4------>0,8------->0,4
b) \(C_{MddHCl}=\dfrac{0,8}{0,1}=8M\)
\(C_{MMgCl2}=\dfrac{0,4}{0,1}=4M\)
Câu 4 :
\(n_{BaCl2}=\dfrac{10,4\%.100}{100\%.208}=0,05\left(mol\right)\)
a) Pt : \(BaCl_2+H_2SO_4\rightarrow BaSO_4+2HCl\)
b) \(n_{BaCl2}=n_{BaSO4}=0,05\left(mol\right)\Rightarrow m_{kt}=m_{BaSO4}=0,05.233=11,65\left(g\right)\)

\(\left(C_{17}H_{33}COO\right)_3C_3H_5+3H_2O\underrightarrow{H^+,t^o}3C_{17}H_{33}COOH+C_3H_5\left(OH\right)_3\)
\(n_{chấtbéo}=\dfrac{4,42}{884}=5\cdot10^{-3}mol\)
Theo pt: \(n_{axitbéo}=3n_{chấtbéo}=3\cdot5\cdot10^{-3}=0,015mol\)
\(m_{axitbéo}=0,015\cdot282=4,23g\)
a) Chất béo tan không trong nước nhưng tan trong benzen và dầu hỏa
b) Phản ứng xà phòng hóa là phản ứng thủy phân este trong môi trường kiềm tạo ra glixerol và các muối của axiit béo
c) Phản ứng của chất béo với nước trong môi trường axit là phản ứng thủy phân nhưng không là phản ứng xà phòng hóa.