Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a/ CT oxit: $CuO$
b/ Vậy CT X: $CuSO_4.5H_2O$
Giải thích các bước giải:
Gọi công thức oxit là: $MO$
Số mol oxit là a mol
$MO+H_2SO_4\to MSO_4+H_2O$
Theo PTHH
$n_{H_2SO_4}=n_{MSO_4}=n_{MO}=a\ mol$
$⇒m_{dd\ H_2SO_4}=\dfrac{98a.100}{24,5}=400a$
$⇒m_{dd\ A}=a.(M+16)+400a = aM+416a$
$m_{MSO_4}=a.(M+96)$
Do nồng độ muối là 33,33% nên:
$\dfrac{a.(M+96)}{aM+416a}.100\%=33,33\\⇒M=64$
Vậy M là Cu, công thức oxit: $CuO$
b.
Trong 60 gam dung dịch muối A có:
$m_{CuSO_4}=\dfrac{60.33,33}{100}=20g$
Gọi công thức tinh thể tách ra là: $CuSO_4.nH_2O$
Khối lượng dung dịch còn lại là:
$60-15,625=44,375g ⇒ m_{CuSO_4\ trong\ dd}=\dfrac{44,375.22,54}{100}=10g$
$⇒m_{CuSO_4\ trong\ tinh\ thể}=20-10=10g$
$⇒n_{tinh\ thể}=n_{CuSO_4}=0,0625\ mol$
$⇒M_{tinh\ thể}=15,625:0,0625=250⇒n=5$
Vậy CT X: $CuSO_4.5H_2O$

a) Gọi công thức oxit là: MO
Số mol oxit là a mol
MO+H2SO4→MSO4+H2O
Theo PTHH
nH2SO4=nMSO4=nMO=a mol
⇒mdd H2SO4=98a.100/24,5=400a
⇒mdd A=a.(M+16)+400a=aM+416a
mMSO4=a.(M+96)
Do nồng độ muối là 33,33% nên:
a.(M+96)/aM+416a.100%=33,33⇒M=64
Vậy M là Cu, công thức oxit: CuO

Đặt kim loại là M, oxit là MO
Giả sử có 1 mol MO phản ứng, 1 mol H2SO4 phản ứng:
MO + H2SO4 -> MSO4 + H2O
C% = mct / mdd . 100%
10% = 1 . 98 / mdd . 100%
-> mDd H2SO4 = 980 g
Theo định luật bảo toàn khối lượng ta có:
Mdd = mMO + mddH2SO4 = (M + 16) + 980
= M + 996
C%muối = m chất tan muối/ m dd muối . 100%
15.17% = (M + 96) / (M + 996) * 100%
M = 64.95 g
M là Zn
Công thức oxit ZnO

a)Giả sử có 1 mol MO phản ứng
\(MO+2HCl\rightarrow MCl_2+H_2O\)
1----------->2----------->1----------->1
=> \(m_{ddHCl}=\dfrac{2.36,5}{10\%}=730\left(g\right)\)
\(m_{ddsaupu}=\left(M+16\right)+730=M+746\left(g\right)\)
=> \(C\%_{MCl_2}=\dfrac{M+71}{M+746}.100=12,34\)
=> M=24 (Mg)
b) Giả sử có 1 mol M2On phản ứng
\(M_2O_n+2nHCl\rightarrow2MCl_n+nH_2O\)
1---------------->2n-------------->2----------->n
=> \(m_{ddHCl}=\dfrac{2n.36,5}{10\%}=730n\left(g\right)\)
\(m_{ddsaupu}=\left(2M+16n\right)+730n=2M+746n\left(g\right)\)
=> \(C\%_{MCl_2}=\dfrac{2\left(M+35,5n\right)}{2M+746n}.100=12,34\)
Chạy nghiệm n=1,2,3
n=1 => M=12 (loại)
n=2 => M=24 (Mg)
n=3 => M=36 (loại)

CTHH cần tìm : $R_2O_3$
Coi $n_{H_2SO_4} = 3(mol)$
R2O3 + 3H2SO4 → R2(SO4)3 + 3H2O
1..............3..................1..................................(mol)
Ta có :
$m_{dd\ H_2SO_4} = \dfrac{3.98}{10\%} = 2940(gam)$
$m_{dd\ sau\ pư} = 2R + 16.3 + 2940 = 2R + 2988(gam)$
Suy ra :
$C\% = \dfrac{2R + 96.3}{2R + 2988}.100\% = 12,9\%$
$\Rightarrow R = 56(Fe)$
Vậy oxit là $Fe_2O_3$

nCO2 = 0,15 mol
MgCO3 + 2HCl ---> MgCl2 + CO2 + H2O
0.1 0,1 --> 0,1
RCO3 + 2HCl ---> RCl2 + CO2 + H2O
0,05 <---- (0,15-0,1)
Ta thấy: n HCl = 2n CO2 = 2.0,15 = 0,3 mol
m dd HCl = (0,3.36,5).100/7,3 = 150g
m CO2 = 0,15.44 = 6,6g
m dd sau phản ứng = m X + m dd HCl - m CO2 = 157,6 g
m MgCl2 = m dd sau phản ứng.C%/100 ~ 9,5g
n MgCl2 = 0,1 mol (thế vào pt trên)
Ta có: m RCO3 = m X - m MgCO3
=> 0,05(R + 60) = 14,2 - 0,1.84
=> R = 56
Vậy R là Fe
Chúc em học tốt!!

Chọn C
Gọi công thức của oxit hóa trị II là RO
Đặt mol RO = 1 (mol)
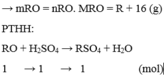
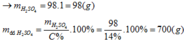
![]()
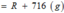
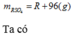

Vậy công thức của oxit kim loại là MgO

Gọi CT của oxit : RO
n RO = a ( mol )
PTHH:
RO + H2SO4 ====> RSO4 + H2O
a--------a------------------a
theo pthh:
n H2SO4 = n RSO4 = n RO = a ( mol )
Có: n H2SO4=a ( mol ) => m H2SO4 = 98a ( g )
=> m dd H2SO4 20% = 490a ( g )
BTKL: m dd sau phản ứng = a ( R + 16 ) + 490a = aR + 506a ( g )
Lại có :
n RSO4 = a ( mol ) => m RSO4 = aR + 96a
=> \(\dfrac{aR+96a}{aR+506a}=\dfrac{22,64}{100}\Rightarrow\dfrac{a\left(R+96\right)}{a\left(R+506\right)}=\dfrac{22,64}{100}\)
\(\Rightarrow R=24\left(Mg\right)\)
Vậy CT: MgO
Đặt kim loại là M, oxit là MO
Giả sử có 1 mol MO phản ứng, 1 mol H2SO4 phản ứng:
MO + H2SO4 -> MSO4 + H2O
C% = mct / mdd . 100%
10% = 1 . 98 / mdd . 100%
-> mDd H2SO4 = 980 g
Theo định luật bảo toàn khối lượng ta có:
Mdd = mMO + mddH2SO4 = (M + 16) + 980
= M + 996
C%muối = m chất tan muối/ m dd muối . 100%
15.17% = (M + 96) / (M + 996) * 100%
M = 64.95 g
M là Zn
Công thức oxit ZnO
lần tới kiếm hình LB gắn vào cho đẹp