Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bổ sung Câu 1 ( Linh làm chả liên quan đến đề hỏi )
\(n_{NaOH}=0,3\left(mol\right)\)
- TH1: Chỉ thu được NaHCO3
\(\Rightarrow n_{NaHCO3}=n_{NaOH}=0,3\left(mol\right)\)
\(\Rightarrow m_{NaHCO3}=0,3.84=25,2\left(g\right)\left(loai\right)\)
- TH2: Chỉ thu được Na2CO3.
\(n_{Na2CO3}=0,5n_{NaOH}=0,15\left(mol\right)\)
\(\Rightarrow m_{Na2CO3}=0,15.106=15,9\left(g\right)\left(loai\right)\)
- TH3: dư NaOH
\(2NaOH+CO_2\rightarrow Na_2CO_3+H_2O\)
Sau phản ứng tạo x mol Na2CO3. Dư 0,3-2x mol NaOH
\(\Rightarrow106x+40.\left(0,3-2x\right)=14,6\)
\(\Rightarrow x=0,1=n_{CO2}\left(TM\right)\)
\(n_{khi}=\frac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{H2}=0,3-0,1=0,2\left(mol\right)\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(MgCO_2+2HCl\rightarrow MgCl_2+CO_2+H_2O\)
\(n_{Mg}=0,2\left(mol\right);n_{MgCO3}=0,1\left(mol\right)\)
\(\Rightarrow m=0,2.24+84.0,1=13,2\left(g\right)\)
- TH4: tạo 2 muối NaHCO3 (a mol) và Na2CO3 (b mol)
\(\Rightarrow a+2b=0,3\left(1\right)\)
Mặt khác , \(84a+106b=14,6\left(2\right)\)
(1)(2) => nghiệm âm (loại)
1.Hỗn hợp khí thu được gồm H2 và CO2 có tổng mol = 6,72/22,4= 0,3 mol
----> nCO2 < 0,3 mol
hỗn hợp khí cho vào NaOH chỉ có CO2 phản ứng
nNaOH/nCO2 > 1 (vì nCO2 < 0,3) --> dung dịch B có 2 khả năng:
TH1: B gồm 2 muối NaHCO3 và Na2CO3 ; NaOH hết
Gọi nNa2CO3=x ; nNaHCO3 = 0,3-2x
-> m=106x + (0,3-2x).84= 14,6 --> x=0,171 ( loại vì nNa2CO3 = 0,171.2=0,342 > nNaOH)
TH2. B gồm Na2CO3 và NaOH dư
Gọi nCO2= x --> nNa2CO3=x -> nNaOH= 0,3-2x
m=106x + (0,3-2x).40 = 14,6
--> x= 0,1 mol ---> nCO2=0,1 mol ; nH2= 0,2 mol
2.
Ta có phương trình phản ứng:
Khi thêm Ba(OH)2 ta có phản ứng:
--> nMg= 0,2 ; nMgCO3 = 0,1
--> m=0,2.24 + 0,1.84= 13,2 g

Hỗn hợp khí thu được gồm H2 và CO2 có tổng mol = 6,72/22,4= 0,3 mol
----> nCO2 < 0,3 mol
hỗn hợp khí cho vào NaOH chỉ có CO2 phản ứng
nNaOH/nCO2 > 1 (vì nCO2 < 0,3) --> dung dịch B có 2 khả năng:
TH1: B gồm 2 muối NaHCO3 và Na2CO3 ; NaOH hết
Gọi nNa2CO3=x ; nNaHCO3 = 0,3-2x
-> m=106x + (0,3-2x).84= 14,6 --> x=0,171 ( loại vì nNa2CO3 = 0,171.2=0,342 > nNaOH)
TH2. B gồm Na2CO3 và NaOH dư
Gọi nCO2= x --> nNa2CO3=x -> nNaOH= 0,3-2x
m=106x + (0,3-2x).40 = 14,6
--> x= 0,1 mol ---> nCO2=0,1 mol ; nH2= 0,2 mol
--> nMg= 0,2 ; nMgCO3 = 0,1
--> m=0,2.24 + 0,1.84= 13,2 g
hh khí: CO2 + H2
n (hh khí) = 6,72 : 22,4 =0,3 =>nCO2 < 0,3
n(NaOH b.đ)= 300 x 0,001 x1 =0,3
Do n(NaOH b.đ) > nCO2 => s.p tạo thành sẽ là NaCO3 (NaOH có thể dư) theo cơ chế:
NaOH + CO2 ----> NaHCO3
sau đó:
NaHCO3 + NaOH ----> Na2CO3 + H2O
Đặt x = nNaOH(dư), y = nNa2CO3
{40x + 106y = 14,6 (khối lượng rắn)
{x + 2y = 0,3 (mol Na ko thay đổi)
=> x= 0,1, y=0,1
y=0,1 =>nC (trong Na2CO3)= 0,1 => nCO2 = 0,1
=>nCO2 =0,1; nH2 = 0,2
nCO2 = 0,1 => nMgCO3 = 0,1
nH2 = 0,2 => nMg =0,2

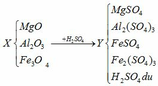
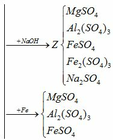
(a) Hòa tan MgO, Al2O3 và Fe3O4 vào H2SO4:
(1) MgO + H2SO4 → MgSO4 + H2O
(2) Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
(3) Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3 + 4H2O
Trung hòa Y:
(4) H2SO4 + 2NaOH → Na2SO4 + 2H2O
Cho dung dịch Y (MgSO4, Al2(SO4)3, FeSO4, Fe2(SO4)3, H2SO4) qua cột chứa bột sắt:
(5) H2SO4 + Fe → FeSO4 + H2
(6) Fe2(SO4)3 + Fe → 3FeSO4
(b) nH2SO4 = 0,45.1 = 0,45 mol
Gọi số mol của MgO, Al2O3 và Fe3O4 trong hỗn hợp ban đầu lần lượt là x, y, z (mol)
Ta có: 40x + 102y + 232z = 20,68 (*)
- Khi hòa tan hỗn hợp vào H2SO4:
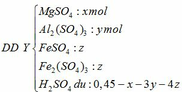
- Trung hòa ¼ dung dịch Y cần 0,025 mol NaOH vậy trung hòa Y cần 0,1 mol NaOH:
Theo PTHH (4): nH2SO4 dư = 0,5nNaOH = 0,05 mol
=> 0,45 – x – 3y – 4z = 0,05
=> x + 3y + 4z = 0,4 (**)
Dung dịch thu được chứa các chất:
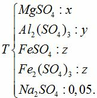
- Giả sử dẫn toàn bộ dung dịch Y qua cột chứa bột Fe:
(5) H2SO4 + Fe → FeSO4 + H2
0,05 → 0,05 (mol)
(6) Fe2(SO4)3 + Fe → 3FeSO4
z → 3z (mol)
Dung dịch sau chứa các chất tan:
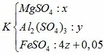
Theo đề bài ta có: mK – mT = 4.1,105
=> [120x + 342y + 152(4z + 0,05)] – [120x + 342y + 152.z + 400z + 0,05.142] = 4,42
=> z = 0,07 (***)
Từ (*) (**) (***) ta giải được z = 0,06; y = 0,02; z = 0,07
Số mol của nguyên tố O trong hỗn hợp X:
nO = nMgO + 3nAl2O3 + 4nFe3O4 = 0,06 + 3.0,02 + 4.0,07 = 0,4 mol
Khối lượng của O: mO = 0,4.16 = 6,4 (gam)
Phần trăm khối lượng của nguyên tố O:


nHCl = 0,4.0,5 = 0,2 mol; nH2SO4 = 0,08.0,5 = 0,04 mol
nH+ = nHCl + 2nH2SO4 = 0,28 mol
Đặt số mol của Zn và Mg trong hỗn hợp ban đầu là x và y (mol)
Ta có: 65x + 24y = 5,34 (1)
Zn + 2H+ → Zn2+ + H2
x → 2x → x (mol)
Mg + 2H+ → Mg2+ + H2
y → 2y → y (mol)
Dung dịch Y gồm có:
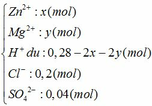
Ta thấy: nH+ + 2nZn2+ + 2nMg2+ (= 0,28 mol) < nNaOH (= 0,3 mol)
=> NaOH dư, Zn(OH)2 bị tan một phần
=> nNaOH hòa tan kết tủa = 0,3 – 0,28 = 0,02 mol
H+ + OH- → H2O
0,28-2x-2y → 0,28-2x-2y (mol)
Zn2+ + 2OH- → Zn(OH)2
x → 2x → x (mol)
Mg2+ + 2OH- → Mg(OH)2
y → 2y → y (mol)
Zn(OH)2 + 2OH- → ZnO22- + H2O
0,01 ← 0,02 (mol)
Khối lượng kết tủa thu được sau phản ứng: m kết tủa = mMg(OH)2 + mZn(OH)2
=> 99(x-0,01) + 58y = 8,43 <=> 99x + 58y = 9,42 (2)
Từ (1) và (2) ta có:

Ta có: nKOH : nBa(OH)2 = 0,4:0,05 = 8
Giả sử số mol của KOH và Ba(OH)2 lần lượt là 8a và a (mol)
=> nBa2+ = a (mol); nOH- = nKOH + 2nBa(OH)2 = 10a (mol)
- Khi kết tủa Mg(OH)2 và Zn(OH)2 đạt giá trị lớn nhất: nOH- = nH+ dư + 2nZn2+ + 2nMg2+
=> 10a = 0,04 + 2.0,06 + 2.0,06 => a = 0,028 mol
Ta thấy a < nSO42- => BaSO4 chưa đạt cực đại
- Giả sử sau khi Mg(OH)2 và Zn(OH)2 đạt cực đại ta thêm 8b mol KOH và b mol Ba(OH)2:
+ Lượng kết tủa sinh thêm là lượng BaSO4: nBaSO4 = nBa(OH)2 = b mol
=> mBaSO4 = 233b (gam)
+ Lượng kết tủa bị tan ra: nZn(OH)2 = nOH-: 2 = 10b : 2 = 5b (mol)
=> mZn(OH)2 = 99.5b = 495b (gam)
Ta thấy khối lượng kết tủa sinh ra nhỏ hơn khối lượng kết tủa bị tan nên khối lượng kết tủa lớn nhất là thời điểm Mg(OH)2 và Zn(OH)2 đạt cực đại. Khi đó: nBa(OH)2 = a = 0,028 mol
=> V = 0,028 : 0,05 = 0,56 (lít)
Kết tủa sau phản ứng gồm có:
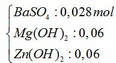
Mg(OH)2 → t ∘ MgO + H2O
0,06 mol → 0,06 mol
Zn(OH)2 → t ∘ ZnO + H2O
0,06 mol → 0,06 mol
=> m = mBaSO4 + mMgO + mZnO = 0,028.233 + 0,06.40 + 0,06.81 = 13,784 gam

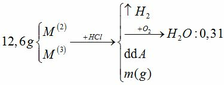
Đồng nhất dữ kiện để thuận lợi cho tính toán, bằng cách nhân đôi khối lượng H2O.
a.
BTNT H: nH2 = nH2O = 0,31 mol
=> nHCl = 0,62mol
BTKL: m kim loại + mHCl = mA + mB => 12,6 + 36,5 . 0,62 = m + 2 . 0,31 => m = 34,61g
b.
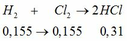
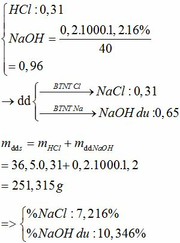

a/ PTHH: Mg + 2HCl ===> MgCl2 + H2
x 2x x x
Fe + 2HCl ===> FeCl2 + H2
y 2y y y
Gọi số mol Mg, Fe lần lượt là x, y
Lập các số mol theo phương trình
nH2 = 8,96 / 22,4 = 0,4 mol
Theo đề ra, ta có hệ phương trình:
\(\begin{cases}24x+56y=12,8\\x+y=0,4\end{cases}\)=>\(\begin{cases}x=0,3\\y=0,1\end{cases}\)
=> mMg = 0,3 x 24 = 7,2 gam
mFe = 0,1 x 56 = 5,6 gam
b/ \(\sum nHCl\) = 0,8 mol
=> VHCl = 0,8 / 2 = 0,4 lít = 400ml
c/ PTHH: MgCl2 + 2NaOH ===> Mg(OH)2 + 2NaCl
0,3 0,6 0,3
FeCl2 + 2NaOH ===> Fe(OH)2 + 2NaCl
0,1 0,2 0,1
=> \(\sum m\downarrow\) = 0,3 x ( 24 + 16 x 2 + 2) + 0,1 x ( 56 + 16 x 2 + 2) = 26,4 gam

Hỗn hợp khí thu được gồm H2 và CO2 có tổng mol = 6,72/22,4= 0,3 mol
----> nCO2 < 0,3 mol
hỗn hợp khí cho vào NaOH chỉ có CO2 phản ứng
nNaOH/nCO2 > 1 (vì nCO2 < 0,3) --> dung dịch B có 2 khả năng:
TH1: B gồm 2 muối NaHCO3 và Na2CO3 ; NaOH hết
Gọi nNa2CO3=x ; nNaHCO3 = 0,3-2x
-> m=106x + (0,3-2x).84= 14,6 --> x=0,171 ( loại vì nNa2CO3 = 0,171.2=0,342 > nNaOH)
TH2. B gồm Na2CO3 và NaOH dư
Gọi nCO2= x --> nNa2CO3=x -> nNaOH= 0,3-2x
m=106x + (0,3-2x).40 = 14,6
--> x= 0,1 mol ---> nCO2=0,1 mol ; nH2= 0,2 mol
--> nMg= 0,2 ; nMgCO3 = 0,1
--> m=0,2.24 + 0,1.84= 13,2 g