Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Cho Al và Ag phản ứng với H 2 S O 4 loãng, dư chỉ có Al phản ứng.
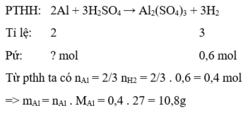
% m A l = 10,8 12 .100 % = 90 % .
% m A g = 100 % - 90 % = 10 %

Đặt số mol Al, Fe, Mg trong 15,8 g hh là x, y, z
pt khối lượng: 27x + 56y+ 24z = 15,8
pt bảo toàn electron: 3x+ 2y+ 2z = 2*nH2
Đặt số mol Al, Fe, Mg trong 0,15 mol lúc sau là kx, ky, kz
(tỉ lệ số mol giữa các chất không đổi)
pt số mol: k(x + y + z) = 0,15 (1)
pt bảo toàn e: k(3x + 3x + 2y) = 3nNO (2)
lấy (1) chia (2) được pt thứ 3, giải 3 pt 3 ẩn là xong :D

Các quá trình khử :
N{+5} + 3e = N{+2} ; N{+5} + e = N{+4} ; 2N{+5} + 8e = 2N{+1} ; S{+6} + 2e = S{+4}
Ʃne (HNO3 nhận) = 3.nNO + nNO2 + 8.nN2O + 2.nSO2 = 1,4 mol
Các quá trình oxy hóa :
Mg - 2e = Mg{+2} ; Al - 3e = Al{+3}
Áp dụng định luật bảo toàn electron, ta có :
2.nMg + 3.nAl = 1,4
Mặt khác, 24.nMg + 27.nAl = 15
=> nMg = 0,4 mol và nAl = 0,2 mol
=> %mMg = 64% và %mAl = 36%

PTHH: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
Ta có: \(n_{H_2}=\frac{13,44}{22,4}=0,6\left(mol\right)\)
\(\Rightarrow n_{Al}=0,4mol\) \(\Rightarrow m_{Al}=0,4\cdot27=10,8\left(g\right)\)
\(\Rightarrow\%m_{Al}=\frac{10,8}{12}\cdot100=90\%\)
\(\Rightarrow\%m_{Ag}=10\%\)

\(Cu+H_2SO_4\rightarrow không.pư\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
a. Sau phản ứng chất rắn không tan là Cu=6,4g
\(n_{Cu}\)=\(\frac{6,4}{64}=0,1\)
\(n_{H_2}=\frac{6,72}{22,4}=0,3mol\)
\(n_{Al}=\frac{2}{3}n_{H_2}=0,2mol\Rightarrow m_{Al}=0,2.27=5,4g\)
b. \(Cu+2H_2SO_4\rightarrow CuSO_4+SO_2+2H_2O\) (1)
\(2Al+6H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3SO_2+6H_2O\) (2)
\(n_{SO_2}\left(1\right)=n_{Cu}=0,1mol\)
\(n_{SO_2}\left(2\right)=\frac{3}{2}n_{Al}\)=0,3mol
\(\Rightarrow n_{SO2}=\)0,4mol
\(V_{SO_2}\left(đktc\right)=0,4.22,4=8,96l\)

2Al + 3S —> Al2S3
Chất rắn X gồm Al2S3, Al dư và S dư. Khí gồm H2S và H2. Chất rắn không tan là S dư.
+)Khí với Pb(NO3)2:
H2S + Pb(NO3)2 —> PbS + 2HNO3
0,03………………..……….0,03
n khí = 0,06 —> nH2 = 0,06 – 0,03 = 0,03 (mol)
+) Chất rắn X với HCl dư:
Al2S3 + 6HCl —> 2AlCl3 + 3H2S
0,01…………….....................0,03
2Al + 6HCl —> 2AlCl3 + 3H2
0,02………………………….0,03
+) Nung Al với S:
2Al + 3S —> Al2S3
0,02…0,03…..0,01
mAl = (0,02 + 0,02).27 = 1,08 g
mS = 0,03.32 + 0,04 = 1 g
\(n_{H_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
PTHH: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
_____0,4<-----------------------------------0,6
=> \(\%Al=\dfrac{0,4.27}{12}.100\%=90\%\)
%Ag = 100% - 90% = 10%