Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, Ta có: 27nAl + 56nFe = 22 (1)
PT: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}+n_{Fe}=\dfrac{19,832}{24,79}=0,8\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}m_{Al}=0,4\left(mol\right)\\n_{Fe}=0,2\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,4.27}{22}.100\%\approx49,09\%\\\%m_{Fe}\approx50,91\%\end{matrix}\right.\)
b, \(n_{HCl}=2n_{H_2}=1,6\left(mol\right)\)
\(\Rightarrow C_{M_{HCl}}=\dfrac{1,6}{0,5}=3,2\left(M\right)\)

a)
Gọi $n_{Fe} = a(mol) ; n_{Al} =b (mol) \Rightarrow 56a + 27b = 11(1)$
$Fe + 2HCl \to FeCl_2 + H_2$
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
Theo PTHH : $n_{H_2} = a + 1,5b = \dfrac{8,96}{22,4} = 0,4(2)$
Từ (1)(2) suy ra : a = 0,1 ; b = 0,2
$\%m_{Fe} = \dfrac{0,1.56}{11}.100\% = 50,9\%$
$\%m_{Al} = 100\% - 50,9\% = 49,1\%$
b) $n_{HCl} = 2n_{H_2} = 0,8(mol)$
$\Rightarrow C_{M_{HCl}} = \dfrac{0,8}{0,4} = 2M$
c)
$C_{M_{FeCl_2}} = \dfrac{0,1}{0,4} = 0,25M$
$C_{M_{AlCl_3}} =\dfrac{0,2}{0,4} = 0,5M$

a) PTHH: 2Al + 3H2SO4 → Al2(SO4)3 + 3H2↑
2 mol : 3 mol : 1 mol : 3 mol
0,1 mol <-- 0,15 mol <--- 0,15 mol
số mol của H2 là: 3,36 / 22,4 = 0,15 mol
khối lượng Al là: 0,1 * 27 = 2,7 g
ta có: 8 g chất rắn không tan sau phản ứng là: Cu
vậy khối lượng hỗn hợp a là: mAl + mCu = 2,7 + 8 = 10,7 g
b) khối lượng chất tan của H2SO4 là: mchất tan= 0,15 * 98 = 14,7 g
ta có: C% H2SO4= (mchất tan/ m dung dịch) * 100
→ m dung dịch H2SO4 = ( m chất tan * 100) / C% = ( 14,7 * 100) / 20= 73,5 g

$n_{H_2}=\dfrac{7,437}{24,79}=0,3(mol)$
$a)PTHH:2Al+6HCl\to 2AlCl_3+3H_2$
$\Rightarrow n_{Al}=\dfrac{2}{3}n_{H_2}=0,2(mol)$
$\Rightarrow \%m_{Al}=\dfrac{0,2.27}{24,6}.100\%=21,95\%$
$\Rightarrow \%m_{Cu}=100-21,95=78,05\%$
$b)n_{AlCl_3}=n_{Al}=0,2(mol)$
$\Rightarrow m_{AlCl_3}=0,2.133,5=26,7(g)$
$c)n_{HCl}=3n_{Al}=0,6(mol)$
$\Rightarrow C_{M_{HCl}}=\dfrac{0,6}{0,3}=2M$

a) \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Cu+HCl\rightarrow\)(không phản ứng)
2Al + 6HCl => 2AlCl3 + 3H2
0,3/3*2 (6,72/22,4)
=> mAl = 0,2 *27 =5,4g; mCu = 11,8 - 5,4 = 6,4g

a. PTHH:
Cu + HCl ---x--->
Fe + 2HCl ---> FeCl2 + H2
Vậy chất rắn A là Cu.
b. Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Theo PT: \(n_{Fe}=n_{H_2}=0,3\left(mol\right)\)
=> \(m_{Fe}=0,3.56=16,8\left(g\right)\)
=> \(\%_{m_{Fe}}=\dfrac{16,8}{30}.100\%=56\%\)
\(\%_{m_{Cu}}=100\%-56\%=44\%\%\)
c.
Theo PT: \(n_{FeCl_2}=n_{Fe}=0,3\left(mol\right)\)
=> \(m_{FeCl_2}=0,3.127=38,1\left(g\right)\)
d.
Ta có: \(m_{dd_{FeCl_2}}=100+16,8=116,8\left(g\right)\)
=> \(C_{\%_{FeCl_2}}=\dfrac{38,1}{116,8}.100\%=32,62\%\)
ta có Cu ko phản ứng với HCl
-> V khí là do Fe phản ứng hết tạo ra
Fe + 2HCl -> FeCl2 + H2
0,3 .............................0,3
n H2 = 6,72 : 22,4=0,3 mol
m Fe = 0,3.56 =16,8 g
% Fe = 16,8 : 30 .100 = 56 %
% Cu = 100% - 56% = 44%

2Al + 6HCl → 2 A l C l 3 + 3 H 2
a……….3/2.a (mol)
Mg + 2HCl → M g C l 2 + H 2
b....................b (mol)
4 gam rắn không tan là Cu, gọi số mol của Al và Mg lần lượt là a và b (mol). Ta có:
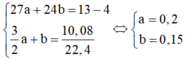
⇒ % m C u = 4 13 .100 = 30,77 % ⇒ % m A l = 0,2.27 13 .100 = 41,54 % ⇒ % m M g = 100 % − 30,77 % − 41,54 % = 27,69 %
⇒ Chọn C.
\(a,n_{H_2}=\dfrac{6,72}{22,4}=0,3(mol)\\ 2Al+6HCl\to 2AlCl_3+3H_2\\ \Rightarrow n_{Al}=0,2(mol)\\ \Rightarrow m_{Al}=0,2.27=5,4(g)\\ b,m_{hh}=5,4+12,8=18,2(g)\\ c,n_{HCl}=0,6(mol)\\ \Rightarrow C_{M_{HCl}}=\dfrac{0,6}{0,3}=2M\)
a) \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
_____0,2<----0,6<---------------0,3
=> mAl = 0,2.27 = 5,4(g)
b) mhh = 5,4 + 12,8 = 18,2(g)
c) \(C_{M\left(HCl\right)}=\dfrac{0,6}{0,3}=2M\)