
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

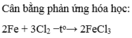

\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\\ 5O_2+4P\underrightarrow{t^o}2P_2O_5\\ P_2O_5+3H_2O\rightarrow2H_3PO_4\\ 3Zn+2H_3PO_4\rightarrow Zn_3\left(PO_4\right)_2+3H_2\\ 2H_2+O_2\underrightarrow{t^o}2H_2O\\ CaCO_3\underrightarrow{t^o}CO_2+CO_2\\ CaO+H_2O\rightarrow Ca\left(OH\right)_2\)

Câu 3: (2.0) Hoàn thành và phân loại các phương trình hóa học sau, ghi rõ điều
kiện phản ứng (nếu có).
a. 2C4H10 +13 O2 → 8CO2 + 10H2O
b. 2KMNO4 → K2MnO4 + MnO2 + O2
c. C3HS + O2 → ?
d. 2KCIO3 → 2KCl + 3O2
e. 2Mg + O2 → 2MgO
f. 4Al + 3O2 → 2Al2O3
g. 3Fe + 2O2 → Fe3O4
h. 4P +5O2 →2P2O5
i. C+O2→ CO2
j. 2Zn + O2→2 Zno
check lại phẩn c hộ mk

\(N_2O_5+H_2O\rightarrow2HNO_3\left(P.Ứ.hoá.hợp\right)\\ 2K+2H_2O\rightarrow2KOH+H_2\left(P.Ứ.thế\right)\\ CaO+H_2O\rightarrow Ca\left(OH\right)_2\left(P.Ứ.hoá.hợp\right)\\ SO_3+H_2O\rightarrow H_2SO_4\left(P.Ứ.hoá.hợp\right)\\ K_2O+H_2O\rightarrow2KOH\left(p.ứ.Hoá.hợp\right)\\ Ca+2H_2O\rightarrow Ca\left(OH\right)_2+H_2\left(P.Ứ.thế\right)\\ P_2O_5+3H_2O\rightarrow2H_3PO_4\left(P.ứ.hoá.hợp\right)\)

\(4P+5O_2\rightarrow\left(t^o\right)2P_2O_5\) - phản ứng hóa hợp
\(2Mg+O_2\rightarrow\left(t^o\right)2MgO\) - phản ứng hóa hợp
\(4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\) - phản ứng hóa hợp
\(4Na+O_2\rightarrow\left(t^o\right)2Na_2O\) - phản ứng hóa hợp
\(H_2+CuO\rightarrow\left(t^o\right)Cu+H_2O\) - phản ứng oxi hóa- khử, phản ứng thế
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\) - phản ứng phân hủy
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\) - phản ứng hóa hợp
\(2H_2+O_2\rightarrow\left(t^o\right)2H_2O\) - phản ứng hóa hợp
\(Zn+2HCl\rightarrow ZnCl_2+H_2\) - phản ứng thế
\(2O_2+CH_4\rightarrow\left(t^o\right)CO_2+2H_2O\) - phản ứng oxi hóa, khử
\(4P+5O_2\rightarrow\left(t^o\right)2P_2O_5\) - phản ứng hóa hợp
\(2KClO_3\rightarrow\left(t^o,MnO_2\right)2KCl+3O_2\) - phản ứng phân hủy
a. 4P + 5O2 -> 2P2O5 ( Phản ứng hóa hợp )
b. 2Mg + O2 -> 2MgO ( Phản ứng hóa hợp )
c. 4Al + 3O2 -> 2Al2O3 ( Phản ứng hóa hợp )
d. 4Na + O2 -> 2Na2O ( Phản ứng hóa hợp )
e. H2 + CuO -> Cu + H2O ( Phản ứng thế )
. 2KMnO4 -> K2MnO4 + MnO2 + O2 ( Phản ứng phân hủy )
f. 4Fe + 3O2 -> 2Fe2O3 ( Phản ứng hóa hợp )
g. 2H2 + O2 -> 2H2O ( Phản ứng hóa hợp )
h Zn + 2HCl -> ZnCl2 + H2 ( Phản ứng thế )
i. 2O2 + CH4 -> CO2 + 2H2O ( Phản ứng thế )
j. Nãy làm rồi
k. 2KClO3 -> 2KCl + 3O2 ( Phản ứng phân hủy )

a) $4P + 5O_2 \xrightarrow{t^o} 2P_2O_5$
b) $Mg + Cl_2 \xrightarrow{t^o} MgCl_2$
c) $2Na + 2H_2O \to 2NaOH + H_2$
d) $C + O_2 \xrightarrow{t^o} CO_2$
e) $C_xH_y + (x + \dfrac{y}{4})O_2 \xrightarrow{t^o} xCO_2 + \dfrac{y}{2}H_2O$
f) $2Al + Fe_2O_3 \xrightarrow{t^o} Al_2O_3 + 2Fe$
g) $2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2$
i) $Fe_xO_y + yCO \xrightarrow{t^o} xFe + yCO_2$
k) $Fe_2O_3 + 6HCl \to 2FeCl_3 +3 H_2O$
l) $3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4$

\(2KMnO_4\underrightarrow{^{t^0}}K_2MnO_4+MnO_2+O_2\left(PH\right)\)
\(3Fe+2O_2\underrightarrow{^{t^0}}Fe_3O_4\left(HH\right)\)
\(4P+5O_2\underrightarrow{^{t^0}}2P_2O_5\left(HH\right)\)
\(2HgO\underrightarrow{^{t^0}}2Hg+O_2\left(PH\right)\)
\(2KClO_3\underrightarrow{^{t^0}}2KCl+3O_2\left(PH\right)\)
\(2Mg+O_2\underrightarrow{^{t^0}}2MgO\left(HH\right)\)
\(2Fe\left(OH\right)_3\underrightarrow{^{t^0}}Fe_2O_3+3H_2O\left(PH\right)\)
\(N_2+\dfrac{5}{2}O_2\underrightarrow{^{t^0}}N_2O_5\left(HH\right)\)

\(2KClO_3\rightarrow3O_2+2KCl\)
\(5O_2+4P\rightarrow2P_2O_5\)
\(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
\(3Zn+2H_3PO_4\rightarrow Zn_3\left(PO_4\right)_2+3H_2\)
\(2H_2+O_2\rightarrow2H_2O\)
\(CaCO_3\rightarrow CO_2+CaO\)
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
lần sau đừng lấy C, K vì dễ lẫn vs cữ viết tắt của cacbon và kali

\(a) 4K + O_2 \xrightarrow{t^o} 2K_2O\\ K_2O + H_2O \to 2KOH\\ 4P + 5O_2 \xrightarrow{t^o} 2P_2O_5\\ P_2O_5 + 3H_2O \to 2H_2PO_4\\ c) 2H_2 + O_2 \xrightarrow{t^o} 2H_2O\\ Na_2O + H_2O \to 2NaOH\\ d) 2Ca + O_2 \xrightarrow{t^o} 2CaO\\ CaO + H_2O \to Ca(OH)_2\\ e) 2Cu + O_2 \xrightarrow{t^o} 2CuO\\ CuO+ 2HCl\to CuCl_2 + H_2O\\ \)
\(b) S + O_2 \xrightarrow{t^o} SO_2 \\2SO_2 + O_2 \xrightarrow{t^o,V_2O_5} 2SO_3\\ SO_3 + H_2O \to H_2SO_4\)

Câu 1 :
b)
Cho quỳ tím ẩm vào mẫu thử
- mẫu thử hóa đỏ là P2O5
P2O5 + 3H2O $\to$ 2H3PO4
- mẫu thử hóa xanh là Na2O,CaO
Na2O + H2O $\to $ 2NaOH
CaO + H2O $\to$ Ca(OH)2
- mẫu thử không đổi màu là NaCl
Cho hai mẫu thử còn vào dung dịch H2SO4
- mẫu thử tạo kết tủa trắng là CaO
CaO + H2SO4 $\to$ CaSO4 + H2O
- mẫu thử không hiện tượng là Na2O
Câu 2 :
1)
\(S_{Na_2SO_4} = \dfrac{m_{Na_2SO_4}}{m_{H_2O}}.100 = \dfrac{7,2}{80}.100\% = 9(gam)\\ C\%_{Na_2SO_4} = \dfrac{S}{S + 100}.100\% = \dfrac{9}{100 + 9}.100\% = 8,26\%\)