Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1/
a)
\(n_{Ba}=\frac{27,4}{137}=0,2mol\); \(n_{H_2SO_4}=\frac{9,8}{98}=0,1mol\)
PTHH: \(Ba+H_2SO_4\rightarrow BaSO_4\downarrow+H_2\uparrow\)
Trước pư: \(0,2\) \(0,1\) \(\left(mol\right)\)
Pư: \(0,1\) \(0,1\) \(0,1\) \(0,1\) \(\left(mol\right)\)
Sau pư: \(0,1\) \(0\) \(0,1\) \(0,1\) \(\left(mol\right)\)
Sau pư còn dư 0,1mol Ba nên Ba tiếp tục pư với H2O trong dd:
\(Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\uparrow\)
\(0,1\) \(0,1\) \(0,1\) \(\left(mol\right)\)
Tổng số mol H2 sau 2 pư : \(n_{H_2}=0,1+0,1=0,2mol\)
Thể tích khí thu được: \(V_{H_2}=0,2.22,4=4,48l\)
b)
Dd thu được sau pư là dd \(Ba\left(OH\right)_2\)
\(m_{Ba\left(OH\right)_2}=0,1.171=17,1g\)
\(m_{dd}=27,4+100-m_{BaSO_4}-m_{H_2}\)\(=27,4+100-0,1.233-0,2.2=103,7g\)
\(C\%_{ddBa\left(OH\right)_2}=\frac{17,1}{103,7}.100\%\approx16,49\%\)
2/
\(n_{H_2S}=\frac{0,672}{22,4}=0,03mol\)
\(CaS+2HBr\rightarrow CaBr_2+H_2S\uparrow\)
Theo pt:
\(n_{CaS}=n_{CaBr_2}=n_{H_2S}=0,03mol\) ; \(n_{HBr}=0,06mol;\)\(m_{HBr}=0,06.81=4,86g\)
\(m=m_{CaS}=0,03.72=2,16g;\)\(m_{CaBr_2}=0,03.200=6g\)
\(\Rightarrow m_1=\frac{4,86.100}{9,72}=50g\)
Áp dụng ĐLBTKL:
\(m_2=m_{ddCaBr_2}=50+2,16-34.0,03=51,14g\)
\(x=C\%_{CaBr_2}=\frac{6.100}{51,14}\approx11,73\%\)

bài 1: nZn= 0,5 mol
Zn + 2HCl → ZnCl2 + H2↑
0,5 mol 1 mol 0,5 mol 0,5 mol
a) mHCl= 36,5 (g) → mdung dịch HCl 10% = 36,5 / 10%= 365 (g)
b) mZnCl2= 0,5x 136= 68 (g)
c) mdung dịch= mZn + mdung dịch HCl 10% - mH2= 32,5 + 365 - 0,5x2 = 396,5 (g)
→ C%ZnCl2= 68/396,5 x100%= 17,15%
Bài 2: Cách phân biệt:
Dùng quỳ tím:→ lọ nào làm quỳ chuyển thành màu đỏ: HCl và H2SO4 (cặp I)
→ quỳ không đổi màu: BaCl2 và NaCl ( cặp II)
→ quỳ chuyển màu xanh: NaOH và Ba(OH)2 ( cặp III)
Đối với cặp I: ta cho dung dịch BaCl2 vào, ống có kết tủa trắng chính là ống đựng H2SO4, ống còn lại chứa dung dịch HCl
Đối với cặp II: ta cho dung dịch H2SO4 vào, ống có kết tủa trắng chính là ống đựng BaCl2, ống còn lại là NaCl
Đối với cặp III: ta cho dung dịch H2SO4 vào, ống có kết tủa trắng chính là ống đựng Ba(OH)2, ống còn lại là NaOH
PTPU: BaCl2 + H2SO4→ BaSO4↓ + 2HCl
Ba(OH)2 + H2SO4→ BaSO4↓ + 2H2O

2 mct trong dd ban đầu = 700*12/100 = 84(g)
mct trong dd bão hoà = 84-5 = 79(g)
mdd bão hoà = 700-300-5 = 395 (g)
=> C% = 79*100/395 = 20%

Ca(OH)2 + CO2 -> CaCO3 + H2O (1)
nCO2=0,3(mol)
Từ 1:
nCa(OH)2=nCaCO3=nCO2=0,3(mol)
mCaCO3=100.0,3=30(g)
CM dd ca(OH)2=\(\dfrac{0,3}{0,2}=1,5M\)

a) PTHH: CaO + H2O ===> Ca(OH)2
b) nCaO = 2,8 / 56 = 0,05 (mol)
=> nCa(OH)2 = nCaO = 0,05 (mol)
=> mCa(OH)2 = 0,05 x 74 = 3,7 (gam)
a) Ta có:
nCaO= \(\frac{m_{CaO}}{M_{CaO}}=\frac{2,8}{56}=0,05\left(mol\right)\)
PTHH: CaO + H2O -> Ca(OH)2
b) Theo PTHH và đề bài, ta có:
\(n_{Ca\left(OH\right)_2}=n_{CaO}=0,05\left(mol\right)\)
Khối lượng Ca(OH)2 thu được:
\(m_{Ca\left(OH\right)_2}=n_{Ca\left(OH\right)_2}.M_{Ca\left(OH\right)_2}=0,05.74=3,7\left(g\right)\)

a/ Fe + H2SO4 ---------> FeSO4 + H2
b/ \(n_{Fe}=\frac{11,2}{56}=0,2\left(mol\right)\)
Theo PTHH thì : \(n_{FeSO_4}=n_{Fe}=0,2\left(mol\right)\)
\(\Rightarrow m_{FeSO_4}=0,2.152=30,4\left(g\right)\)
c/ Theo PTHH thì \(n_{H_2SO_4}=n_{Fe}=0,2\left(mol\right)\)
\(\Rightarrow C_{M_{H_2SO_4}}=\frac{0,2}{0,5}=0,4\left(mol\text{/}l\right)\)



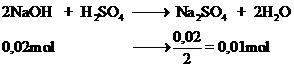


Số mol
Phương trình :

Số mol Ca(OH)2 tạo thành
Thể tích dd :
Nồng độ dd Ca(OH)2