Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Pt: 2Pb(NO3)2 --to--> 2PbO + 4NO2 + 4O2
...........x..........................x
nPb(NO3)2 ban đầu = 66,2\331=0,2 mol
Nếu Pb(NO3)2 bị nhiệt phân hết => nPb = 0,2 mol
=> mPbO = 0,2 . 223 = 44,6g < 55,4g
Vậy Pb(NO3)2 ko bị nhiệt phân hết
Gọi x là số mol Pb(NO3)2 pứ
Ta có: mPb(NO3)2 dư + mPbO = 55,4
<=> (0,2 - x).331 + 223x = 55,4
=> x = 0,1
Hiệu suất pứ:
H = 0,1\0,2.100\%=50%
bài 2
pt: 2KMnO4---t*-->K2MnO4+MnO2+O2
Áp dụng định luật bảo toàn khối lượng:
mO2=mKMnO4-mhhX=79-72,6=6,4(g)
=>nO2=6,4/32=0,2(mol)
Theo pt: nKMnO4=2nO2=2.0,2=0,4(mol)
=>mKMnO4=0,4.158=63,2(g)
=>mKMnO4 dư=79-63,2=15,8(g)
Theo pt: nK2MnO4=nO2=0,2(mol)
=>mK2MnO4=0,2.197=39,4(g)
=>%K2MnO4=39,4/72,6.100~54,27%
Theo pt: nMnO2=nO2=0,2(mol)
=>mMnO2=0,2.87=17,4(g)
=>%mMnO2=17,4/72,6.100~23,97%
=>%KMnO4 dư=100%-23,97%-54,27%=21,76%
b) H%=63,2/79.100=80%
Bài 1
\(2Pb\left(NO3\right)2-->2PbO+4NO2+4O2\)
\(n_{Pb\left(NO3\right)2}=\frac{66,2}{331}=0,2\left(mol\right)\)
\(n_{PbO}=n_{Pb\left(NO3\right)2}=0,2\left(mol\right)\)
\(m_{PBO}=0,2.223=44,6\left(g\right)\)
\(H\%=\frac{44,6}{55,4}=80,5\%\)
Bài 2 : tham khảo nha


a) PTHH: 2KMnO4 \(\underrightarrow{t^o}\) K2MnO4 + MnO2 + O2
Áp dụng ĐLBT khối lượng: Khối lượng chất rắn giảm sau phản ứng chính là khối lượng khí O2 tạo thành.
Khối lượng O2 thu được là: 79 - 72,6 = 6,4 g
Số mol khí O2 là: 6,4 : 32 = 0,2 mol
Theo PTHH, số mol KMnO4 bị nhiệt phân là: 2.0,2= 0,4 mol
Khối lượng KMnO4 bị nhiệt phân là: 0,4.158 = 63,2 g < 79 g
Chứng tỏ KMnO4 bị nhiệt phân không hoàn toàn
Khối lượng KMnO4 dư là: 79 - 63,2 = 15,8 g
Số mol KMnO4 thu được là: 0,2 mol
Khối lượng KMnO4 thu được là: 0,2.197 = 39,4 g
Trong hỗn hợp X gồm KMnO4 dư, MnO2 , K2MnO4
Vậy thành phần % khối lượng các chất trong hỗn hợp X là:
% KMnO4 = \(\dfrac{15,8.100\%}{72,6}\)= 21,76%
% K2MnO4 = \(\dfrac{39,4.100\%}{72,6}\)= 54,27 %
% MnO2 = 100% - 21,76% - 54,27 % = 23,97%
b)
Hiệu suất phản ứng nhiệt phân KMnO4 là:
H% =\(\dfrac{63,2.100\%}{79}\)= 80%
pt: 2KMnO4---t*-->K2MnO4+MnO2+O2
Áp dụng định luật bảo toàn khối lượng:
mO2=mKMnO4-mhhX=79-72,6=6,4(g)
=>nO2=6,4/32=0,2(mol)
Theo pt: nKMnO4=2nO2=2.0,2=0,4(mol)
=>mKMnO4=0,4.158=63,2(g)
=>mKMnO4 dư=79-63,2=15,8(g)
Theo pt: nK2MnO4=nO2=0,2(mol)
=>mK2MnO4=0,2.197=39,4(g)
=>%K2MnO4=39,4/72,6.100~54,27%
Theo pt: nMnO2=nO2=0,2(mol)
=>mMnO2=0,2.87=17,4(g)
=>%mMnO2=17,4/72,6.100~23,97%
=>%KMnO4 dư=100%-23,97%-54,27%=21,76%
b) H%=63,2/79.100=80%

Gọi số mol KMnO4 là a; KClO3 là b
-> m hỗn hợp ban đầu=158a + 122,5b
Nung hỗn hợp
2KMnO4 -to> K2MnO4 + MnO2 + O2
2KClO3 -to> 2KCl + 3O2
-> nK2MnO4=nMnO2=1/2nKMnO4=0,5a
-> nKCl=nKClO3=b
-> m rắn=mK2MnO4 +mMnO2 +mKCl=197.0,5a +87.0,5a+74,5b=142a+74,5b
-> 142a+74,5b=75%(158a+122,5b)=118,5a+91,875b
->23,5a=17,375b
-> a=0,74b
-> %mKMnO4=158a/(158a+122,5b) =48,8% -> %mKClO3=51,2%

2K2MnO4-toK2MnO4+MnO2+O2
nKMnO4=15,8/158=0,1 mol
->nK2MnO4=nMnO2=0,05 mol
mcr=0,05.197+0,05.87=14,2g
H,=14,2/14,5=97,7%
\(n_{KMnO_4}=\dfrac{15,8}{158}=0,1mol\)
Gọi \(n_{KMnO_4}=x\)
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
x 1/2 x 1/2 x ( mol )
Ta có:
\(158\left(0,1-x\right)+\dfrac{1}{2}x\left(197+87\right)=14,52\)
\(\Leftrightarrow x=0,08mol\)
\(H=\dfrac{0,08}{0,1}.100=80\%\)

Gọi số mol lần lượt là a,b (mol)
Khối lượng giảm = khối lượng O2 thoát ra
\(n_{O2}=\frac{5,76}{32}=0,18\left(mol\right)\)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
_______ a ----------------------------------------> 0,5a (mol)
2KClO3 --to--> 2KCl + 3O2
b -------------------------> 1,5b (mol)
=> \(\left\{{}\begin{matrix}158a+122,5b=28,76\\0,5a+1,5b=0,18\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}a=0,12\left(mol\right)\\b=0,08\left(mol\right)\end{matrix}\right.\)
%m KMnO4 = \(\frac{0,12.158}{28,76}.100\%=65,92\%\)
%m KClO3 = \(\frac{0,08.122,5}{28,76}.100\%=34,08\%\)
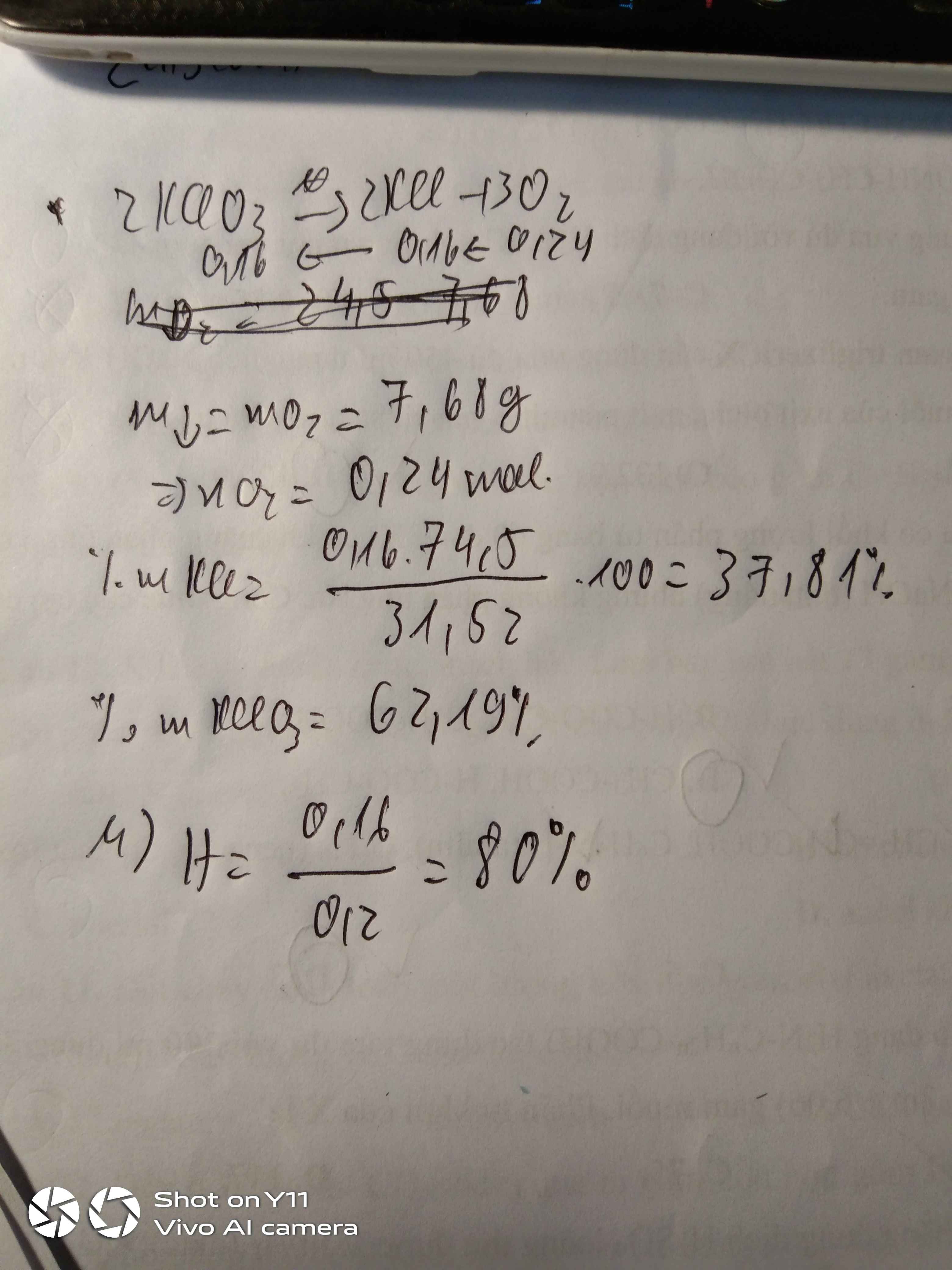



pt: 2KMnO4 ---> K2MnO4 + MnO2 + O2
Áp dụng định luật bảo toàn khối lượng:
=> mO2 = mKMnO4 - mhh X= 79-72,6=6,4(g)
=>nO2=6,4/32=0,2(mol)
Theo pt: nKMnO4=2nO2=2.0,2=0,4(mol)
=>mKMnO4=0,4.158=63,2(g)
===>mKMnO4 dư=79-63,2=15,8(g)
Theo pt: nK2MnO4=nO2=0,2(mol)
=>mK2MnO4=0,2.197=39,4(g)
=>%K2MnO4=39,4/72,6.100~54,27%
Theo pt: nMnO2=nO2=0,2(mol)
=>mMnO2=0,2.87=17,4(g)
=>%MnO2=17,4/72,6.100~23,97%
=>%mKMnO4 dư=100%-23,97%-54,27%=21,76%
b)H%=63,2/79.100=80%