Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

3Fe + 2O2 \(\underrightarrow{t^0}\) Fe3O4
Áp dụng ĐLBTKL, ta có
mFe + mO2 = mFe3O4
16,8 + mO2 = 23,2
mO2 = 6,4 (g)
nFe\(_3\)O\(_4\)=0,1 mol
nFe=0,3 mol
3Fe + 2O2 →Fe3O4
0,3 0,2 0,1
\(\Rightarrow\)mO2\(=0,2\times32=6,4\) g

a) nFe= 0,25(mol)
PTHH: Fe + H2SO4 -> FeSO4 + H2
0,25______0,25______0,25__0,25(mol)
b) V(H2,đktc)=0,25.22,4=5,6(l)
c) mH2SO4= 0,25.98= 24,5(g)

a, Phương trình chữ: Magie + Oxi \(\rightarrow\) Magieoxit
b, Công thức khối lượng: mMg + m\(O_2\) = mMgO
c, Áp dụng công thức khối lượng của phương trình, ta có:
mMg + m\(O_2\) = mMgO \(\Rightarrow\) m\(O_2\) = mMgO - mMg = 60g - 36g = 24g
Vậy số oxi đã phản ứng là 24g

\(a) 4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3\\ n_{Al} = \dfrac{5,4}{27} = 0,2(mol)\\ n_{Al_2O_3} = \dfrac{1}{2}n_{Al} = 0,1(mol) \Rightarrow m_{Al_2O_3} = 0,1.102 = 10,2(gam)\\ b) n_{O_2} = \dfrac{3}{4}n_{Al} = 0,15(mol)\\ 2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2\\ n_{KMnO_4} = 2n_{O_2} = 0,3(mol) \Rightarrow m_{KMnO_4} = 0,3.158 = 47,4(gam)\)
a, PT: \(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
Ta có: \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
Theo PT: \(n_{Al_2O_3}=\dfrac{1}{2}n_{Al}=0,1\left(mol\right)\)
\(\Rightarrow m_{Al_2O_3}=0,1.102=10,2\left(g\right)\)
b, Theo PT: \(n_{O_2}=\dfrac{3}{4}n_{Al}=0,15\left(mol\right)\)
PT: \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
Theo PT: \(n_{KMnO_4}=2n_{O_2}=0,3\left(mol\right)\)
\(\Rightarrow m_{KMnO_4}=0,2.158=47,4\left(g\right)\)
Bạn tham khảo nhé!

Câu 4:
PTHH: Zn + 2HCl ===> ZnCl2 + H2
Áp dụng định luật bảo toàn khối lượng, ta có:
\(m_{Zn}+m_{HCl}=m_{ZnCl_2}+m_{H_2}\)
\(\Leftrightarrow m_{HCl}=m_{ZnCl_2}+m_{H_2}-m_{Zn}\)
\(\Leftrightarrow m_{HCl}=27,2+0,4-13=14,6\left(gam\right)\)
Vậy khối lượng axit cần dùng là 14,6 gam

\(n_{Zn}=\dfrac{m_{Zn}}{M_{Zn}}=\dfrac{19,5}{65}=0,3mol\)
\(Zn+\dfrac{1}{2}O_2\rightarrow\left(t^o\right)ZnO\)
1 1/2 1 (mol)
0,3 0,15 0,3 ( mol )
PƯ trên thuộc loại phản ứng hóa hợp
\(m_{ZnO}=n_{ZnO}.M_{ZnO}=0,3.81=24,3g\)
\(V_{O_2}=n_{O_2}.22,4=0,15.22,4=3,36l\)

a) 4Al + 3O2 --to--> 2Al2O3
b) \(n_{O_2}=\dfrac{19,2}{32}=0,6\left(mol\right)\)
PTHH: 4Al + 3O2 --to--> 2Al2O3
0,8<-0,6---------->0,4
=> mAl = 0,8.27 = 21,6(g)
c) mAl2O3 = 0,4.102 = 40,8(g)

a) PTHH: 4Al + 3O2 =(nhiệt)=> 2Al2O3
b) Ta có: nAl = \(\frac{32,4}{27}=1,2\left(mol\right)\)
nO2 = \(\frac{21,504}{22,4}=0,96\left(mol\right)\)
Lập tỉ lệ số mol: \(\frac{1,2}{4}< \frac{0,96}{3}\)
=> Al hết, Oxi dư
=> Tính theo số mol Al
=> nO2 (dư) = 0,96 - \(\frac{1,2\times3}{4}=0,06\left(mol\right)\)
=> mO2 = 0,06 x 32 = 1,92 (gam)
c) Chất tạo thành là Al2O3
=> nAl2O3 = \(\frac{1,2\times2}{4}=0,6\left(mol\right)\)
=> mAl2O3 = 0,6 x 102 = 61,2 (gam)
a)PTHH: 4Al + 3O2 -> 2Al2O3
b) Ta có:
\(n_{Al}=\frac{32,4}{27}=1,2\left(mol\right)\\ n_{O_2}=\frac{21,504}{22,4}=0,96\left(mol\right)\)
Ta có:
\(\frac{n_{Al\left(đềbài\right)}}{n_{Al\left(PTHH\right)}}=\frac{1,2}{4}=0,3< \frac{n_{O_2\left(đềbài\right)}}{n_{O_2\left(PTHH\right)}}=\frac{0,96}{3}=0,32\)
Vậy: Al hết, O2 dư nên tính theo nAl.
Theo PTHH và đề bài, ta có:
\(n_{O_2\left(phảnứng\right)}=\frac{3.n_{Al}}{4}=\frac{3.1,2}{4}=0,9\left(mol\right)\)
\(n_{O_2\left(dư\right)}=n_{O_2\left(banđầu\right)}-n_{O_2\left(phảnứng\right)}=0,96-0,9=0,06 \left(mol\right)\)
Khối lượng O2 dư:
\(m_{O_2\left(dư\right)}=n_{O_2\left(dư\right)}.M_{O_2}=0,06.32=1,92\left(g\right)\)
c) Theo PTHH và đề bài, ta có:
\(n_{Al_2O_3}=\frac{2.n_{Al}}{4}=\frac{2.1,2}{4}=0,6\left(mol\right)\)
Khối lượng Al2O3 thu được:
\(m_{Al_2O_3}=n_{Al_2O_3}.M_{Al_2O_3}=0,6.102=61,2\left(g\right)\)
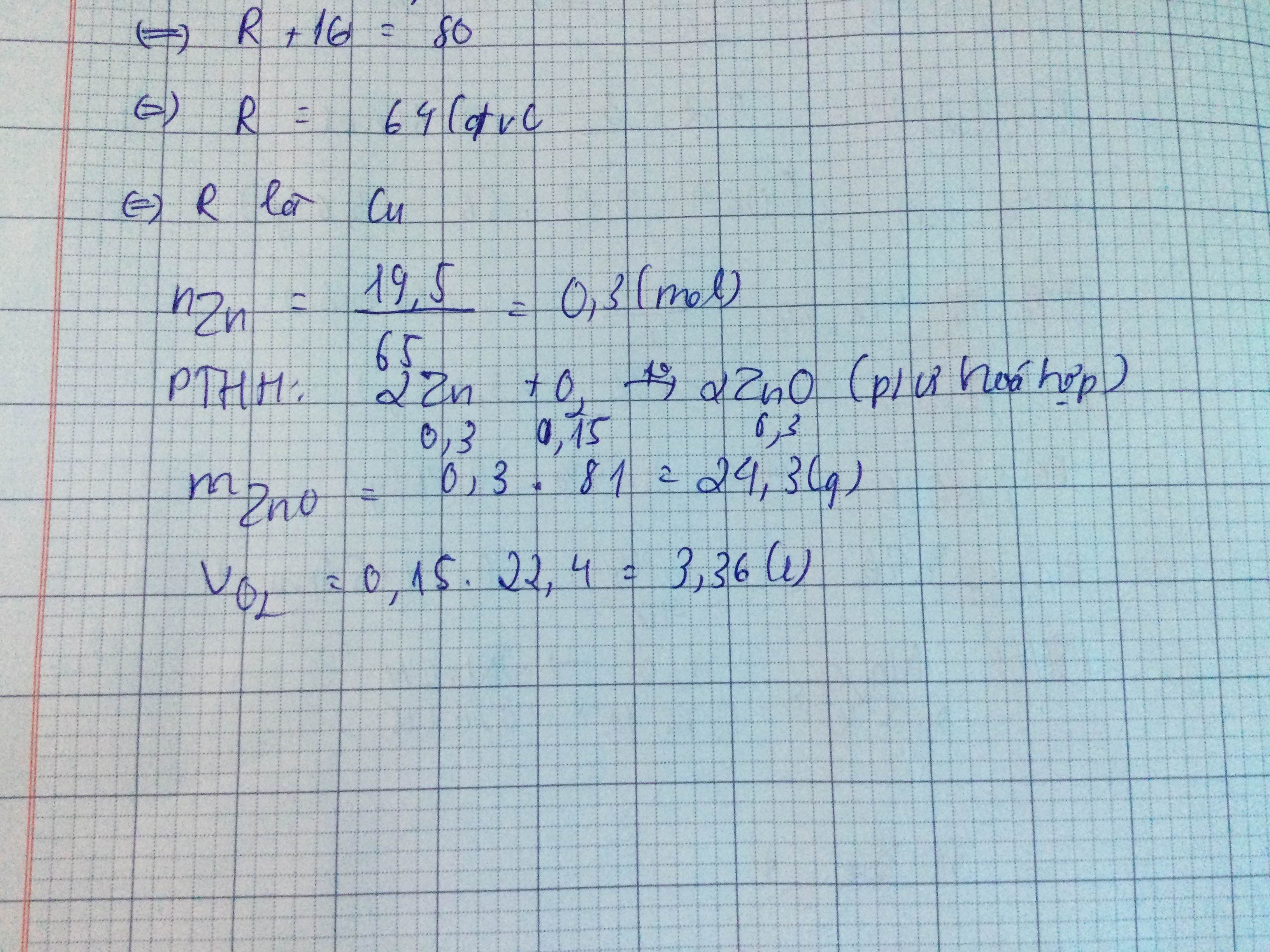
1/
a) PTHH 2Mg + O2 ===> 2MgO
b) Phương trình bảo toàn khối lượng là:
mMgO + mO2 = mMgO
c) Áp dụng định luật bào toàn khối lượng theo câu b) ta có:
mO2 = mMgO - mMg
<=> mO2 = 15 - 9 = 6 gam