Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1) có 18 công thức phân tử nước
2) 63Cu16O , 63Cu17O ,63Cu18O
65Cu16O ,65Cu17O .65Cu18O

1) Có 18 công thức phân tử nước
2) Có 6 công thức: 63Cu16O ; 63Cu17O ;63Cu18O
65Cu16O ; 65Cu17O ; 65Cu18O

Ta có: \(63,54=\frac{63.x+65.\left(100-x\right)}{100}\)
\(\Rightarrow\%^{63}_{29}Cu=x=73\%;\%^{65}_{29}Cu=100-73=27\%\)
Đặt nCuCl2=1 mol
=> nCu=1 mol
=> \(n_{^{63}_{29}Cu}=1.73\%=0,73\left(mol\right)\)
%m63Cu/mCuCl2=\(\frac{63.0,73}{1.\left(63,54+35.2\right)}.100=34,44\%\)

Khối lượng nguyên tử của Cu :
\(\frac{\left(105.63+245.65\right)}{105+245}=64,4\left(g\right)\)
Vậy khối lượng của Cu là 64,4(g)

a) Gọi % số nguyên tử \(^{65}Cu\) là x
% số nguyên tử \(^{63}Cu\) là 100 - x
\(\overline{M}_{Cu}=63,546=\frac{65x+63\left(100-x\right)}{100}\)
\(\Rightarrow x=27,3\%\)
\(\Rightarrow M_{^{65}Cu}=A.x=65.27,3\%=17,745\)
\(\overline{M}_{CuO}=\overline{M_{Cu}}+\overline{M_O}=63,546+15,994=79,54\)
\(\%\left(m\right)^{65}Cu=\frac{M_{^{65}Cu}}{M_{CuO}}.100=\frac{17,745}{79,54}.100=22,31\%\)

Khối lượng nguyên tử trung bình của Cu là:
M=(63*72,7+65*27,3):100=63,54
Phần trăm khối lượng của 63Cu trong CuSO4=(63*72,7):(63,54+16*4 + 32)=28,71%

Viết nhầm:
Mtb= 63.69,09+65.30,91
100
Mtb=63,6182 và xấp xỉ bằng 64
=> Mtb=64

Gọi % đồng vị 21H là a: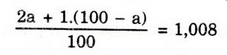
⇒ a = 0,8;
Khối lượng riêng của nước 1 g/ml, vậy 1ml nước có khối lượng 1g. Khối lượng mol phân tử của nước là 18g.




Câu 1
Câu 3: Đề ghi chưa chuẩn lắm!