Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{hh}=\dfrac{2,8}{22,4}=0,125mol\)
\(n_{Br_2}=\dfrac{4}{160}=0,025mol\)
\(n_{Br_2}=n_{C_2H_4}=0,025mol\)
\(\%V_{C_2H_4}=\dfrac{0,025}{0,125}.100=20\%\)
\(V_{CH_4}=100\%-20\%=80\%\)
=> Chọn D

\(n_{hh.khí}=\dfrac{2,8}{22,4}=0,125\left(mol\right)\\ n_{Br_2}=\dfrac{4}{160}=0,025\left(mol\right)\\ C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Khí metan không tác dụng với dd Br2
\(n_{C_2H_4}=n_{Br_2}=0,025\left(mol\right)\)
Vì số mol tỉ lệ thuận với thể tích. Nên:
\(\%V_{C_2H_4}=\%n_{C_2H_4}=\dfrac{0,025}{0,125}.100=20\%\\ \Rightarrow\%V_{CH_4}=100\%-20\%=80\%\)
Vậy chọn D
Chúc em học tốt và có được POP!
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
\(n_{Br_2}=\dfrac{4}{160}=0,025mol\)
\(V_{Br_2}=0,025.22,4=0,56l\)
\(\%V_{C_2H_4}=\dfrac{0,56.100}{2,8}=20\%\)

a) nC2H4Br2=47/188=0,25(mol)
n(CH4,C2H4)=11,2/22,4=0,5(mol)
PTHH: C2H4 + Br2 -> C2H4Br2
0,25<----------0,25<---------0,25(mol)
mBr2(p.ứ)=0,25 x 160= 40(g)
b) V(C2H4,đktc)=0,25 x 22,4= 5,6(l)
=> %V(C2H4)=(5,6/11,2).100=50%
=>%V(CH4)=100% - 50%= 50%

a, nBr2 = 8/160 = 0,05 (mol)
PTHH: C2H4 + Br2 -> C2H4Br2
Mol: 0,05 <--- 0,05 <--- 0,05
Vhh khí = 2,8/22,4 = 0,125 (mol)
%VC2H4 = 0,05/0,125 = 40%
%CH4 = 100% - 40% = 60%
b, nCH4 = 0,125 - 0,05 = 0,075 (mol)
PTHH: C2H4 + 3O2 -> (t°) 2CO2 + 2H2O
Mol: 0,05 ---> 0,15
CH4 + 2O2 -> (t°) CO2 + 2H2O
Mol: 0,075 ---> 0,15
Vkk = (0,15 + 0,15) . 5 . 22,4 = 33,6 (l)

\(n_{hh}=6,72:22,4=0,3mol\\ C_2H_2+2Br_2->C_2H_2Br_4\\ C_2H_4+Br_2->C_2H_2Br_2\\ n_{Br_2}=0,4mol\\ n_{C_2H_2}=a;n_{C_2H_4}=b\\ a+b=0,3\\ 2a+b=0,4\\ a=0,2;b=0,1\\ \%V_{C_2H_2}=\dfrac{0,2}{0,3}.100\%=66,67\%\\ \%V_{C_2H_4}=33,33\%\)
1/2 hỗn hợp có 0,1 mol C2H2 và 0,05mol C2H4
\(BT.C:n_{CO_2}=2n_{C_2H_2}+2n_{C_2H_4}=0,3mol\\ n_{CaCO_3}=n_{CO_2}=0,3\\ m_{KT}=0,3.100=30g\)

1. \(n_{Br_2}=0,4.0,5=0,2\left(mol\right)\)
PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Theo PT: \(n_{C_2H_4}=n_{Br_2}=0,2\left(mol\right)\Rightarrow V_{C_2H_4}=0,2.22,4=4,48\left(l\right)\)
2. \(n_{C_2H_4Br_2}=\dfrac{9,4}{188}=0,05\left(mol\right)\)
PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Theo PT: \(n_{C_2H_4}=n_{C_2H_4Br_2}=0,05\left(mol\right)\)
\(\Rightarrow\%V_{C_2H_4}=\dfrac{0,05.22,4}{1,4}.100\%=80\%\)
\(\Rightarrow\%V_{CH_4}=100-80=20\%\)

nBr2 = 0,125 mol
Khi đốt cháy nA = 0,25 mol
mNaOH ban đầu = 36g => nNaOH = 0,9 mol
Gọi x, y lần lượt là số mol của CO2 và H2O
mdd = 180 + 44x + 18y
Vì NaOH dư do đó chỉ tạo muối trung hòa
CO2 +2NaOH → Na2CO3 + H2O
x 2x
nNaOH dư = 0,9 – 2x
có 2 , 75 % = 40 ( 0 , 9 - 2 x ) 180 + 44 x + 18 y . 100 % (1)
=> 81,21x + 0,495y = 31,05n
2,8 lít khí A tác dụng với 0,125 mol Br2
=> 5,6 lít khí A tác dụng với 0,25 mol Br2
Gọi số mol khí của CH4, C2H4 và C2H2 lần lượt là a; b; c
Ta có a + b + c = 0,25 mol
Và b + 2c = 0,25
=> a = c
=> khi đốt cháy hỗn hợp A cho nCO2 = nH2O
Thay vào (1) => x = y = 0,38 mol
Bảo toàn C, H khi đốt cháy ta có
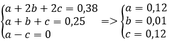
=> %VCH4 = %VC2H2 = 48%
%VC2H4 = 4%
Câu 1 :
Etilen: C2H4
Metan CH4
\(n_{Br2}=\frac{4}{160}=0,025\left(mol\right)\)
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
0,025_____0,025______
\(n_{khi}=\frac{2,8}{22,4}=0,125\left(mol\right)\)
\(V\%_{C2H4}=n\%_{C2H4}=\frac{0,025}{0,125}.100\%=20\%\)
\(\Rightarrow\%V_{CH4}=100\%-80\%=20\%\)
Câu 2 :
Etilen : C2H4
\(n_{C2H4}=0,01\left(mol\right)\)
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
0,01_______0,01____
\(\Rightarrow V=\frac{0,01}{0,1}=0,1\left(l\right)=100ml\)
Câu 3 :
Etilen : C2H4
\(n_{C2H4}=0,1\left(mol\right)\)
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
0,1___________0,1____
\(\Rightarrow m_{C2H4Br2}=0,1.188=18,8\left(g\right)\)
1. Dẫn 2.8l (đktc) hỗn hợp khí metan và etilen qua bình đựng dung dịch brom dư thấy 4g brom đã phản ứng. Thành phần % về V các khí trong hỗn hợp lần lượt là:
A. 50:50 B. 40:60 C. 30:70 D. 80:20
2. Cho 0.224l khí etilen phản ứng vừa đủ với V (l) dd brom 0.1M. Giá trị của V tính theo ml là:
A. 200 B. 150 C. 100 D.50
3. Dẫn 2.24l khí etilen vào dd brom dư thu được m (g) sản phẩm hữu cơ. Giá trị của m là:
A. 18.8 B.2.8 C. 10.8 D.13.8