Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Pham Van Tien, Nguyễn Nhật Anh, Nguyễn Công Minh, Thiên Thảo, Nguyễn Thị Ngọc An, Đặng Anh Huy 20141919, Nguyễn Thị Thu, Trịnh Thị Kỳ Duyên, 20143023 hồ văn nam, 20140248 Trần Tuấn Anh, buithianhtho, Duong Le, Linh, Quang Nhân, Hùng Nguyễn, Cù Văn Thái, Phạm Hoàng Lê Nguyên, Huyền, Băng Băng 2k6, Trần Hữu Tuyển, Phùng Hà Châu, Hoàng Tuấn Đăng, Nguyễn Trần Thành Đạt, Nguyễn Thị Minh Thương , Nguyễn Thị Kiều, Nguyễn Anh Thư,...

Ở 20oC: 100 gam nước hoà tan 32 gam KNO3
=> 500 gam nước hoà tan \(\frac{500.32}{100}=160\left(gam\right)KNO_3\)
Vậy khối lượng KNO3 tách ra khỏi dung dịch là:
450 - 160 = 290 (gam)
Gọi khối lượng KNO3 tách ra là a
Khối lượng của dung dịch ở 85°C là
mdd=mct+mH2O
=450+500=950(g)
mdd sau khi tách là
950-a(g)
mKNO3 có trong dung dịch sau khi tách là
450-a(g)
Ở 20°C 100 g H2O hòa tan 32 g KNO3 để tạo 132 g dung dịch bão hòa
Hay 100 g H2O hòa tan 450-a g KNO3 để tạo
950-a g dung dịch bão hòa
->32.(950-a)=132.(450-a)
->30400-32a=59400-132a
->132a-32a=59400-30400
->100a=29000
->a=290
Vậy khối lượng KNO3 tách ra là 290 g

\(n_{K2O}=\dfrac{9,4}{94}=0,1\left(mol\right)\)
Pt : \(K_2O+H_2O\rightarrow2KOH|\)
1 1 2
0,1 0,2
a) \(n_{KOH}=\dfrac{0,1.2}{1}=0,2\left(mol\right)\)
200ml = 0,2l
\(C_{M_{ddKOH}}=\dfrac{0,2}{0,2}=1\left(M\right)\)
b) Pt : \(KOH+HCl\rightarrow KCl+H_2O|\)
1 1 1 1
0,1 0,1
\(n_{HCl}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
\(m_{HCl}=0,1.36,5=3,65\left(g\right)\)
\(m_{ddHCl}=\dfrac{3,65.100}{10}=36,5\left(g\right)\)
c) \(CO_2+2KOH\rightarrow K_2CO_3+H_2O|\)
1 2 1 1
0,05 0,1
\(n_{CO2}=\dfrac{0,1.1}{2}=0,05\left(mol\right)\)
\(V_{CO2\left(dktc\right)}=0,05.22,4=1,12\left(l\right)\)
Chúc bạn học tốt

Gọi hóa trị của Fe là x.
\(Feclx+xAgnO_3\rightarrow Fe\left(NO_3\right)+xAgCl\uparrow\)
Số mol AgCl sinh ra:
\(n_{AgCl}=8,61\text{/}143,5=0,06mol\)
- Ta có (56 + 35,5x) gam FeClx tham gia phản ứng thì có x mol AgCl tạo thành.
- Tương tự 3,25 g muối tạo thành 0,06 mol kết tủa.
Vậy 3,25x = 0,06.(56 + 35,5x) → x = 3.
→ Vậy muối đó là FeCl3.

K + H2O -------> KOH + 1/2 H2
nK = 5,85/39=0,15 (mol)
Theo PT : nKOH=nK = 0,15 (mol)
=> CM KOH = n/V = 0,15/0,1=1,5M
=> Chọn C
Số mol của kali
nK = \(\dfrac{m_K}{M_K}=\dfrac{5,85}{39}=0,15\left(mol\right)\)
Pt : 2K + 2H2O → 2KOH + H2\(|\)
2 2 2 1
0,15 0,15
Số mol của dung dịch kali hidroxit
nKOH= \(\dfrac{0,15.2}{2}=0,15\left(mol\right)\)
Nồng độ mol của dung dịch kali hidroxit
CMKOH = \(\dfrac{0,15}{0,1}=1,5\left(M\right)\)
⇒ Chọn câu : C
Chúc bạn học tốt
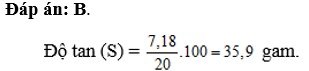

Ở 20oC: 190g nước hòa tan tối đa 60g KNO3
→ 100g nước hòa tan tối đa\(\frac{100.60}{190}=31,58gKNO3\)
-độ tan của KNO3 ở 20°C;
S=60×100:190=600:190=31,58 (g)