Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi n KMnO4 = a
n KClO3 = b ( mol )
--> 158a + 122,5 b = 43,3
PTHH :
\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\uparrow\)
0,9b 1,35b
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
0,9a 0,45a
\(\%Mn=\dfrac{55a}{43,3-32\left(0,45a+1,35b\right)}=24,103\%\)
\(\rightarrow a=0,15\)
\(b=0,16\)
\(m_{KMnO_4}=0,15.158=23,7\left(g\right)\)
\(m_{KClO_3}=0,16.122,5=19,6\left(g\right)\)

Đặt :
nFeO (bđ) = a (mol)
nZnO ( bđ) = b (mol)
=> mhh = 72a + 81b = 15.3 (g) (1)
FeO + H2 -to-> Fe + H2O
ZnO + H2 -to-> Zn + H2O
m chất rắn = mFeO dư + mZnO dư + mFe + mZn
=> 0.2a*72 + 0.2b*81 + 56*0.8a + 65*0.8b = 12.74
=> 59.2a + 68.2b = 12.74 (2)
(1) , (2) :
a = b = 0.1
%FeO = 0.1*72/15.3 * 100% = 47.06%
%ZnO = 100 - 47.06 = 52.94%

Câu 7 :
1) \(n_{Fe3O4}=\dfrac{34,8}{232}=0,15\left(mol\right)\)
Pt : \(Fe_3O_4+4H_2\underrightarrow{t^o}3Fe+4H_2O|\)
1 4 3 4
0,15 0,45
\(n_{Fe}=\dfrac{0,15.3}{1}=0,45\left(mol\right)\)
\(m_{Fe\left(Lt\right)}=0,45.56=25,2\left(g\right)\)
⇒ \(m_{Fe\left(tt\right)}=25,2.90\%=22,68\left(g\right)\)
Chúc bạn học tốt
\(n_{Fe_3O_4}=\dfrac{34,8}{232}=0,15\left(mol\right)\)
\(pthh:Fe_3O_4+H_2\underrightarrow{t^o}Fe+H_2O\)
0,15 0,15
=> \(m_{Fe}=\dfrac{90.0,15}{100}.56=7,56\left(g\right)\)

a) PTHH : \(FeO+H_2-t^o->Fe+H_2O\)
\(CuO+H_2-t^o->Cu+H_2O\)
Đặt \(\hept{\begin{cases}n_{FeO}=x\left(mol\right)\\n_{CuO}=y\left(mol\right)\end{cases}}\) => \(72x+80y=11,2\left(I\right)\)
Có : \(m_{O\left(lấy.đi\right)}=m_{giảm}=1,92\left(g\right)\)
=> \(n_{O\left(lấy.đi\right)}=\frac{1,92}{16}=0,12\left(mol\right)\) Vì H% = 80% => Thực tế : \(n_{O\left(hh\right)}=\frac{0,12}{80}\cdot100=0,15\left(mol\right)\)
BT Oxi : \(x+y=0,15\left(II\right)\)
Từ (I) và (II) suy ra : \(\hept{\begin{cases}x=0,1\\y=0,05\end{cases}}\)
=> \(\hept{\begin{cases}m_{FeO}=7,2\left(g\right)\\m_{CuO}=4\left(g\right)\end{cases}}\)
b) PTHH : \(Fe+H_2SO_4-->FeSO_4+H_2\)
BT Fe : \(n_{Fe}=n_{FeO}=0,1\left(mol\right)\)
Theo pthh : \(n_{H_2}=n_{Fe}=0,1\left(mol\right)\)
=> \(V_{H_2}=2,24\left(l\right)\)
BT Cu : \(n_{Cu}=n_{CuO}=0,05\left(mol\right)\)
=> \(m_{CR\left(ko.tan\right)}=0,05\cdot64=3,2\left(g\right)\)

CaCO3 →to CaO + CO2 (1)
MgCO3 →to MgO + CO2 (2)
\(n_{CO_2}=\dfrac{15,4}{44}=0,35\left(mol\right)\)
Gọi \(x,y\) lần lượt là số mol của CaCO3 và MgCO3
Theo PT1: \(n_{CO_2}=n_{CaCO_3}=x\left(mol\right)\)
Theo PT2: \(n_{CO_2}=n_{MgCO_3}=y\left(mol\right)\)
Ta có: \(\left\{{}\begin{matrix}100x+84y=31,8\\x+y=0,35\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,15\\y=0,2\end{matrix}\right.\)
Vậy \(n_{CaCO_3}=0,15\left(mol\right);n_{MgCO_3}=0,2\left(mol\right)\)
Theo PT1: \(n_{CaO}=n_{CaCO_3}=0,15\left(mol\right)\)
\(\Rightarrow m_{CaO}=0,15\times56=8,4\left(g\right)\)
Theo PT2: \(n_{MgO}=n_{MgCO_3}=0,2\left(mol\right)\)
\(\Rightarrow m_{MgO}=0,2\times40=8\left(g\right)\)
\(\Sigma m_{oxit}=m_{CaO}+m_{MgO}=8,4+8=16,4\left(g\right)\)

\(a.MgCO_3-t^{^0}->MgO+CO_2\\ CaCO_3-t^{^0}->CaO+CO_2\\ b.n_{MgCO_3}=a,n_{CaCO_3}=b\\ 84a+100b=26,8\\ 40a+56b=13,6\\ a=0,2;b=0,1\\ \%m_{MgCO_3}=\dfrac{84a}{26,8}.100\%=62,69\%\\ \%m_{CaCO_3}=37,31\%\\ c.V_{CO_2}=22,4\left(a+b\right)=6,72L\)

Đầu tiên phải đổi về số mol đã:
PTHH: 2 KMnO4
K2MnO4 + MnO2 + O2
pt 2 1 1 1
Mol 0,9 0,45 0,45 0,45
Hp/ứ = 80% m KMnO4 ban đầu =
nKMnO4 ban đầu = 177,75: 158 = 1,125 mol
nKMnO4 dư= 1,125 – 0,9 = 0,225 mol.
Thuốc tím có lẫn 10% tạp chất
m thuốc tím =
Khối lượng chất rắn sau phản ứng: 197,5 – 0,45.32 = 183,1 gam
Chất rắn sau phản ứng gồm KMnO4 dư, K2MnO4, MnO2, tạp chất.
%MnO2/CR=
%K2MnO4/CR=
\(n_K=n_{O_2}=\dfrac{V}{22,4}=0,45\left(mol\right)\)
\(PTHH:2KMnO_4\rightarrow K_2MnO_4+MnO_2+O_2\)
....................0,9..............................................0,45........
\(\Rightarrow m_{KMnO_4}=n.M=142,2\left(g\right)\)
Mà H = 80 %
\(\Rightarrow m_{KMnO_4tg}=177,75\%\)
Lại có : Trong m g thuốc tím chỉ có 90% phản ứng .
\(\Rightarrow m=197,5\left(g\right)\)
Vậy ...
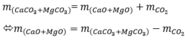
\(MgCO_3\underrightarrow{^{t^o}}MgO+CO_2\\ CaCO_3\underrightarrow{^{t^o}}CaO+CO_2\\ n_{CO_2}=\dfrac{4,4}{44}=0,1\left(mol\right)\\ m_{CO_2\left(90\%\right)}=0,1.90\%.44=3,96\left(g\right)\)