Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(m_{CO_2}=\dfrac{3,36}{22,4}.44=6,6(g)\)
Áp dụng định luật BTKL: \(m_{\text{hh muối}}=m_{\text{hh oxit}}+m_{CO_2}=76+6,6=82,6(g)\)

Gọi số mol CaCO3;MgCO3 lần lượt là : a;b
PTHH:
CaCO3 -->(nhiệt độ) CaO+CO2 (1)
P/ứ: a -------------------> a ---> a (mol)
MgCO3-->(nhiệt độ) MgO+CO2 (2)
P/ứ: b--------------------> b ---> b Mol)
Theo PTHH (1);(2) => mCaO+mMgO
=56a+40b=76(g) (*1)
và nCO2=a+b=33.6/22.4=1.5(mol) (*2)
Kết hợp (*1) và (*2) => a=1;b=0.5
=>mCaCO3=1*100=100(g)
mMgCO3=0.5*84=42(g)
=>%mCaCO3=100/(100+42)*100%
=70.42%
%mMgCO3=100%-76.42%=23.58%

PTHH: \(CaCO_3\underrightarrow{t^o}CaO+CO_2\) (1)
\(MgCO_3\xrightarrow[]{t^o}MgO+CO_2\) (2)
\(2NaOH+CO_2\xrightarrow[]{t^o}Na_2CO_3+H_2O\) (3)
\(n_{Na_2CO_3}=\dfrac{15,9}{106}=0,15\left(mol\right)\)
=> \(n_{CO_2}=0,15\left(mol\right)\)
Bảo toàn khối lượng pư 1,2:
\(m_{hh}=m_{oxit}+m_{CO_2}=7,6+0,15\times44=14,2\left(g\right)\)
vậy khối lượng hh muối là 14,2 gam

nNa2CO3=0,15 mol
MgCO3 -----> MgO+ CO2
x mol x mol x mol
CaCO3--------> CaO + CO2
y mol y mol y mol
NaOH + CO2-----> Na2CO3+ H2O
0,15mol 0,15mol
ta được hệ phương trình
\(\left\{{}\begin{matrix}56x+40y=7,6\\x+y=0,15\end{matrix}\right.\)
\(\left\{{}\begin{matrix}x=0,05\\y=0,1\end{matrix}\right.\)
khối lượng hỗn hợp muối là
mhh=mCaCO3+mMgCO3
=100.0,05+84.0,1
=13,4g
bạn cân bằng phương trình Thứ 3 sai rồi, phải là
2NaOH + CO2 = Na2CO3 + H2O

\(a.MgCO_3-t^{^0}->MgO+CO_2\\ CaCO_3-t^{^0}->CaO+CO_2\\ b.n_{MgCO_3}=a,n_{CaCO_3}=b\\ 84a+100b=26,8\\ 40a+56b=13,6\\ a=0,2;b=0,1\\ \%m_{MgCO_3}=\dfrac{84a}{26,8}.100\%=62,69\%\\ \%m_{CaCO_3}=37,31\%\\ c.V_{CO_2}=22,4\left(a+b\right)=6,72L\)
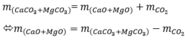
Đáp án:
Giải thích các bước giải:
Gọi x, y lần lượt là số mol của CaCO3 và MgCO3
Ta có
56x+40y= 76
x+y= 66/44=1,5
Suy ra x=1 y=0,5
Khối lượng muối ban đầu là 100.1+84.0,5= 142g
Hoặc m=76+66=142g