Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
80 g a m C a C O 3 . M g C O 3 t ạ p c h ấ t → t 0 C a O M g O t ạ p c h ấ t → H 2 O C a ( O H ) 2 + M g O t ạ p c h ấ t

Đáp án A
2 Al + Fe 2 O 3 → t o Al 2 O 3 + 2 Fe
Vì chia hỗn hợp Y thành hai phần bằng nhau nên số mol mỗi chất trong hai phần đều bằng nhau.
Vì phần 1 tác dụng với dung dịch NaOH có xuất hiện khí nên Y có Al.
Do đó Y có Al, Fe, A12O3 và có thể có Fe2O3.


Giải thích: Đáp án C
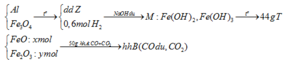
CO+O(trong FeO+Fe2O3) →CO2
1 1 m↑=44-28=16 g
a a m↑=16a
Do nA = nB => mB / mA = (50+16a) /50 = 1,208 => a = 0,65 mol.
Ta có:
56x + 160y = 44
x + 3y = nCopu = 0,65
=> x = 0,5; y = 0,05 (mol).
BTNT Fe: 3nFe3O4 = nFeO + 2nFe2O3 => nFe3O4 = 0,2 mol f
Al0 - 3e → Al+ 3 H+ + 2e → H2
Fe3 +8/3 -1e → 3Fe + 3 Fe3+8/3 + 2e→ 3Fe +2
Đặt nAl = b mol. Bảo toàn e: 3b + + 1/3nFe3+ = 2nH2 + 3/2nFe2+ => b = 91/180 mol.
=> m=91/180.27+0,2.232= 60,05 gam.
BTNT S: nH2SO4pu = 3nAl2(SO4)3 + nFeSO4 + 3nFe2(SO4)3 = 3.91/360 + 0,5 + 3.0,05 = 169/120 mol.
=>V=169/120 /0,7=169/84 lít.
=> m - V= 60,5 - 169/84 = 58,038 ≈ 58,04

\(n_{NaCl} = 0,5.0,1 = 0,05(mol); n_{AlCl_3} = 0,5.0,3 = 0,15(mol)\)
2AlCl3 + 6H2O → 2Al(OH)3 + 3H2 + 3Cl2
0,15..........................0,15.................................(mol)
2NaCl + 2H2O → 2NaOH + H2 + Cl2
0,05.........................0,05.........................(mol)
Al(OH)3 + NaOH → NaAlO2 + 2H2O
0,05............0,05.....................................(mol)
\(n_{Al(OH)_3} = 0,15 - 0,05 =0,1(mol)\\ 2Al(OH)_3 \xrightarrow{t^o} Al_2O_3 + 3H_2O\\ n_{Al_2O_3} = \dfrac{1}{2}n_{Al(OH)_3} = 0,05(mol)\\ m_{Al_2O_3} = 0,05.102 = 5,1(gam)\)

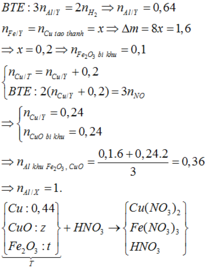
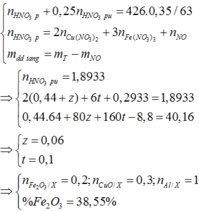
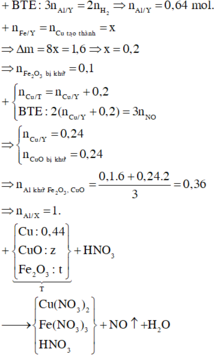
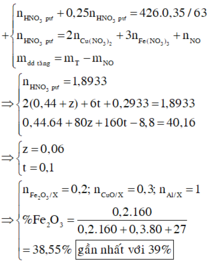

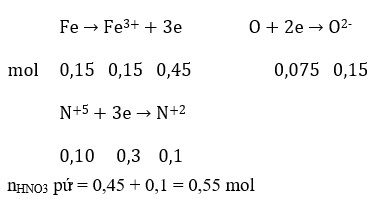
2KMnO4 = K2MnO4 + MnO2 + O2
Độ giảm khối lượng chất rắn = m O2 = 47,4 – 44,04 = 3,36 gam
Suy ra n CO2 = 3,36 : 32 = 0,105 mol => n KMnO4 tham gia = 0,105.2 = 0,21 mol.
=>% m KMnO4 phản ứng = ((0,21.158):47,4).100% = 70%