Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{KMnO_4}=\dfrac{15,8}{158}=0,1\left(mol\right)\)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
a-------------->0,5a----->0,5a
=> 158(0,1-a) + 197.0,5a + 87.0,5a = 14,84
=> a = 0,06 (mol)
PTHH: 2KMnO4 + 16HCl --> 2KCl + 2MnCl2 + 5Cl2 + 8H2O
0,04----------------------------------->0,1
K2MnO4 + 8HCl --> 2KCl + MnCl2 + 2Cl2 + 4H2O
0,03--------------------------------->0,06
MnO2 + 4HCl --> MnCl2 + Cl2 + 2H2O
0,03--------------------->0,03
=> \(n_{Cl_2}=0,1+0,06+0,03=0,19\left(mol\right)\)
=> \(V_{Cl_2}=0,19.22,4=4,256\left(l\right)\)

Theo đề bài, sắt còn dư sau khi phản ứng với lưu huỳnh
PTHH: \(Fe+S\underrightarrow{t^o}FeS\) (1)
\(FeS+2HCl\rightarrow FeCl_2+H_2S\uparrow\) (2)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\) (3)
Ta có: \(n_{hhkhí}=\dfrac{2,688}{22,4}=0,12\left(mol\right)=n_{Fe\left(3\right)}+n_{FeS}=\Sigma n_{Fe}\)
\(\Rightarrow m_{Fe}=0,12\cdot56=6,72\left(g\right)\)

Em có thể tham khảo cách giải sau:
Ta có: mO2 = (15,8 + 24,5)-36,3 = 4 gam. => nO2 = 0,125 mol.
nKMnO4 = 0,1 mol, nKClO3 = 0,2 mol.
Mn7+ + 5e -> Mn2+
Cl5+ + 6e -> Cl-1
2O2- -> O2 + 4e
2Cl-1 -> Cl2 + 2e
Bảo toàn electron, ta có: 0,1*5 + 0,2*6 = 0,125*4 + 2*nCl2
=> nCl2 =0,6 mol.
3Cl2 + 6NaOH -> 5NaCl + NaClO3 + 3H2O (vì đun nóng).
Bđ 0,6 1,5
P/ư 0,6 1,2 1,0 0,2
Sau p/ư 0 0,3 1,0 0,2.
=> m Rắn =0,3*40 + 1,0*58,5 + 0,2*106,5 = 91,8 gam.

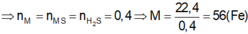
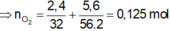
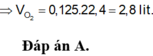
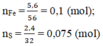
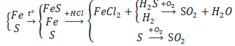

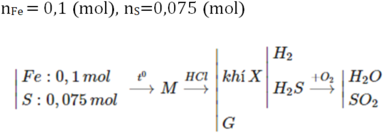

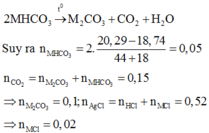
2KMnO4=>K2MnO4 + MnO2 + O2
1 0,5 0,5 0,5 (mol)
như vậy hh rắn gồm 0,5 mol MnO2 và 1 mol KMnO4
MnO2 + 2e =>Mn+2
0,5 1
MnO4 + 5e=>Mn+2
1 5
MnO4(2-) +4e=>Mn+2
0,5 2
=>e trao đổi=8mol
2Cl- -2e=>Cl2
8 4
=>V=4.22,4=89,6(l)
Cách của bn trên đúng nhưng vẫn cần viết pt, nêu bn muốn full bt e thì nnày ha :v
\(m_{O_2}=316-300=16\left(g\right)\)
=> \(n_{O_2}=\dfrac{16}{32}=0,5\left(mol\right)\)
\(n_{KMnO_4}=\dfrac{316}{158}=2\left(mol\right)\)
Mn+7 +5e --> Mn+2
2---->10
2O-2 -4e --> O20
2<---0,5
2Cl- - 2e --> Cl20
2x<---x
Bảo toàn e: 2x = 8
=> x = 4
=> V = 4.22,4 = 89,6 (l)