Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{CaO} = \dfrac{11,2.1000}{56} = 200(kmol)\\ CaCO_3 \xrightarrow{t^o} CaO + CO_2\\ n_{CaCO_3\ pư} = n_{CaO} = 200(kmol)\\ n_{CaCO_3\ đã\ dùng} = \dfrac{200}{80\%} = 250(kmol)\\ m_{CaCO_3} = 250.100 = 25000(kg)\\ \Rightarrow m_{đá\ vôi} = \dfrac{25000}{90\%} = 27777,78(kg)\)

CaCO3 -----to---> CaO + CO2
mcaco3 = 100.8,4/56 = 15 tấn
khối lượng đá vôi thực tế cần là:
15:85% :90% = 19,61 tấn

PTHH: \(CaCO_3\xrightarrow[]{t^o}CaO+CO_2\)
Một tấn đá vôi có 80% CaCO3
\(\Rightarrow m_{CaCO_3}=800\left(kg\right)\) \(\Rightarrow n_{CaCO_3}=\dfrac{800}{100}=8\left(kmol\right)=n_{CaO\left(lý.thuyết\right)}\)
\(\Rightarrow m_{CaO\left(thực\right)}=8\cdot56\cdot90\%=403,2\left(kg\right)=403200\left(g\right)\)

1tấn đá vôi mà chứa 90% CaCO3 tuc la chua 900kg caco3
nCaCO3=9mol
CaCO3=>CaO+CO2
9mol-------> 9mol->9mol
=> mCaO=9.56=504kg
=> m vôi sống thu được 504:100.95=478,8kg

0,5 tấn = 500kg
\(\rightarrow m_{CaCO_3}=500.\left(100\%-10\%\right)=450kg\)
\(\rightarrow n_{CaCO_3}=\frac{450}{100}=0,45kmol\)
PTHH: \(CaCO_3\rightarrow^{t^o}CaO+CO_2\uparrow\)
Theo phương trình \(n_{CaO}=n_{CaCO_3}=0,45kmol\)
\(\rightarrow m_{CaO}=0,45.56=25,2kg=0,252\) tấn
\(\rightarrow m_{CaO\left(tt\right)}=0,252.85\%=0,2142\) tấn \(=214,2kg\)

\(m_{CaCO_3}=50\cdot80\%=40\left(tấn\right)=40000\left(kg\right)\)
\(n_{CaCO_3}=\dfrac{40000}{100}=400\left(kmol\right)\)
\(n_{CaCO_3\left(pư\right)}=400\cdot80\%=320\left(kmol\right)\)
\(CaCO_3\underrightarrow{^{t^0}}CaO+CO_2\)
\(320..........320\)
\(m_{CaO}=320\cdot56=17920\left(kg\right)=17.92\left(tấn\right)\)

\(n_{CaCO_3}=\dfrac{20}{100}.90\%.80\%=0,144(mol)\\ CaCO_3\xrightarrow{t^o}CaO+CO_2\\ \Rightarrow n_{CaO}=n_{CaCO_3}=0,144(mol)\\ \Rightarrow m_{CaO}=0,144.56=8,064(g)\)
C
Đáp án: C
CaCO3 \(\underrightarrow{to}\) CaO + CO2
Khối lượng CaCO3 trong 20g đá vôi là: 20 * 90% = 18 (g)
Số mol của CaCO3 là :\(n_{CaCO_3}\) = 18 : 100 = 0,18 (mol)
Số mol của CaO là: \(_{n_{CaO}}\) = \(n_{CaCO_3}\)= 0,18 (mol)
Khối lượng của CaO nếu hiệu suất phản ứng là 100% là: m = 0,18 * 56 = 10,08 (g)
Khối lượng của CaO nếu hiệu suất phản ứng là 80% là: 10,08 * 80% = 8,064 (g)

15 tấn = 15 000(kg)
$m_{CaCO_3} = 15000.90\% = 13500(kg)$
$n_{CaCO_3} = \dfrac{13500}{100} = 135(kmol)$
$n_{CaCO_3\ pư} = 135.85\% = 114,75(kmol)$
$CaCO_3 \xrightarrow{t^o} CaO + CO_2$
Theo PTHH : $n_{CaO} = n_{CaCO_3} = 114,75(kmol)$
$m_{CaO} = 114,75.56 = 6426(kg)$
Giải đáp thắc mắc :
100 là phân tử khối của $CaCO_3$
56 là phân tử khối của $CaO$
Cách làm như ảnh trên là áp số tỉ lệ về khối lượng theo PTHH
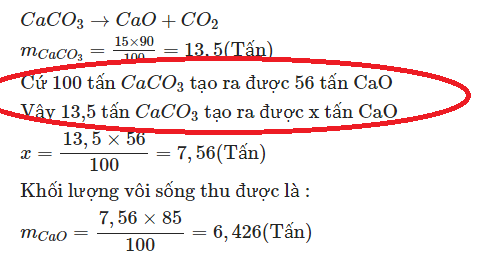
đổi 1 tấn = 1000000g
CaCO3 ---t*--> CaO + CO2
mCaCO3 =1000000*90%=900000g
nCaCO3=9000mol
nCaO=9000mol
hiệu suất đạt 80 % nên thực tế : n CaO=7200mol
mCaO=7200*56=403200g
mCaCO3=\(\frac{1.90}{100}\)=0,9 (tấn)
CaCO3 -to➝ CaO+ CO2
Tỉ lệ khối lượng: 100g ➝ 56g
0,9 tấn ➝ x tấn
x=\(\frac{0,9.56}{100}\) =0,504 (tấn)
Vì H=90%
\(\Rightarrow\) mCaO ttế= \(\frac{0,504.90}{100}\)= 0,4536 (tấn)