Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
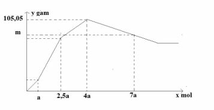
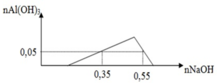
+ Tại n = 0,55 mol: BaSO4 đạt cực đại
nBa2+ = nSO42- => 0,55 = 3a + b
+ Tại n = 0,3 mol: Al(OH)3 bắt đầu bị hòa tan khiến cho lượng kết tủa tăng chậm lại
nOH- = 3nAl3+ => 2.0,3 = 3.2a => a = 0,1
=> b = 0,25
=> a : b = 2 : 5

Đáp án C
Định hướng tư duy giải
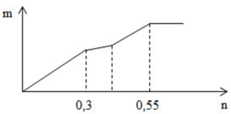
Giai đoạn 1: Tạo đến 102,6 gam kết tủa
là Ba(OH)2 chơi với (x mol) Al2(SO4)3
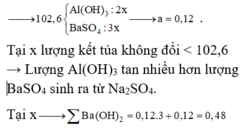

Chọn đáp án C.
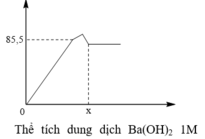
Khi mkết tủa = 85,5 gam, Al2(SO4)3 vừa phản ứng hết, K2SO4 bắt đầu phản ứng.
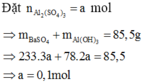
· Khi V dd Ba ( OH ) 2 = x ml, kết tủa Al(OH)3 tan hết, chỉ còn kết tủa BaSO4.
![]()

Giải thích:
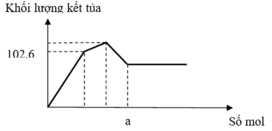
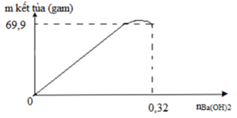
Tại nBa(OH)2=0,32 mol thì Al(OH)3 vừa bị hòa tan hết.
=> 4nAl3+=nOH-=>4.2b=0,32=>b=0,04 mol.
Mặt khác nBaSO4 max=a+3b=69,9/233=0,3 mol
=>a=0,06 mol.
Đáp án B

Đáp án D
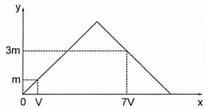
Ta có: x = 0,35 – 0,05.3 = 0,2
Tại điểm kết tủa cực đại là
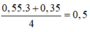
=> z = 0,2.
Khi thêm 0,27 Ba(OH)2 thì thu được kết tủa Z chứa
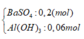
=> m = 51,28 gam



Đáp án cần chọn là: A