Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nFe2O3 = 23/160=0.14375mol
2Fe(OH)3 -> Fe2O3 + 2H2O
(mol) 0.2875 0.14375
mFe(OH)3 = x = 0.2875*107=30.7625g

a) PTHH: \(Cu\left(OH\right)_2\xrightarrow[]{t^o}CuO+H_2O\)
Ta có: \(n_{CuO}=\dfrac{4}{80}=0,05\left(mol\right)=n_{Cu\left(OH\right)_2}\) \(\Rightarrow m_{Cu\left(OH\right)_2}=0,05\cdot98=4,9\left(g\right)\)
b) PTHH: \(Cu\left(OH\right)_2+H_2SO_4\rightarrow CuSO_4+2H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{Cu\left(OH\right)_2}=0,05\left(mol\right)\\n_{H_2SO_4}=\dfrac{250\cdot9,8\%}{98}=0,25\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) Axit còn dư
\(\Rightarrow\left\{{}\begin{matrix}n_{CuSO_4}=0,05\left(mol\right)\\n_{H_2SO_4\left(dư\right)}=0,2\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}C\%_{CuSO_4}=\dfrac{0,05\cdot160}{4,9+250}\cdot100\%\approx3,14\%\\C\%_{H_2SO_4\left(dư\right)}=\dfrac{0,2\cdot98}{4,9+250}\cdot100\%\approx7,7\%\end{matrix}\right.\)

a) \(2Fe\left(OH\right)_3-^{t^o}\rightarrow Fe_2O_3+3H_2O\)
\(Cu\left(OH\right)_2-^{t^o}\rightarrow CuO+H_2O\)
Gọi x,y lần lượt là số mol Fe(OH)3 và Cu(OH)2
=> \(\left\{{}\begin{matrix}107x+98y=20,5\\160.\dfrac{x}{2}+80y=16\end{matrix}\right.\)
=> x= 0,1 ; y=0,1
=> \(\%m_{Fe\left(OH\right)_3}=\dfrac{0,1.107}{20,5}.100=52,2\%\)
\(\%m_{Cu\left(OH\right)_2}=47,8\%\)
b) \(2Fe\left(OH\right)_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+6H_2O\)
\(Cu\left(OH\right)_2+H_2SO_4\rightarrow CuSO_4+2H_2O\)
\(n_{H_2SO_4}=0,1.\dfrac{3}{2}+0,1=0,25\left(mol\right)\)
\(m_{ddH_2SO_4}=\dfrac{0,25.98}{20\%}=122,5\left(g\right)\)
\(m_{ddsaupu}=20,5+122,5=143\left(g\right)\)
\(C\%_{Fe_2\left(SO_4\right)_3}=\dfrac{0,05.400}{143}.100=13,97\%\)
\(C\%_{CuSO_4}=\dfrac{0,1.160}{143}.100=11,19\%\)
c) \(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
\(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)
\(n_{Fe_2O_3}=0,05\left(mol\right);n_{CuO}=0,1\left(mol\right)\)
=> \(n_{H_2SO_4}=0,05.3+0,1=0,25\left(mol\right)\)
\(m_{ddH_2SO_4\left(pứ\right)}=\dfrac{0,25.98}{20\%}=122,5\left(g\right)\)
=> \(m_{ddH_2SO_4\left(bđ\right)}=122,5.110\%=134,75\left(g\right)\)

PTHH: Mg(OH)2 =(nhiệt)==> MgO + H2O
x x
4Fe(OH)2 + O2 =(nhiệt)==> 2Fe2O3 + 4H2O
y 0,25y 0,5y
Gọi số mol của Mg(OH)2, Fe(OH)2 lần lượt là x, y
Lập các số mol theo phương trình và theo đề ra ta có hệ phương trình sau:
\(\begin{cases}58x+90y=1,32a\\40x+80y=a\end{cases}\)
Giải phương trình ta đc \(\begin{cases}x=0,015a\\y=0,005a\end{cases}\)
=> %mMgO =\(\frac{0,015a.40}{a}\) x 100% = 60%
=>%mFe2O3 = 100% - 60% = 40%
Chúc bạn hoc tốt!!!
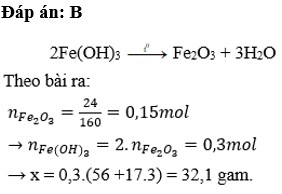

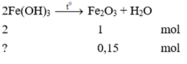
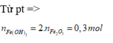
nFe2O3= 24/160= 0,15(mol)
PTHH: 2 Fe(OH)3 -to-> Fe2O3 +3 H2O
nFe(OH)3= 2. 0,15=0,3(mol)
=>x=mFe(OH)3= 107.0,3= 32,1(g)
=>x=32,1(g)