Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Na2CO3 không bị nhiệt phân, nên 2,24 lít khí sinh ra chính là CO2 do CaCO3 bị nhiệt phân theo phản ứng
![]()
Cách 1:
![]()
Áp dụng định luật bảo toàn khối lượng ta có:
m X = m c h ấ t r ắ n + m C O 2 = 11,6 + 0,1.44 = 16 (gam)
Vậy phần trăm khối lượng của CaCO3 trong hỗn hợp X là:
![]()
Cách 2:
Ta có:
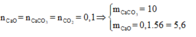
Hỗn hợp rắn thu được gồm CaO và Na2CO3
![]()
![]()
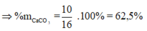
Đáp án D

Đáp án D
nCO2= nCaCO3 = 0,15 mol
ð mCaCO3 = 15 gam
mX= mrắn + mCO2
= 17,4+ 0,15.44=24 gam
%mCaCO3= (15:24).100%=62,5%

Chọn B.
Khi đốt cháy hoàn toàn muối X thì: mX = ![]() 7,32 (g)
7,32 (g)
Khi cho A tác dụng với NaOH thì: n H 2 O = m A + 40 . 2 n N a 2 C O 3 - m X 18 = 0 , 04 m o l
+ Nếu A là este đơn chức thì: n A = n H 2 O = 0 , 04 m o l ⇒ M A = 121 (loại)
+ Nếu A là este hai chức thì: n A = 0 , 5 n H 2 O = 0 , 02 m o l ⇒ M A = 242 : A là C6H5OOC-COOC6H5
Hỗn hợp X gồm (COONa)2: 0,02 mol và C6H5ONa: 0,04 mol Þ % m C 6 H 5 O N a = 63 , 39 %

Đáp án là C
Ta có ![]()
Bảo toàn khối lượng → mmuối =1,8+0,24.44+4,24-0,29.32= 7,32 gam
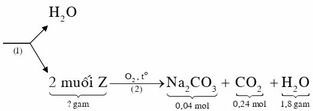
Bảo toàn nguyên tố → n N a O H = 2 n N a 2 C O 3 = 0 , 08 m o l
Bảo toàn khối lượng cho phản ứng đốt cháy m H 2 O = 4 , 84 + 0 , 08 . 40 - 7 , 32 m o l → n H 2 O = 0 , 04 m o l
Bảo toàn nguyên tố n C ( X ) = 0 , 04 + 0 , 24 = 0 , 28 m o l
Bảo toàn nguyên tố n H ( X ) = 0 , 1 . 2 + 0 , 04 . 2 - 0 , 08 = 0 , 2 m o l
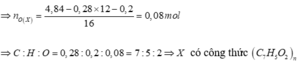
Số nguyên tử H luôn chẵn =>X có công thức C 14 H 10 O 4
X thủy phân tác dụng với NaOH chỉ sinh ra muối với nước=>X là este của phenol
X có công thức C 6 H 5 - O O C - C O O - C 6 H 5 : 0 , 02 m o l
Vậy muối thu được gồm NaOOC-COONa: 0,02 mol và C 6 H 5 O N a : 0,04 mol
⇒ % C 6 H 5 O N a = 0 , 04 . 116 7 , 32 . 100 % = 63 , 38 %

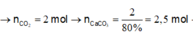


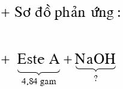
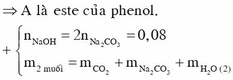
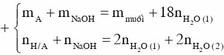
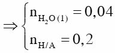
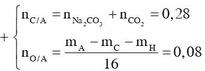
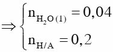
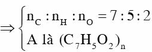
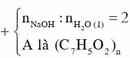
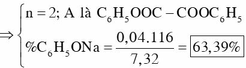
Giải thích:
CaCO3→CaO+CO2
nCO2=nCaCO3=20,37/22,4=0,9094 mol
=> mCaCO3=0,9094.100=94,94 gam
=> %mCaCO3=90,94/100=90,94%
Đáp án D