Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
n C 3 H 8 ban đầu = 0 , 2 . 90 % - 0 , 18 ( mol ) = > n C 3 H 8 dư = 0 , 02
Áp dụng định luật bảo toàn khối lượng ta có:
m A = m C 3 H 8 ban đầu
=8,8 gam
![]()
![]()
Vậy ![]()

\(n_{C_3H_8}=0,4\left(mol\right)\)
\(M_X=13,75.2=27,5\left(g/mol\right)\)
\(\Rightarrow n_X=\dfrac{17,6}{27,5}=0,64\left(mol\right)\)
\(\Rightarrow n_{C_3H_8\left(pư\right)}=0,64-0,4=0,24\left(mol\right)\)
\(\Rightarrow H=\dfrac{0,24}{0,4}.100\%=60\%\)
Đề bài có thiếu đoạn nào từ X ra Y không bạn nhỉ?

BTKL :
\(m_A=m_{C_3H_8}=8.8\left(g\right)\)
\(n_{C_3H_8}=\dfrac{8.8}{44}=0.2\left(mol\right)\)
\(\Rightarrow n_{C_3H_8\left(pư\right)}=0.2\cdot90\%=0.18\left(mol\right)\)
\(C_3H_8\underrightarrow{t^0,xt}C_aH_{2a+2}+C_bH_{2b}\left(a+b=3\right)\)
\(n_{C_3H_8\left(dư\right)}=0.02\left(mol\right)\)
\(M_A=\dfrac{8.8}{0.18\cdot2+0.02}=23.16\left(\dfrac{g}{mol}\right)\)
\(C_3H_8 \to H_2 + C_3H_6\\ C_3H_8 \to CH_4 + C_2H_4\\ C_3H_8 \to C_3H_{8\ dư}\\ m_A = m_{propan}= 8,8(gam)\\ n_{C_3H_8} = \dfrac{8,8}{44} = 0,2\\ n_{C_3H_8\ dư} = 0,2 - 0,2.90\% =0,02(mol)\\ n_A = 2n_{C_3H_8\ pư} + n_{C_3H_8\ dư} = 0,2.90\%.2 + 0,02=0,38(mol)\\ M_A = \dfrac{8,8}{0,38} = 23,167\)

Đáp án D
Crackinh 1 mol C4H10 thu được hhA gồm CH4, C2H6, C2H4, C3H6, H2 và C4H10 dư.
hhA + O2 → x gam CO2 + y gam H2O.
• Đốt cháy hhA cũng chính là đốt cháy 1 mol C4H10 ban đầu.
→ nCO2 = 1 x 4 = 4 mol; nH2O = 1 x 5 = 5 mol
→ x = 4 x 44 = 176 gam; y = 5 x 18 = 90 gam

Đáp án : D
Bảo toàn nguyên tố của một chất trước và sau phản ứng không quan trọng trung gian .
Ban đầu là C4H10 và cuối cùng là CO2 ; H2O .
Bảo toàn Nguyên tố C : 4nC4H10 = nCO2 => nCO2 = 4 mol => m = 176 g
“Vì C4H10 có 4C => 4nC4H10 ; CO2 có 1C => nCO2”
Bảo toàn nguyên tố H : 10nC4H10 = 2nH2O => nH2O = 5 mol => m = 90 g
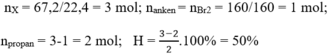
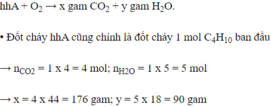
Về bản chất, đốt cháy X giống đốt cháy C3H8
\(n_{C_3H_8} = \dfrac{8,8}{44} = 0,2(mol)\\ n_{CO_2} = 3n_{C_3H_8} = 0,2.3 = 0,6(mol)\Rightarrow m_{CO_2} = 0,6.44 = 26,4(gam)\\ n_{H_2O} = 4n_{C_3H_8} = 0,2.4 = 0,8(mol)\Rightarrow m_{H_2O} =0,8.18 = 14,4(gam)\)