Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

10 ml dung dịch RSO4 cần 0,15.0,02 = 0,003 mol BaCl2
⇒ 50 ml dung dịch RSO4 cần 0,015 mol BaCl2
⇒ R + 96 = 1,8/0,015 ⇒ R = 24 là Mg ⇒ Chọn C.

10 ml dung dịch RSO4 cần 0,003 mol BaCl2
![]() 50 ml dung dịch RSO4 cần 0,015 mol BaCl2
50 ml dung dịch RSO4 cần 0,015 mol BaCl2
![]() RSO4 = 1,8/0,015
RSO4 = 1,8/0,015 ![]() R = 24
R = 24
![]() R là Mg
R là Mg
![]() Chọn C
Chọn C

Đáp án C
Ta có phương trình hóa học
2Fe + 6H2SO4đặc → t 0 Fe2(SO4)3 + 3SO2 + 6H2O
Fe + 6HNO3 → Fe(NO3)3 + 3NO2 + 3H2O
Fe + 2FeCl3 → 2FeCl2

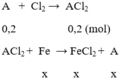
số mol FeCl2 là n = 0,25 . 0,4 = 0,1 (mol)
gọi x là số mol Fe phản ứng
khối lượng kim loại tăng là Δm = mA - mFe = Ax – 56x = 0,8
x = 0,1 → A.0,1 – 56.0,1 = 0,8 → A = 64. A là Cu
số mol Cu là nCu = 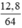 = 0,2 (mol)
= 0,2 (mol)
số mol CuCl2 → n(CuCl2) = nCu = 0,2 (mol)
nồng độ mol/l CuCl2 là C(M(CuCl2)) = 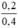 = 0,5M
= 0,5M

Giải thích: Đáp án A
Với 0,1 mol sẽ tăng 0,1 . ( MM – MMg ) = 4
=> MM = 24 + 40 = 64 => là Cu
=> Ngoài muối CuSO4 còn có thể là CuCl2 , Cu(NO3)2 (các muối tan của đồng)
(Bản chất của phản ứng là kim loại mạnh đẩy kim loại yếu ra khỏi dung dịch muối, còn gốc muối gì cũng được miễn là phải tan trong nước)
A
giải hẳn ra đc ko bạn