
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Nguyên liệu điều chế Hidro : \(Mg,Fe,Zn,...\) và dung dịch \(HCl,H_2SO_4\)
Ví dụ : \(Mg + 2HCl \to MgCl_2 + H_2\)
Nguyên liệu điều chế Oxi : \(KMnO_4,KClO_3,KNO_3,...\)
Ví dụ : \(2KMnO_4 \xrightarrow{t^o}2 KCl + 3O_2\)
*Nguyên liệu điều chế O2 trong phòng thí nghiệm : Hợp chất giàu O2 và dễ phân huỷ ở nhiệt độ cao : KMnO4 , KCLO3 hoặc KNO3
*Nguyên liệu để điều chế H2 trong phòng thí nghiệm:
- Nguyên liệu: KIm loại trước H , dung dịch axit loãng ( HCl ,H2SO4,H3PO4)

H2 : kim loại và axit
O2 : những chất giàu Oxi và dễ phân hủy : KClO3 , KMnO4 , ...

- Tính chất hoá học:
+ Phản ứng với O2 ---> nước: \(2H_2+O_2\underrightarrow{t^o}2H_2O\)
+ Phản ứng với phi kim ---> hợp chất khí (axit không có oxi):
\(H_2+Cl_2\underrightarrow{\text{ánh sáng}}2HCl\)
\(H_2+S\underrightarrow{t^o}H_2S\)
+ Phản ứng với oxit kim loại (đứng sau Al) ---> kim loại + nước:
\(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\\ Ag_2O+H_2\underrightarrow{t^o}2Ag+H_2O\)
- Điều chế:
+ Nguyên liệu: Mg, Al, Pb, Zn, Fe, HCl, H2SO4 (loãng),...
+ Phương pháp: cho kim loại + axit ---> muối + H2
\(Mg+2HCl\rightarrow MgCl_2+H_2\\ 2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ Zn+2HCl\rightarrow ZnCl_2+H_2\\ Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
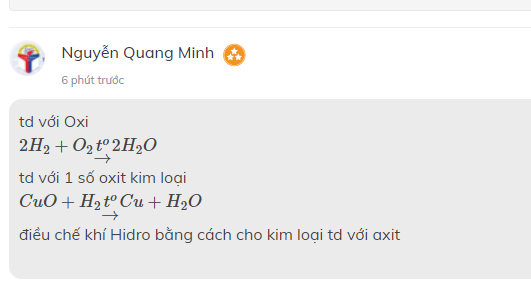
td với Oxi
\(2H_2+O_2\underrightarrow{t^o}2H_2O\)
td với 1 số oxit kim loại
\(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
điều chế khí Hidro bằng cách cho kim loại td với axit

a) bạn tự học SGK
b) Nguyên liệu điều chế O2: KMnO4, KClO3, KNO3 (độc), H2O,...
2KMnO4 -> (t°) K2MnO4 + MnO2 + O2
2KClO3 -> (t°, MnO2) 2KCl + 3O2
2KNO3 -> (t°) 2KNO2 + O2
2H2O -> (đp) 2H2 + O2
Nguyên liệu điều chế H2: Pb, Zn, Fe, Al, HCl, H2SO4 loãng,...
Fe + 2HCl -> FeCl2 + H2
2Al + 3H2SO4 ->
Al2(SO4)3 + 3H2
2H2O -> (đp) 2H2 + O2

Nguyên liệu để điều chế H 2 trong phòng thí nghiệm:
- Kim loại: Fe, Zn, Al, Mg.
- Axit: HCl, H 2 S O 4 loãng.
Nguyên liệu dể điều chế H 2 trong công nghiệp:
- Chủ yếu là khí thiên nhiên, chủ yếu là C H 4 ( metan) có lẫn O 2 và hơi nước:
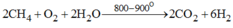
- Tách hidro tử khí than hoặc từ chế biến dầu mỏ, được thực hiện bằng cách làm lạnh, ở đó tất cả các khí, trừ hidro, đều bị hóa lỏng.


Dựa vào tính chất H2 tan rất ít trong nước.
PTHH:
Fe + H2SO4 -> FeSO4 + H2
Fe + 2HCl -> FeCl2 + H2
Zn + H2SO4 -> ZnSO4 + H2
Zn + 2HCl -> ZnCl2 + H2
2Al + 3H2SO4 -> Al2(SO4)3 + 3H2
2Al + 6HCl -> 2AlCl3 + 3H2

a. – Trong phòng thí nghiệm để điều chế H2 thường sử dụng axit HCl (hoặc H2SO4 loãng) và kim loại Zn (hoặc Fe, hoặc Al).
Zn + 2HCl → ZnCl2 + H2↑
– Khí H2 ít tan trong nước và nhẹ hơn không khí nên ta có thể thu H2 theo 2 cách: Đẩy nước và đẩy không khí.
b. – Trong phòng thí nghiệm, người ta điều chế khí oxi bằng cách đun nóng những hợp chất giàu oxi và dễ phân hủy ở nhiệt độ cao.
2KMnO4 ---t° → K2MnO4 + MnO2 + O2
2KClO3 ---t° → 2KCl + 3O2
– Khí O2 ít tan trong nước và nặng hơn không khí nên ta có thể thu O2 theo 2 cách: Đẩy nước và đẩy không khí.
refer
Điều chế khí hiđro trong phòng thí nghiệm
– Trong phòng thí nghiệm để điều chế H2 thường sử dụng axit HCl (hoặc H2SO4 loãng) và kim loại Zn (hoặc Fe, hoặc Al). – Khí H2 ít tan trong nước và nhẹ hơn không khí nên ta có thể thu H2 theo 2 cách: Đẩy nước và đẩy không khí.