Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Trong phân tử có 3 nguyên tử oxi, khối lượng là :
m O = 16 x 3 = 48 (đvC). Ta có 48 đvC ứng với 60% phân tử khối của oxit.
Như vậy 40% phân tử khối ứng với nguyên tử khối của nguyên tố R.
Nguyên tử khối của R = 48x40/60 = 32 (đvC) => Nguyên tố R là lưu huỳnh (S).
→ Công thức oxit : SO 3

a) CTHH: R2O3
\(m_{H_2SO_4}=\dfrac{294.20}{100}=58,8\left(g\right)=>n_{H_2SO_4}=\dfrac{58,8}{98}=0,6\left(mol\right)\)
PTHH: R2O3 + 3H2SO4 --> R2(SO4)3 + 3H2O
_______0,2<------0,6---------->0,2_________________(mol)
=> \(M_{R_2O_3}=\dfrac{32}{0,2}=160\left(g/mol\right)=>M_R=56\left(Fe\right)\)
b) \(m_{Fe_2\left(SO_4\right)_3}=0,2.400=80\left(g\right)\)

Gọi công thức 2 oxit là A 2 Ox và A 2 Oy, đồng thời kí hiệu A là nguyên tử khối. Ta có tỉ lệ khối lượng oxi trong 2 oxit là : 50% và 60%. Vậy tỉ lệ khối lượng A trong 2 oxit là 50% và 40%.
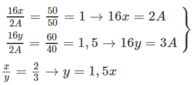
Chỉ có các cặp x, y sau có thể chấp nhận :
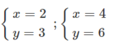
- Nếu chọn x = 2 → ta có 32 = 2A → A = 16 (loại) vì A = 16 là oxi.
- Nếu chọn x = 4 → ta có 64 = 2A → A = 32 → A là lưu huỳnh (S).
Tỉ lệ giữa các nguyên tố là tối giản, ta có hai oxit là : S O 2 và S O 2

n oxit kim loại = 116 : 232 = 0,5 mol
n H2 = 44,8 : 22,4 = 2 mol
Gọi CTHH của oxit kl là: R\(_2O_n\)
có:
\(R_2O_n+nH_2\rightarrow2R+nH_2O\)
0,5 2
có:
2 = 0,5n
=> n = 4
Vậy CTHH của oxit kim loại là Fe3O4

Sửa đề : 70% kim loại
\(CT:A_2O_3\)
\(\%A=\dfrac{2A}{2A+16\cdot3}\cdot100\%=70\%\)
\(\Leftrightarrow A=56\)
\(CT:Fe_2O_3\)
Gọi CTHH của oxit là M2O3
Ta có %mM = 70%
=> \(\dfrac{2.M_M}{2.M_M+3.16}.100\%=70\%\Rightarrow M_M=56\left(Fe\right)\)
Vậy cthh của oxit là Fe2O3
Bài này phải là 30% oxi về khối lượng thì đúng hơn

Dung dịch Ca(OH)2 không hấp thụ khí CO nên 6,72 lít khí thoát ra chính là khí CO dư.


a)Giả sử có 1 mol MO phản ứng
\(MO+2HCl\rightarrow MCl_2+H_2O\)
1----------->2----------->1----------->1
=> \(m_{ddHCl}=\dfrac{2.36,5}{10\%}=730\left(g\right)\)
\(m_{ddsaupu}=\left(M+16\right)+730=M+746\left(g\right)\)
=> \(C\%_{MCl_2}=\dfrac{M+71}{M+746}.100=12,34\)
=> M=24 (Mg)
b) Giả sử có 1 mol M2On phản ứng
\(M_2O_n+2nHCl\rightarrow2MCl_n+nH_2O\)
1---------------->2n-------------->2----------->n
=> \(m_{ddHCl}=\dfrac{2n.36,5}{10\%}=730n\left(g\right)\)
\(m_{ddsaupu}=\left(2M+16n\right)+730n=2M+746n\left(g\right)\)
=> \(C\%_{MCl_2}=\dfrac{2\left(M+35,5n\right)}{2M+746n}.100=12,34\)
Chạy nghiệm n=1,2,3
n=1 => M=12 (loại)
n=2 => M=24 (Mg)
n=3 => M=36 (loại)
\(\%_O=100-72,41=27,59\%\)
\(\Rightarrow\dfrac{Mx}{72,41}=\dfrac{16y}{27,59}\\ \Leftrightarrow1158,56y=27,59Mx\)
Với x = 3; y = 4 thì M \(\approx\) 56(Fe)
Vậy CTHH: \(Fe_3O_4\)