Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Giả sử khối lượng phân là 100g ⇒ mCa3(PO4)3 = 35 gam.
Bảo toàn nguyên tố ta có: Ca3(PO4)2 → P2O5.
⇒ mP2O5 = 35 × 142/310 = 16,03 gam.
⇒ Độ dinh dưỡng của phân bón đã cho = 16,03×100/100 = 16,03%.

Đáp án : D
Giả sử cần mg quặng => mCa3(PO4)2 = 0,95m (g)
=> Thực tế chỉ có 0,8.0,95m = 0,76m (g) Ca3(PO4)2 phản ứng
Ca3(PO4)2 -> 2H3PO4
310g 2.98g
0,76m(g) 980g
=> m = 2040g = 2,04 kg

Đáp án B
Giả sử có 100 gam quặng → mCa3(PO4)2 = 93 gam.
Ca3(PO4)2 + 2H2PO4 → Ca(HPO4)2 + 2 CaSO4 <=> P2O5
310-----------2 x 98------------------------------------142
93--------------x----------------------------------------y
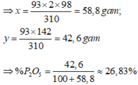

Đáp án : D
Độ dinh dưỡng của phân kali tính bằng % m K 2 O
Xét 100g phân có 55g K2O
94g K2O có lượng K trong 149g KCl
55g K2O có lượng K trong 87,18g KCl
=> %mKCl = 87,18%
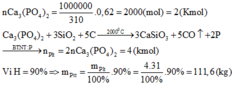


Để điều chế phân đạm NH4NO3 cần phải có NH3 và HNO3.
Từ không khí, than, nước, có thể lập sơ đồ điều chế phân đạm NH4NO3 như sau:
C + O2 → CO2: cung cấp nhiệt cho các phản ứng.
Có thể tính như sau: Trong 310 gam Ca3(PO4)2(3CaO.P2O5) có chứa x gam P2O5.
Từ đó ta tính được khối lượng P2O5: x = 142 x (35 : 310) = 16 (g)
Hàm lượng P2O5 là 6%.