Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PTHH: Fe + CuSO4 --> FeSO4 + Cu
______a------------------------------>a
=> 64a - 56a = 0,2
=> 0,025 (mol)
=> mFe(pư) = 0,025.56 = 1,4 (g)
=> mCu = 0,025.64 = 1,6 (g)

Đặt nFe(pứ)=a(mol)
PTHH Fe +CuSO4------>FeSO4+Cu
Theo phương trình =>nFe=nCu=a(mol)
mđinh sắt tăng=mcu-mFe=64a-56a=0,2(g)
=>a=0,025(mol)
=>mFe(pứ)=0,025.56=1,4(g)
mCu=0,025.64=1,6(g)

mddCuSO4 = 25.1,12 = 28g
⇒mCuSO4 = 4,2g
⇒nCuSO4 = 0,02625mol
Fe + CuSO4→→ FeSO4 + Cu
x →→ x-----------------x---------x
mtăng = 64x-56x = 0,08g
⇒ x=0,01mol
nFe(bđ)= 5/112 mol ⇒⇒ Fe dư, CuSO4 dư ( vì phản ứng ko hoàn toàn)
⇒⇒trong dd sau pứ có FeSO4=0,01mo; CuSO4=0,01625mol
mdd = mCuSO4 + mFepư - mCu = mddCuSO4 - mgiảm =28 - 0,08 = 27,92g
⇒ C% FeSO4 = 0,01(56 + 96).100/ 27,92 = 5,44%
C% CuSO4 = 0,01625.(64 + 96).100/27,92 = 9,31%

Tham khảo:
PTHH: Fe + CuSo4 ---->FeSo4 + Cu
Gọi a(mol) là số mol của Fe phản ứng
mCu - mFe = 3.5 - 2.3 = 1.2(g)
<--> 64a - 56a = 1.2
<--> 8a = 1.2
<--> a = 0.15
Dựa vào PTHH: nFe = nFeSo4 = 0.15(mol)
--> mFeSo4 = 0.15×152 = 22.8(g)

Khối lượng dung dịch CuSO 4 : m dd CuSO 4 = 1,12 x 50 = 56 (gam).
CuSO 4 + Fe → FeSO 4 + Cu
64x — 56x = 5,16 - 5 = 0,16 (gam) => x = 0,02 mol.
m CuSO 4 tham gia phản ứng = 0,02 x 160 = 3,2 (gam);
100 gam dung dịch CuSO 4 có 15 gam CuSO 4 nguyên chất.
56 gam dung dịch CuSO 4 có X gam CuSO 4 nguyên chất.
x = 56 x 15/100 = 8,4g; m CuSO 4 còn lại = 8,4 - 3,2 = 5,2g
m FeSO 4 = 0,02 x 152 = 3,04g
m dd sau p / u = 56 - 0,16 = 55,84g
C % CuSO 4 = 5,2/55,84 x 100% = 9,31%
C % FeSO 4 = 3,04/55,84 x 100% = 5,44%

\(n_{CuSO_4}=\dfrac{40.20}{100}:160=0,05\left(mol\right)\)
\(Fe+CuSO_4\rightarrow FeSO_4+Cu\)
x x x x
Gọi x là số mol Fe pứ.
có: \(64x-56x=4,5-4,2=0,3\)
<=> 8x = 0,3
=> x = 0,0375
=> \(n_{Fe\left(pứ\right)}=n_{CuSO_{4\left(pứ\right)}}=n_{FeSO_{4\left(pứ\right)}}=x=0,0375\left(mol\right)\)
Vì: \(\dfrac{0,0375}{1}< \dfrac{0,05}{1}\) nên dd \(CuSO_4\) dư sau pứ là: \(0,05-0,0375=0,0125\left(mol\right)\)
Có: \(m_{dd}=4,2+40-4,5=39,7\left(g\right)\)
\(C\%_{dd.CuSO_{4\left(sau.pứ\right)}}=\dfrac{0,0125.160.100}{39,7}=5,04\%\)
\(C\%_{dd.FeSO_4}=\dfrac{0,0375.152.100}{39,7}=14,36\%\)

Fe + CuSO4 → FeSO4 + Cu
1mol 1 mol => tăng 8 gam
x mol x mol tăng 0,8gam
=> x= 0,8:8= 0,1 mol
=> CM ( dung dịch CuSO4) = 0,1:0,2= 0,5 M
Bài 3 :
Pt : \(Fe+CuSO_4\rightarrow FeSO_4+Cu|\)
1 1 1 1
x 0,1 x
Gọi x là số mol của Fe
Vì khối lượng của sắt tăng so với ban đầu nên ta có phương trình :
\(m_{Cu}-m_{Fe}=0,8\left(g\right)\)
64x - 56x = 0,8
8x = 0,8
⇒x = \(\dfrac{0,8}{8}=0,1\)
\(n_{CuSO4}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
200ml = 0,2l
\(C_{M_{ddCuSO4}}=\dfrac{0,1}{0,2}=0,5\left(M\right)\)
Chúc bạn học tốt

a, \(Fe+CuSO_4\rightarrow FeSO_4+Cu\)
____x_______x________x_____x (mol)
b, Ta có: m lá sắt tăng = mCu - mFe
⇒ 2,58 - 2,5 = 64x - 56x
⇒ x = 0,01 (mol)
Ta có: mCuSO4 = 25.1,12 = 28 (g) \(\Rightarrow n_{CuSO_4}=\dfrac{28.15\%}{160}=0,02625\left(mol\right)\)
Theo PT: \(n_{FeSO_4}=n_{CuSO_4\left(pư\right)}=n_{Cu}=0,01\left(mol\right)\)
Có: m dd sau pư = 2,5 + 28 - 2,58 = 27,92 (g)
Dung dịch sau pư gồm: FeSO4: 0,01 (mol) và CuSO4: 0,01625 (mol)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{FeSO_4}=\dfrac{0,01.152}{27,92}.100\%\approx5,44\%\\C\%_{CuSO_4}=\dfrac{0,01625.160}{27,92}.100\%\approx9,31\%\end{matrix}\right.\)

Gọi a là số mol C u S O 4 tham gia phản ứng
Phương trình hóa học:
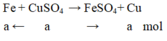
Theo đề bài ta có: m C u b á m v à o – m F e tan r a = m K L t ă n g
64a – 56a = 0,8 ⇒ a = 0,01 mol
Nồng độ dung dịch C u S O 4 là: C M = n V = 0,01 0,2 = 0,5 M
⇒ Chọn C.
Ta có PT: Fe + CuSO4 -----> FeSO4 + Cu
Gọi x là số mol Fe đã pư
=> nCu= x ( mol)
Ta có : mkim loại tăng = mCu - mFe = 64x - 56x = 4,2 - 4 = 0,2
=> x = 0,025(mol)
mFe đã phản ứng= 0,025. 56 = 1,4(g)
m\(CuSO_4\) đã phản ứng = 0,025 . 160 = 4(g)
m\(FeSO_4\) thu được = 0,025 . 152 = 3,8(g)
mCu thu được = 0,025 . 64 = 1,6(g)