Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Khối lượng dung dịch sau phản ứng:
m d d = 200 + 44 x ( g a m )
Ta có phương trình về tổng nồng độ các chất:
84. ( 2 x − 0,2 ) + 106. ( 0,2 − x ) 200 + 44 x .100 = 0,0663 ⇔ x = 0,15
Phân tử khối của muỗi đem nhiệt phân là: M = 15 0,15 = 100 ( g / m o l ) .
Vậy muối là C a C O 3
⇒ Chọn A.

tham khảo
Coi mdd H2SO4=100(gam)mdd H2SO4=100(gam)
⇒nH2SO4=100.9,8%98=0,1(mol)⇒nH2SO4=100.9,8%98=0,1(mol)
Gọi CTHH của muối cacbonat kim loại R hóa trị n là R2(CO3)nR2(CO3)n
R2(CO3)n+nH2SO4→R2(SO4)n+nCO2+nH2OR2(CO3)n+nH2SO4→R2(SO4)n+nCO2+nH2O
Theo phương trình ,ta có :
nCO2=nH2SO4=0,1(mol)nCO2=nH2SO4=0,1(mol)
nR2(SO4)n=nR2(CO3)n=nH2SO4n=0,1n(mol)nR2(SO4)n=nR2(CO3)n=nH2SO4n=0,1n(mol)
Sau phản ứng ,
mdd=0,1n(2R+60n)+100−0,1.44=0,2Rn+101,6(gam)mdd=0,1n(2R+60n)+100−0,1.44=0,2Rn+101,6(gam)
mR2(SO4)n=0,1n(2R+96n)=0,2Rn+9,6(gam)mR2(SO4)n=0,1n(2R+96n)=0,2Rn+9,6(gam)
⇒C%muối=(0,2Rn+9,6):(0,2Rn+101,6).100%=14,18%⇒C%muối=(0,2Rn+9,6):(0,2Rn+101,6).100%=14,18%
⇒R=28n⇒R=28n
Với n=1n=1 thì R=28R=28(loại)
Với n=2n=2 thì R=56(Fe)R=56(Fe)
Với n=3n=3 thì R=84R=84(loại)
Vậy kim loại R hóa trị n là FeFe hóa trị II

a)
$RCO_3 + H_2SO_4 \to RSO_4 + CO_2 + H_2O$
Theo PTHH :
$n_{RCO_3} = n_{RSO_4}$
Suy ra : \(\dfrac{12,4}{R+60}=\dfrac{16}{R+96}\)
Suy ra : R = 64(Cu)
Vậy muối là $CuCO_3$
b)
$n_{CO_2} = n_{H_2SO_4} = n_{CuSO_4} = 16 : 160 = 0,1(mol)$
$m_{dd\ H_2SO_4} = \dfrac{0,1.98}{9,8\%} = 100(gam)$
$m_{dd\ sau\ pư} = 12,4 + 100 -0,1.44 = 108(gam)$
$C\%_{CuSO_4} = \dfrac{16}{108}.100\% = 14,81\%$

a) Đặt số mol của MO, M(OH)2, MCO3 tương ứng là x, y, z.
Nếu tạo muối trung hòa ta có các phản ứng:
MO + H2SO4 →MSO4 + H2O (1)
M(OH)2 + H2SO4 →MSO4 + 2H2O (2)
MCO3 + H2SO4 →MSO4 + H2O + CO2 (3)
Nếu tạo muối axít ta có các phản ứng:
MO + 2H2SO4 →M(HSO4)2 + H2O (4)
M(OH)2 + 2H2SO4 →M(HSO4)2 + 2H2O (5)
MCO3 + 2H2SO4 →M(HSO4)2 + H2O + CO2 (6)
Ta có :
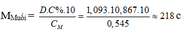
– TH1: Nếu muối là MSO4 M + 96 = 218 M = 122 (loại)
– TH2: Nếu là muối M(HSO4)2 M + 97.2 = 218 M = 24 (Mg)
Vậy xảy ra phản ứng (4, 5, 6) tạo muối Mg(HSO4)2
b) Theo (4, 5, 6) Số mol CO2 = 0,448/22,4 = 0,02 molz = 0,02 (I)
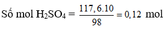
2x + 2y + 2z = 0,12 (II)
Đề bài: 40x + 58y + 84z = 3,64 (III)
Giải hệ (I, II, III): x = 0,02; y = 0,02; z = 0,02
%MgO = 40.0,02.100/3,64 = 21,98%
%Mg(OH)2 = 58.0,02.100/3,64 = 31,87%
%MgCO3 = 84.0,02.100/3,64 = 46,15%

Tham khảo
Gọi m_ddH2SO4 = 294 gam → nH2SO4 =0,6 mol
R2O3 + 3H2SO4 → R2(SO4)3 +3H2O
0,2 0,6 0,2 0,6
=> m = 294 + 9,6 + 0,4R
=> 0,2(2R + 96.3)/303,6 + 0,4R = 0,21756
=> R = 27 => R = AI
b ơi cái này người ta cho kim loại chứ k phải oxit của kim loại, mà kim loại hóa trị 2 chứ không phải 3 nha :<

Phân tử khối của mỗi chất là: M = 1,875.32 = 60
Gọi CTPT là CxHyOz
+ z = 1: 12x + y = 44
Do 0 < H ≤ 2C + 2 => 0 < y ≤ 2x+2 => 0 < 44-12x ≤ 2x+2 => 3 ≤ x < 3,67 => x = 3
CTPT là C3H8O
+ z = 2: 12x + y = 28
Do 0 < H ≤ 2C + 2 => 0 < y ≤ 2x+2 => 0 < 28-12x ≤ 2x+2 => 1,857 ≤ x < 2,33 => x = 2
CTPT là C2H4O2
- Do X, Y, Z đều có khả năng phản ứng với Na nên có chứa nhóm –OH hoặc –COOH.
- Y tác dụng với dung dịch NaHCO3 nên Y là hợp chất axit. Công thức phân tử của Y là C2H4O2. Công thức cấu tạo của Y là CH3COOH.
- Khi oxi hóa X tạo X1 có khả năng tham gia phản ứng tráng gương nên X là ancol bậc 1. Công thức phân tử của X là C3H8O. Công thức cấu tạo của X là: CH3-CH2-CH2-OH.
- Chất Z có khả năng tham gia phản ứng tráng gương nên Z có chứa nhóm chức –CHO. Công thức phân tử của Z là C2H4O2. Công thức cấu tạo của Z là HO-CH2-CHO.
Chú ý:
+ Tác dụng với Na thì trong phân tử có nhóm – OH hoặc –COOH
+ Có phản ứng tráng bạc => trong phân tử có nhóm –CHO

a/ CT oxit: $CuO$
b/ Vậy CT X: $CuSO_4.5H_2O$
Giải thích các bước giải:
Gọi công thức oxit là: $MO$
Số mol oxit là a mol
$MO+H_2SO_4\to MSO_4+H_2O$
Theo PTHH
$n_{H_2SO_4}=n_{MSO_4}=n_{MO}=a\ mol$
$⇒m_{dd\ H_2SO_4}=\dfrac{98a.100}{24,5}=400a$
$⇒m_{dd\ A}=a.(M+16)+400a = aM+416a$
$m_{MSO_4}=a.(M+96)$
Do nồng độ muối là 33,33% nên:
$\dfrac{a.(M+96)}{aM+416a}.100\%=33,33\\⇒M=64$
Vậy M là Cu, công thức oxit: $CuO$
b.
Trong 60 gam dung dịch muối A có:
$m_{CuSO_4}=\dfrac{60.33,33}{100}=20g$
Gọi công thức tinh thể tách ra là: $CuSO_4.nH_2O$
Khối lượng dung dịch còn lại là:
$60-15,625=44,375g ⇒ m_{CuSO_4\ trong\ dd}=\dfrac{44,375.22,54}{100}=10g$
$⇒m_{CuSO_4\ trong\ tinh\ thể}=20-10=10g$
$⇒n_{tinh\ thể}=n_{CuSO_4}=0,0625\ mol$
$⇒M_{tinh\ thể}=15,625:0,0625=250⇒n=5$
Vậy CT X: $CuSO_4.5H_2O$

a) Gọi công thức oxit là: MO
Số mol oxit là a mol
MO+H2SO4→MSO4+H2O
Theo PTHH
nH2SO4=nMSO4=nMO=a mol
⇒mdd H2SO4=98a.100/24,5=400a
⇒mdd A=a.(M+16)+400a=aM+416a
mMSO4=a.(M+96)
Do nồng độ muối là 33,33% nên:
a.(M+96)/aM+416a.100%=33,33⇒M=64
Vậy M là Cu, công thức oxit: CuO

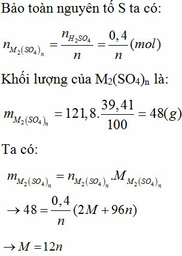

gọi dd muối CO3 là ACO3
ACO3 +H2SO4 -->ASO4 +CO2+H2O
giả sử có 1 mol ACO3
=>mACO3= MA +60(g)
theo PTHH : nH2SO4=nACO3=1(mol)
=>mdd H2SO4=1.98.100/20=490(g)
nASO4=nACO3=1(mol)
=>mASO4=MA +96(g)
nCO2=nACO3=1(mol)
=>mCO2=44(g)
=>\(\dfrac{MA+96}{MA+60+490-44}\).100=24,91
giải ra ta được MA=40(g/mol0
=>ACO3:CaCO3
ta có pthh: ACO3 +H2SO4--ASO4+H2O+CO2
(A+60)g......98g.......(A+96)g..........44g
mdd H2SO4=(98.100):20=490g
mdd muối sau phản ứng=(A+60)+490-44= (A+506)g
theo đê bài ta có:C% ASO4=(A+96).100:A+506
suy ra A=40 CÓ: CTHH :CACO3