Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

448 ml ở đktc là 0,02 mol.
Số mol ozon có trong oxi đã được ozon hoá : 0,03/16 = 0,001875 (mol) hay 0,09 (g).
Số mol oxi có trong bình : 0,02 - 0,001875 = 0,018125 (mol) hay 0,58 g.
Khối lượng của hỗn hợp : 0,09 + 0,58 = 0,67 (g).
Phẩn trăm khối lượng cua ozon trong hỗn hợp : 0,09 x 100/0,67 = 13,43%

Đáp án B
Phương trình hóa học: 2 O 3 → 3 O 2
Theo phương trình thì 2 phân tử O3 mất đi sẽ sinh ra 3 phân tử O 3 Số phân tử khí tăng = 3 - 2 = 1 => Số phân tử O3 mất đi = 2 lần số phân tử khí tăng

Phần trăm thể tích O3 trong hỗn hợp ban đầu là:
![]()

Ta có; 0,5y ứng với 2% nên y ứng với 4%
Vậy O3 chiếm 4%, O2 chiếm 96%.

Đặt số mol O2 ban đầu và số mol O3 ban đầu lần lượt là a mol và b mol.
Xét 1 mol hỗn hợp ⇒a+b=1⇒a+b=1
2O3→3O2b→1,5b2O3→3O2b→1,5b
Vì O3 đã bị phân hủy hết nên sau phản ứng:
Quảng cáo
O2 (a + 1,5b) (mol)
Số mol khí tăng thêm: (a + 1,5b) – (a + b) = 0,5b mol
Theo đề bài:
%Vtăng thêm = 0,5b.100(a+b)=2⇒b=0,04⇒a=0,940,5b.100(a+b)=2⇒b=0,04⇒a=0,94
Thành phần phần trăm thể tích các khí trong hỗn hợp đầu
%VO3=0,04.1001=4%,%VO2=96%

Đặt x và y lần lượt là số mol của O2 và O3 trong hỗn hợp
2O3 -> 3O2
y 1,5y
Trước phản ứng (x + y) mol hỗn hợp.
Sau phản ứng (x + 1,5y) mol.
Số mol tăng là (x + 1,5y) – (x + y) = 0,5y.
b) 0,5y tương ứng với 2% => y tương ứng với 4%.
Vậy thành phần phần trăm khí oxi là 96% và ozon là 4%.

PT: \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
Ta có: \(n_{KMnO_4}=\dfrac{59,25}{158}=0,375\left(mol\right)\)
Theo PT: \(n_{O_2}=\dfrac{1}{2}n_{KMnO_4}=0,1875\left(mol\right)\)
Giả sử: \(\left\{{}\begin{matrix}n_{CO}=x\left(mol\right)\\n_{CO_2}=y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow x+y=\dfrac{6,72}{22,4}=0,3\left(1\right)\)
Các quá trình:
\(C^0\rightarrow C^{+2}+2e\)
x__________ 2x (mol)
\(C^0\rightarrow C^{+4}+4e\)
y__________ 4y (mol)
\(O_2^0+4e\rightarrow2O^{-2}\)
0,1875_0,75 (mol)
Theo ĐLBT mol e, có: 2x + 4y = 0,75 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,225\left(mol\right)\\y=0,075\left(mol\right)\end{matrix}\right.\)
Ở cùng điều kiện nhiệt độ và áp suất, % số mol cũng là %V.
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CO}=\dfrac{0,225}{0,3}100\%=75\%\text{ }\\\%V_{CO_2}=25\%\end{matrix}\right.\)
Bạn tham khảo nhé!

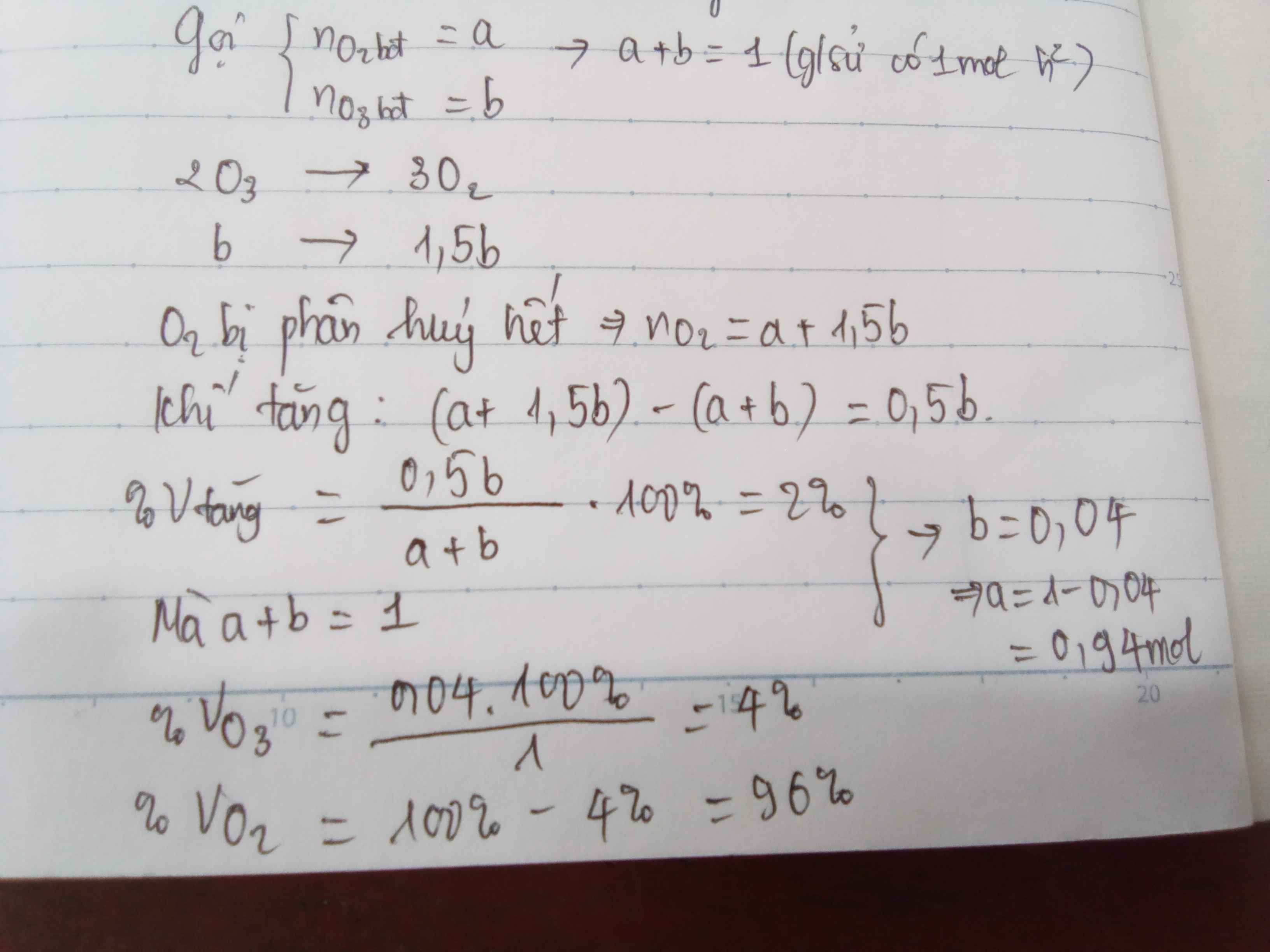
Cứ 1 mol O3 tạo thành có khối lượng nhiều hơn 1 mol O2 là:
48-32 = 16 gam.
Vậy x mol O3 tạo thành có khối lượng nhiều hơn x mol O2 là 0,04 gam