Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Qui đổi hh X về Fe, Cu, Mg, Zn và S
Gọi số mol e cho của hh kim loại là x và số mol của S là y
Ta có m kim loại = 10,42 – 32y

m kết tủa lớn nhất = mM(OH)n + mBaSO4
mM(OH)n = m kim loại + mOH- = 10,42 – 32y + 17x
n BaSO4 = nSO42- =x/2 => mBaSO4 =x/2 .233
=> m kết tủa = 10,42 – 32y + 17x + x/2.233 = 43,96 (2)
Từ (1) và (2) => x = 0,28 và y = 0,12
=> m = 10,42 – 32 . 0,12 + . 96 = 20,02

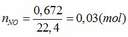
Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O (1)
a → 4a → a → a (mol)
3Fe + 8HNO3 → 3Fe(NO3)2 + 2NO + 4H2O (2)
B → 8/3b → b →2/3b (mol)
TH1: xảy ra phản ứng (1) tạo muối Fe(NO3)3 => nFe(NO3)3 = nNO = 0,03 (mol)
=> mmuối = mFe(NO3)3 = 0,03. 242 = 7,26 (g) # 7,82 => loại
TH2: xảy ra phản ứng (2) tạo muối Fe(NO3)2 => nFe(NO3)2 = 3/2 nNO = 3/2 . 0,03 = 0,045 (mol)
=> mmuối = mFe(NO3)2 = 0,045. 180 = 8,1 (g) # 7,82 => loại
TH3: xảy ra cả (1) và (2) phản ứng tạo 2 muối.
Gọi số mol của Fe ở phản ứng (1) và (2) lần lượt là a và b (mol)
Đặt vào phương trình ta có:
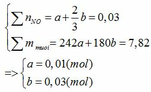
∑ nFe = 0,01 + 0,03 = 0,04 (mol) => mFe = 0,04.56 = 2,24 (g)
∑ nHNO3 pư = 4a + 8/3b = 4. 0,01 + 8/3. 0,03 = 0,12 (mol)
mHNO3 = 0,12.63 = 7,56 (g)
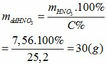
Khối lượng dd sau: mdd sau = mFe + mddHNO3 - mNO = 2,24 + 30 – 0,03.30 = 31,34 (g)
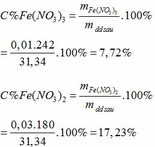

Gọi \(n_{Fe\left(X\right)}=a\left(mol\right)\)
Ta có sơ đồ phản ứng:
\(Fe+O_2\xrightarrow[]{t^o}X\left\{{}\begin{matrix}Fe\\FeO\\Fe_3O_4\\Fe_2O_3\end{matrix}\right.\xrightarrow[]{+HNO_{3\left(lo\text{ãng},d\text{ư}\right)}}Fe\left(NO_3\right)_3+NO+H_2O\)
Đặt \(n_{Fe}=a\left(mol\right)\)
BTNT Fe: \(n_{Fe\left(NO_3\right)_3}=n_{Fe}=a\left(mol\right)\)
BTNT N: \(n_{HNO_3}=3n_{Fe\left(NO_3\right)_3}+n_{NO}=3a+0,06\left(mol\right)\)
BTNT H: \(n_{H_2O}=\dfrac{1}{2}n_{HNO_3}=1,5a+0,03\left(mol\right)\)
Áp dụng ĐLBTKL:
\(m_X+m_{HNO_3}=m_{Fe\left(NO_3\right)_3}+m_{NO}+m_{H_2O}\)
\(\Rightarrow11,36+63.\left(3a+0,06\right)=242a+0,06.30+18.\left(1,5a+0,03\right)\)
\(\Leftrightarrow a=0,16\left(mol\right)\)
\(\Rightarrow m=m_{Fe}=0,16.56=8,96\left(g\right)\)

Ta có: \(n_{Fe}=\dfrac{12,6}{56}=0,225\left(mol\right)\)
Coi X gồm Fe và O.
BTNT Fe: nFe (X) = 0,225 (mol)
Ta có: \(n_{SO_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\)
BT e, có: 3nFe = 2nO + 2nSO2 ⇒ nO = 0,2625 (mol)
⇒ m = mFe + mO = 0,225.56 + 0,2625.16 = 16,8 (g)

2yAl +3FexOy -to-> 3xFe + yAl2O3 (1)
phần 1 : Fe +4HNO3 --> Fe(NO3)3 + NO +2H2O (2)
Al2O3 + 6HNO3 --> 2Al(NO3)3 +3H2O (3)
Al +4HNO3 --> Al(NO3)3 +NO +2H2O (4)
P2 : Al2O3 +2NaOH --> 2NaAlO2 +H2O (5)
2Al +2H2O +2NaOH --> 2NaAlO2 +3H2 (6)
vì khi cho phần 2 td vs NaOH dư thấy giải phóng H2 => Al dư sau (1)
nH2=0,015(mol)
nFe(P2)=0,045(mol)
giả sử P1 gấp k lần P2
=> nFe(P1)=0,045k(mol)
theo (5) : nAl(P2)=2/3nH2=0,01(mol)
=>nAl(P1)=0,01k(mol)
nNO=0,165(mol)
theo (2,4) :nNO=(0,045k+0,01k) (mol)
=>0,055k=0,165=> k=3
=>nAl(P1)=0,03(mol)
nFe(p1)=0,135(mol)
\(\Sigma nFe=0,045+0,135=0,18\left(mol\right)\)
\(\Sigma nAl=0,03+0,01=0,04\left(mol\right)\)
mAl2O3=\(14,49-0,135.56-0,03.27=6,12\left(g\right)\)
nAl2O3(P1)=0,06(mol)
=> nAl2O3(P2)=0,02(mol)
\(\Sigma nAl2O3=0,08\left(mol\right)\)
theo (1) : nFe=3x/ynAl2O3
=> 0,18=3x/y.0,08=> x/y=3/4
=>CTHH : Fe3O4
theo (1) :nFe3O4 =1/3nFe=0,06(mol)
=>m=0,04.27+0,06.232=15(g)
bạn Lê Đình Thái ơi bạn giải nhầm tìm m rồi. Cái 0,04 mol đó là mol dư, bạn phải cộng với 0,16 mol phản ứng khi xảy ra phản ứng nhiệt phân nữa.
Kết quả là m=0,2.27+0,06.232=19,32 gam

Quy đổi X thành hai nguyên tố R (x mol) và O (y mol).
nSO2 = 8,96/22,4 = 0,4 (mol)
Quá trình khử:
S+6 + 2e ---> S+4
0,8 <-- 0,4
O0 + 2e ----> O-2
y -> 2y
Quá trình oxi hóa:
R0 ----> R+3 + 3e
x --------------> 3x
Áp dụng định luật bảo toàn e:
0,8 + 2y = 3x (1)
Ta lại có:
mO2/mhh . 100% = 22,222%
<=> mO2/46,8 = 0,22222
=> mO2 \(\approx\) 10,4 (g)
=> y = nO2 = 10,4/16 = 0,65 (mol)
Thế y vào (1) ta được x = 0,7 (mol)
mR = 46,8 - 10,4 = 36,4 (g)
=> MR = 36,4/0,7 = 52 (g/mol)
=> R là Cr.

bạn dcd chữa bài này chưa