Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bài 9:
\(C_xH_y+Br_2\rightarrow C_xH_yBr_2\)
+) Từ tỉ lệ %Br trong Y \(\Rightarrow\) biện luận tìm x, y \(\Rightarrow\) CTPT của X
+) X + HBr thu được 2 sản phẩm hữu cơ \(\Rightarrow\) X bất đối xứng
Vậy CTPT là but-1-en.
Bài 10:
Anken có dạng CnH2n
\(C_nH_{2n}+Br_2\rightarrow C_{n_n}H_{2n}Br_2\)
BTKL:
\(m_A+m_{Br2}=m_{Sp}\Rightarrow m_{Br2}=4,32-1,12=3,2\left(g\right)\)
\(\Rightarrow n_{Br2}=\frac{3,2}{80.2}=0,02\left(mol\right)=n_A\)
\(\Rightarrow M_A=\frac{1,12}{0,02}=56=14n\Rightarrow n=4\)
Vậy A là C4H8
Bài 11 :
B có dạng CnH2n
\(C_nH_{2n}+Br_2\rightarrow C_nH_{2n}Br_2\)
Ta có:
\(n_{Br2}=n_B=\frac{8}{80.2}=0,05\left(mol\right)\)
\(\Rightarrow M_B=\frac{2,8}{0,05}=56=14n\Rightarrow n=4\)
Suy ra B là C4H8
Vì hidrat hóa B chỉ cho 1 ancol duy nhất
B có cấu trúc đối xứng
B có CTCT là \(CH_3-CH=CH-CH_3\)
Gọi tên: but-2-en

Đáp án B
, nCO2 = nBaCO3 = 0,2 mol
, mdd giảm = mBaCO3 – (nCO2 + nH2O) => nH2O = 0,35 mol
Xét 6,75g A phản ứng tạo 0,075 mol N2
=> Vậy 4,5 g A thì tạo 0,05 mol N2
=> nN(A) = 0,1 mol
Ta có : mA = mC + mH + mO + mN => nO = 0
=> nC : nH : nN = 0,2 : 0,7 : 0,1 = 2 : 7 : 1
=> CTĐG nhất và cũng là CTPT của A là C2H7N

Đáp án C
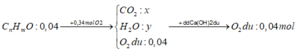
+ B T N T O : 0 , 04 + 0 , 34 . 2 = 2 n C O 2 + n H 2 O + 2 . 0 , 04 ⇒ 2 x + y = 0 , 64 ( 1 ) + n C O 2 + n H 2 O + n O 2 d u = 0 , 44 ⇒ x + y + 0 , 04 = 0 , 44 ( 2 )
⇒ n = 0 , 24 0 , 04 = 6 ; m = 0 , 16 . 2 0 , 04 = 8 ⇒ C 6 H 8 O ⇒ k = 2 . 6 + 2 - 8 2 = 3
Có 2 đặc điểm cấu tạo của X phản ứng với AgNO3 sinh ra kết tủa:
+ Liên kết ≡ đầu mạch
+ Có nhóm chức –CHO
Nếu chỉ có 1 nhóm –CHO=> mAg=0,1.108=10,8 g => loại
Nếu chỉ có lk ≡ đầu mạch => mC6H7OAg=0,05.203=10,15g<10,8g => loại
=> Chất ban đầu vừa có lk ≡ đầu mạch vừa có nhóm chức –CHO
Công thức:
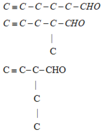
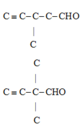
Có 5 đồng phân

Đáp án D.
BTKL:
![]()
X phản ứng với dung dịch NaOH thu được 1 muối và 1 ancol; nancol < nmuối nên có các trường hợp:
+ X chứa 1 axit và 1 ancol
![]()
![]()
![]()
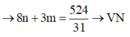
+ X chứa 1 axit và 1 este tạo bởi axit đó
![]()
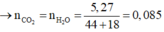
![]()
![]()
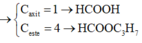

Đáp án C
Trong 100ml dd X có 0,1 mol Ba2+, 0,15 mol .
Trong 200ml dung dịch X có 0,2 mol Cl-.
Do đó trong 50 ml dung dịch X có 0,05 mol Ba2+, 0,075 mol , 0,05 mol Cl- và x mol K+
Theo định luật bảo toàn điện tích được x = 0,025
Khi cô cạn xảy ra quá trình:

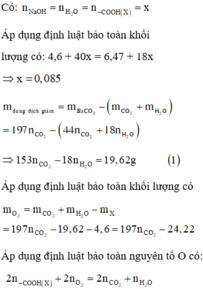
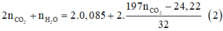
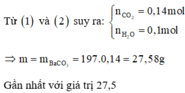

\(m_{giam}=m_{MnO2}-m_{Anken}\Rightarrow m_{Anken}=4,2\left(G\right)\)
\(n_{MnO2}=0,1\left(mol\right)\)
\(3C_nH_{2n}+2KMnO_4=4H_2O\rightarrow3C_nH_{2n}\left(OH\right)_2+2MnO_2+2KOH\)
0,15___________________________________________0,1________
\(\Rightarrow M_{Anken}=\frac{4,2}{0,15}=28=14n\)
\(\Rightarrow n=2\left(C_2H_4\right)\)
\(n_{C2H4\left(OH\right)2}=n_{C2H4}=0,15\left(mol\right)\)
\(\Rightarrow m_{C2H4\left(OH\right)2}=9,3\left(g\right)\)