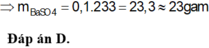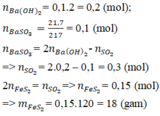Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Nồng độ phần trăm của các chất trong dung dịch :
Biết số mol NaOH (0,3 mol) nhiều hơn 2 lần số mol SO 2 (0,1 mol) vậy sản phẩm là muối Na 2 SO 3 . Ta có PTHH :
SO 2 + 2NaOH → Na 2 SO 3 + H 2 O
- Khối lượng của dung dịch sau phản ứng :
m dd = 146,6 + 3,4 = 150 (g)
- Khối lượng các chất có trong dung dịch sau phản ứng :
m Na 2 SO 3 = 126.0,1 = 12,6g
m NaOH dư = 40.(0,3 - 0,2) = 4g
- Nồng độ phần trăm các chất trong dung dịch sau phản ứng :
C % Na 2 SO 3 = 12,6/150 x 100% = 8,4%
C % NaOH dư = 4/150 x 100% = 2,67%

X + O2 → CO2 + H2O (1)
CO2 + Ca(OH)2 → CaCO3 + H2O (2)
2 CO2 + Ca(OH)2 → Ca(HCO3)2 (3)
Áp dụng ĐLBTKL ta có
\(m_{CO_2}+m_{H_2O}+m_{ddCa\left(OH\right)_2}=m_{CaCO_3}+m_{Ca\left(HCO_3\right)_2}\)
mà \(m_{Ca\left(HCO_3\right)_2}=m_{ddCa\left(OH\right)_2}\)+ 8,6
=>\(m_{CO_2}+m_{H_2O}\)= 10 + 8,6=18,6(g)
Từ (2), (3) =>\(n_{CO_2}=\dfrac{10}{100}\)+ 2. 0,5 . 0,2 = 0,3 (mol)
=> m = 0,3 .12 = 3,6 (gam)
\(m_{H_2O}\)= 18,6 - 0,3 . 44 = 5,4 (gam) => mH=\(\dfrac{5,4}{18}.2\) = 0,6 (gam)
Áp dụng ĐLBTKL ta có : mX +mO2 = mCO2 + mH2O
mX = \(18,6-\dfrac{6,72}{22,4}.32\) = 9(g)
mO = 9 – (3,6 + 0,6) = 4,8 (g)
Vậy A chứa C, H, O có công thức CxHyOz
Ta có tỷ lệ x : y : z = \(\dfrac{3,6}{12}:\dfrac{0,6}{1}:\dfrac{4,8}{16}\) = 1: 2: 1
Công thức đơn giản nhất của X có dạng (CH2O)n

Đáp án A.
2CuS + 3O2 → 2CuO + 2SO2 ↑ (1)
(mol) a → a
2ZnS + 3O2 → 2ZnO + 2SO2 ↑ (2)
(mol) b → b
SO2 + I2 + 2H2 O → H2SO4 + 2HI (3)
(mol) 0,01 0,01
Khối lượng của hỗn hợp: ZnS và CuS là:
![]()
![]()
Gọi a là số mol của CuS và b là số mol của ZnS
Ta có: 96a + 97b = 0,968
a + b = 0,01
=> a = 0,002, b = 0,008 (mol)
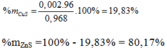

Phương trình hóa học của phản ứng:
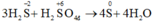
Do H2S có tính khử và H2SO4 có tính oxi hóa nên chúng có khả năng tác dụng với nhau sinh ra kết tủa vàng là S
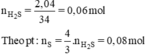
mS = 0,08 × 32 = 2,56g.

Đáp án C.
nBa(OH)2= 0,1.2 = 0,2 (mol); nBaSO3 = 0,1 (mol)
nBaSO3 = 2 nBa(OH)2 - nSO2 ⇒ nSO2 = 2.0,2 – 0,1 = 0,3 (mol)
FeS2 → 2SO2 (Bảo toàn S)
0,15 0,3 (mol)
⇒ mFeS2 = 0,15.(56+32.2) = 18 (g)