Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Sau phản ứng có Al dư do phản ứng với NaOH tạo H2
=> nAl dư = 2/3 .nH2 = 0,02 mol
Sau phản ứng có Al và Al2O3 + NaOH => NaAlO2
Bảo toàn Al ta có :
2nAl2O3 sau nung= nAl dư + 2nAl2O3 => nAl2O3 = 0,04 mol
=>nAl ban đầu = 0,1 mol
Do các phản ứng hàn toàn , mà khi nhiệt nhôm Al dư => oxit sắt hết
=>D chỉ có Fe
=>Bảo toàn e : 3nFe = 2nSO2 => nFe = 0,08 mol
Bảo toàn khối lượng : mA = mB = mFe + mAl + mAl2O3 = 9,1g
=>%mAl(A) = 29,67% gần nhất với giá trị 24%
=>A

Chọn đáp án A.
![]()
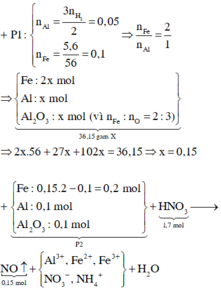
· Phần 1 + NaOH dư → 0,075 mol H2 + 5,6g Fe
n A l = 2 3 n H 2 = 0 , 05 m o l
n A l p h ả n ứ n g = n F e = 5 , 6 56 = 0 , 1 m o l
· Phần 2 + 1,7 mol HNO3 → 0,15 mol NO + m gam muối
=> HNO3 phản ứng hết.
Giả sử phần 2 có khối lượng gấp k lần phần 1.
![]()
⇒ k = 2
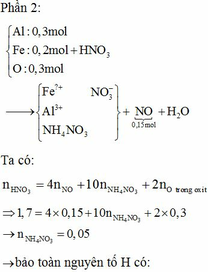
=> Phần 2 gồm: 0,2 mol Fe, 0,1 mol Al, 0,1 mol Al2O3.
Đặt a, b lần lượt là số mol của Fe2+, Fe3+ tạo thành.
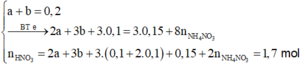
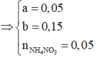
![]()
Gần nhất với giá trị 113

Chọn đáp án D
m(Mg, Fe, Cu) = 0,8a (g); mO = 0,2a (g). Đặt n H 2 S O 4 = 1 , 32 x ⇒ n N a N O 3 = 0 , 8 x
![]()
![]()
![]()
![]()
n H + = 2 n O + 10 n NH 4 + + 4 n NO ⇒ n NH 4 + = ( 0 , 264 x - 0 , 0025 a - 0 , 032 ) mol
Bảo toàn nguyên tố nitơ:
![]()
![]()
Bảo toàn điện tích: n K + + n N a + = 2 n S O 4 2 - + n N O 3 - ⇒ 1 , 22 + 0 , 8 x = 3 , 176 x + 0 , 0025 a - 0 , 048
![]()
= 183,104x + 0,91a - 3,552
⇒ 183 a = 50 x ( 183 , 104 x + 0 , 91 a - 3 , 552 )
Giải hệ có: x = 0,5mol; a = 32 (g) ⇒ b = 117 , 12 ( g )
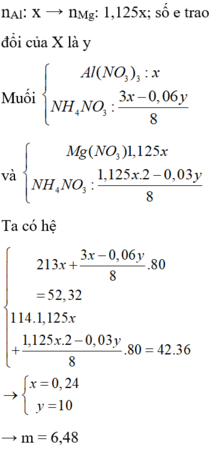
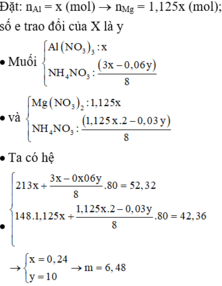
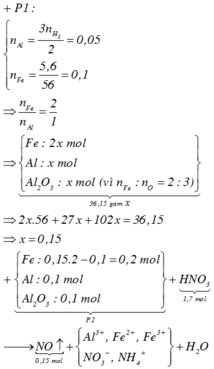
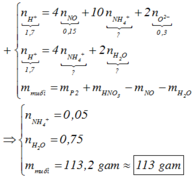

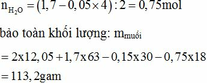

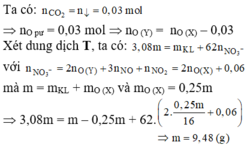
nAl: x → nMg: 1,125x; số e trao đổi của X là y
Muối
Ta có hệ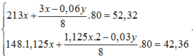
Đáp án C