Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án B
+ Loại Cu và Ag vì k tác dụng với HCl.
+ Loại Fe vì phản ứng HCl → FeCl2 và phản ứng với Cl2 → FeCl3.
⇒ Chọn B

Đáp án C
Loại B và D vì không tác dụng được với HCl.
– Xét A: Fe + 2HCl → FeCl2 + H2
2Fe + 3Cl2 → 2FeCl3 ⇒ loại.
– Xét C: Zn + 2HCl → ZnCl2 + H2
Zn + Cl2 → ZnCl2

Loại B và D vì không tác dụng được với HCl.
– Xét A: Fe + 2HCl → FeCl2 + H2
2Fe + 3Cl2 → 2FeCl3 ⇒ loại.
– Xét C: Zn + 2HCl → ZnCl2 + H2
Zn + Cl2 → ZnCl2
Đáp án C

Giải thích:
Cu, Ag không cảm ứng với dung dịch HCl
Phương trình hóa học
Mg + Cl2 → MgCl2
2Fe + 3Cl2 → 2FeCl3
Mg + 2HCl → MgCl2 + H2 ↑
Fe + 2HCl → FeCl2 + H2 ↑
Đáp án B.

Đáp án B.
Cu, Ag không cảm ứng với dung dịch HCl
Phương trình hóa học
Mg + Cl2 → MgCl2
2Fe + 3Cl2 → 2FeCl3
Mg + 2HCl → MgCl2 + H2 ↑
Fe + 2HCl → FeCl2 + H2 ↑

Đáp án B
Các kim loại tác dụng được với dung dịch H2SO4 loãng đứng trước H trong dãy điện hóa.
⇒ các kim loại thỏa mãn là Zn, Al và Fe

Đáp án C.
Gọi M là kim loại nhóm II, số mol là x
M + 2HCl → MCl2 + H2
x x(mol)
theo bài ra ta có hệ pt
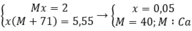
Vậy M là Ca
+ Loại Cu và Ag vì k tác dụng với HCl.
+ Loại Fe vì phản ứng HCl → FeCl2 và phản ứng với Cl2 → FeCl3.
Đáp án B