Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1/Gọi công thức oxit kim loại:MxOy
_Khi cho tác dụng với khí CO tạo thành khí CO2.
MxOy+yCO=>xM+yCO2
_Cho CO2 tác dụng với dd Ca(OH)2 tạo thành CaCO3:
nCaCO3=7/100=0.07(mol)=nCO2
CO2+Ca(OH)2=>CaCO3+H2O
0.07------------------>0.07(mol)
=>nO=0.07(mol)
=>mO=0.07*16=1.12(g)
=>mM=4.06-1.12=2.94(g)
_Lượng kim loại sinh ra tác dụng với dd HCl,(n là hóa trị của M)
nH2=1.176/22.4=0.0525(mol)
2M+2nHCl=>2MCln+nH2
=>nM=0.0525*2/n=0.105/n
=>M=28n
_Xét hóa trị n của M từ 1->3:
+n=1=>M=28(loại)
+n=2=>M=56(nhận)
+n=3=>M=84(loại)
Vậy M là sắt(Fe)
=>nFe=0.105/2=0.0525(mol)
=>nFe:nO=0.0525:0.07=3:4
Vậy công thức oxit kim loại là Fe3O4.

Dung dịch Ca(OH)2 không hấp thụ khí CO nên 6,72 lít khí thoát ra chính là khí CO dư.


3. CuO +H2SO4 -->CuSO4 +H2O
nCuO=64/80=0,8(mol)
theo PTHH :nCuO =nH2SO4=nCuSO4=0,8(mol)
=>mddH2SO4 20%=0,8.98.100/20=392(g)
mCuSO4=0,8.160=128(g)
mdd sau phản ứng =64 +392=456(g)
mH2O=456 -128=328(g)
giả sử có a g CuSO4.5H2O tách ra
trong 250g CuSO4 tách ra có 160g CuSO4 và 90g H2O tách ra
=> trong a g CuSO4.5H2O tách ra có : 160a/250 g CuSO4 và 90a/250 g H2O tách ra
=>mCuSO4(còn lại)=128 -160a/250 (g)
mH2O (còn lại)=328 -90a/250 (g)
=>\(\dfrac{128-\dfrac{160a}{250}}{328-\dfrac{90a}{250}}.100=25\)
=>a=83,63(g)

Gọi oxit kim loại là R2On Kim loại này phải có số oxh thay đổi
nCO=1,792/22,4=0,08 mol
R2On + nCO =>2 R + nCO2
0,08/n mol<=0,08 mol=>0,16/n mol
nH2=1,344/22,4=0,06 mol
2R +2mHCl =>2RClm +m H2
0,12/m mol<= 0,06 mol
=>m/n=4/3
Có 0,08/n(2R+16n)=4,64=>R=21n chọn n=8/3=>R=56 Fe
Oxit kim loại là Fe3O4
Gọi công thức oxit kim loại là :MxOy
_Tác dụng với CO:
nCO=1.792/22.4=0.08(mol)
MxOy+yCO=>xM+yCO2
0.08/y->0.08(mol)
=>nMxOy=0.08/y(1)
=>nO=0.08mol
=>mO=0.08*16=1.28(g)
=>mM=4.64-1.28=3.36(g)
nH2=1.344/22.4=0.06(mol)
2M+2nHCl=>2MCln+nH2
0.12/n----------------->0.06(mol)
=>M=3.36/0.12/n=28n
_Xét hóa trị của M từ 1->3:
+n=1=>M=28(loại)
+n=2=>M=56(nhận)
+n=3=>M=84(loại)
=>M là sắt (Fe)
=>nFe=0.12/2=0.06(mol)
=>nFexOy=0.06/x (2)
Từ(1)(2)=>
0.08/y=0.06/x
<=>0.08x=0.06y
<=>x/y=3/4
Vậy công thức oxit đầy đủ là Fe3O4

PTHH: AxOy + yCO --to--> xA + yCO2
Có: nCO(dư) + nCO2 = nCO(bd) = \(\dfrac{1,344}{22,4}=0,06\left(mol\right)\)
Mà \(\dfrac{28.n_{CO\left(dư\right)}+44.n_{CO_2}}{n_{CO}+n_{CO_2}}=20,4.2=40,8\)
=> nCO2 = 0,048 (mol)
\(n_{A_xO_y}=\dfrac{2,784}{x.M_A+16y}\left(mol\right)\)
AxOy + yCO --to--> xA + yCO2
=> \(\left\{{}\begin{matrix}n_{CO_2}=\dfrac{2,784y}{x.M_A+16y}=0,048\left(mol\right)\left(1\right)\\n_A=\dfrac{2,784x}{x.M_A+16y}\left(mol\right)\end{matrix}\right.\)
(1) => \(M_A=\dfrac{42y}{x}=>\dfrac{y}{x}=\dfrac{M_A}{42}\) (2)
PTHH: 2A + 2nHCl --> 2ACln + nH2
=> \(n_{H_2}=\dfrac{1,392xn}{x.M_A+16y}=0,036\left(mol\right)\)
=> \(1,392n=0,036.M_A+\dfrac{0,576y}{x}\) (3)
(2)(3) => MA = 28n
Xét n = 1 => L
Xét n = 2 => MA = 56 (Fe) => \(\dfrac{x}{y}=\dfrac{3}{4}\) => CTHH: Fe3O4
Xin cảm ơn mọi người đã đọc câu hỏi này nhưng em đã nghĩ ra đáp án cho bài tập này rồi ạ
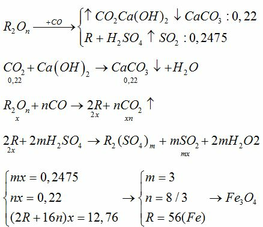
Tham khảo
* Ồ , cố lên ☺☺*
a) - Ca(OH)2 dư =) nCaCO3=nCO2= 0,07 mol
. - bảo toàn Cacbon và oxi =) nO ( oxit) = 0,07 mol
. - mM( kim loại trong oxit )= 4,06-0,07*16=2,94g
bảo toản mol e => nM=2*nH2/n=0.105/n ( n lả số oxi hóa )
=> MM=2.94/(0.105/n)=28.n
=> n =2 => M = Fe
- n Fe = 0.0525
tỉ lệ nFe : nO =3:4 =) Fe3O4
b) nFe3O4=0,0175 mol
. 10H2SO4 + 2Fe3O4 → 3Fe2(SO4)3 + 10H2O + SO2
=) n Fe2(SO4)3 = 0,02625
=) CM = 0,0525M